Биотехнология - Ю.О. Сазыкин 2006
Общая биотехнология
Биобъекты: способы их создания и совершенствования
Создание биообъектов методами генетической инженерии - Общая характеристика
Генетическая инженерия гораздо конкретнее и точнее клеточной по характеристике используемых объектов и оперирует в основном с разными по форме и размерам фрагментами клетки. Отметим, что термины «генетическая инженерия», «генная инженерия», «рекомбинантная ДНК» — равноценны.
Понятие генетической инженерии имеет очень широкий спектр и поэтому не может быть сформулировано кратко. В качестве одного из вариантов генетическую инженерию можно представить как соединение фрагментов ДНК природного и синтетического происхождения или их комбинацию in vitro с последующим введением полученных рекомбинантных структур в живую клетку для того, чтобы введенный фрагмент ДНК после включения его в хромосому либо реплицировался, либо автономно экспрессировался. Следовательно, вводимый генетический материал становится частью генома клетки.
До перечисления этапов работы генного инженера укажем, что он должен иметь в своем распоряжении:
а) генетический материал (клетку-хозяина);
б) транспортное устройство — вектор, переносящий генетический материал в клетку;
в) набор специфических ферментов — «инструментов» генной инженерии.
Принципы и методы генетической инженерии отработаны, прежде всего, на микроорганизмах; бактериях — прокариотах и дрожжах — эукариотах.
Наибольшие практические успехи генетической инженерии применительно к биотехнологии лекарственных средств достигнуты в настоящее время в области создания штаммов микроорганизмов — продуцентов видоспецифичных для человека белков. Такие белки для микробной клетки являются чужеродными, в организме же человека одни из них играют роль биорегуляторов (белковые гормоны), другие — факторов врожденного иммунитета (интерфероны и т.д.)
Стратегическая цель генного инженера — создание принципиально нового биообъекта для биотехнологического производства — микроорганизма с человеческим геном.
При выборе микроорганизма как потенциального продуцента учитывается ряд обстоятельств.
1. Поскольку микроорганизм будет выращиваться в производственных условиях в большом количестве и с ним будут контактировать многие работники предприятия (биологи, химики и др.), желательно, чтобы он не был патогенным. Кроме того, целевой генно-инженерный продукт, выделяемый из микроорганизма, должен иметь гарантии отсутствия даже следов микробных токсинов.
2. Проникший в клетку микроорганизма вектор с чужеродным для нее геном (или кластером генов) не должен расщепляться эндонуклеазами этой клетки, т.е. генетический материал должен сохраняться. При этом рибосомы потенциального продуцента должны воспринимать информационную РНК, соответствующую чужеродному материалу.
3. Образовавшийся чужеродный для клетки белок (для биотехнолога — целевой продукт) не должен расщепляться ее протеазами, т.е. не подвергаться воздействию систем репарации клетки, гидролизующих чужеродные белки. Ослабление действия таких систем также является одним из предварительных этапов работы генного инженера с продуцентом.
4. Желательно, чтобы у потенциального продуцента чужеродного белка (целевого продукта) последний выводился из клетки в питательную среду, что значительно облегчит его последующее выделение и очистку.
Предварительная работа генного инженера начинается с самого гена, кодирующего целевой белок. К этому гену присоединяется нуклеотидная последовательность, в свою очередь кодирующая так называемую лидерную последовательность аминокислот (преимущественно гидрофобных). Синтезированный в клетке целевой продукт с такой лидерной последовательностью аминокислот с их помощью проходит через липидные слои цитоплазматической мембраны из клетки наружу. Однако в этом случае клетка продуцента должна быть изменена генным инженером. В частности, в мембране должна находиться «сигнальная протеаза», отщепляющая от генного продукта лидерную последовательность аминокислот перед его выходом в среду.
Для того чтобы вектор с чужеродным геном проник в клетку, ее подвергают специальной обработке солями лития или кальция в зависимости от вида микроорганизма. В результате в стенке оболочки клетки формируются небольшого диаметра отверстия, через которые в нее проникают молекулы вектора. Обработанные таким путем клетки получили название компетентных: они способны воспринимать переносимую вектором информацию.
Важным предварительным этапом работы генного инженера является подбор вектора. Векторы, используемые при работе с микроорганизмами, конструируются чаще всего на основе умеренных фагов или плазмид. Преимущество плазмид перед фагами заключается в отсутствии лизиса клетки, возможного при работе с умеренными фагами.
При создании нового рекомбинантного продуцента ключевым моментом в работе генного инженера является встраивание гена (кластера генов) в вектор, точнее в ДНК векторной молекулы, например в плазмиду. Это становится возможным благодаря тому, что в распоряжении генных инженеров имеется большой набор разных по субстратной специфичности эндонуклеаз, получивших рабочий термин рестриктазы (от англ. restriction — разрезание). В настоящее время известны многие десятки разных рестриктаз, дифференцируемые на рестриктазы, разрезающие либо одну из двух комплементарных нитей ДНК, либо сразу обе нити.
Для биотехнолога в первую очередь представляют интерес рестриктазы, катализирующие разрез только одной нити в углеводно-фосфатной цепи ДНК. Помимо этого важно, чтобы рестриктаза, которая будет разрезать эту нить, была достаточно высоко специфична. Это значит, что последовательность нуклеотидов, обязательная для выбора данной рестриктазой места разреза углеводно-фосфатного каркаса ДНК, должна быть относительно велика. Например, часто используемая в генно-инженерных исследованиях рестриктаза EcoRI, выделенная из Е. coli (Escherichia coli — кишечная палочка) распознает нуклеотидную последовательность, если азотистые основания располагаются в ней в таком порядке: —GAATTC—; разрез (разрыв) углеводно-фосфатного каркаса одной из двух комплементарных нитей ДНК происходит между G и А. Однако вторая комплементарная нить имеет фактически одинаковую последовательность: —CTTAAG —. Поэтому рестриктаза расщепляет и вторую нить, также между G и А. Как видно из рис. 3, разрезы отстоят один от другого на четыре пары нуклеотидов. Таким образом, сохраняя свою субстратную специфичность, рестриктаза, способная к расщеплению одной нити, разрезает фактически обе, при этом разрезы находятся не напротив, а на некотором расстоянии один от другого. В результате комплементарные нити расходятся вследствие непрочности водородных связей между основаниями в каждой нуклеотидной паре и создаются однонитевые участки — согласно рабочей терминологии «липкие концы». Образно говоря, в двухнитевой ДНК появляется щель, с двух сторон которой находится по липкому концу. В эту щель может быть встроен ген — фрагмент ДНК, если он фланкирован (четко обозначен) однонитевыми участками, комплементарными однонитевым липким концам, сформированным в результате действия рестриктазы на вектор.
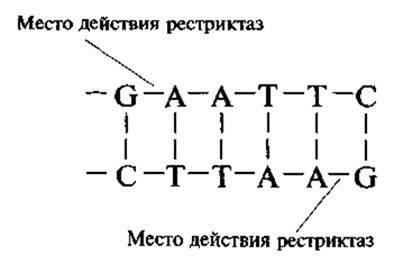
Рис. 3. Схема расщепления рестриктазой двухцепочной ДНК:
А — аденин; С — цитозин; G — гуанидин; Т — тимидин
Чтобы подготовить включение гена в вектор, надо использовать рестриктазу той же специфичности. Если для образования липких концов в векторе применялась рестриктаза EcoRl, то ее и следует применять для образования липких концов во встраиваемом фрагменте. Разумеется, липкие концы не должны образовываться в самом гене. Здесь выявляется преимущество рестриктаз, распознающих длинные последовательности по порядку расположения пар нуклеотидов.
Количество таких последовательностей в молекуле ДНК, которые обнаруживает рестриктаза, резко уменьшается по мере возрастания в них числа пар нуклеотидов. Следовательно, уменьшается возможность повредить рестриктазой сам ген, который, оказываясь между местами «посадки» молекул рестриктазы на ее субстрат — ДНК, включается в вектор в неповрежденном виде.
Другой прием, который может быть использован генным инженером — фланкирование гена синтетическими последовательностями нуклеотидов, т.е. получение методами биоорганической химии липких концов с заданным порядком нуклеотидов.
Ген (или кластер генов), встроившийся в вектор, удерживается в нем вначале только за счет водородных связей между комплементарными липкими концами. Эта стадия получила название «отжиг». Для того чтобы ген оказался прочно встроенным в вектор, необходимо его закрепление ковалентными связями. Для этих целей служат ферментылигазы (от «лиговать» — сшивать), замыкающие разрывы в углеводно-фосфатном каркасе ДНК. После этой стадии работы генного инженера вектор с прочно закрепленным в нем геном может вводиться в микробную клетку. Однако процент успешного включения вектора в клетку, как правило, крайне невелик.
Суспензия клеток микроорганизма с вектором после инкубации высевается на твердую питательную среду, а затем выросшие колонии переносятся на агаровый косяк. Полученные культуры (клоны) должны быть проверены на содержание в их клетках вектора с геном (кластером генов), кодирующим целевой продукт, например, видоспецифичный для человека белковый гормон или видоспецифичный фактор врожденного иммунитета и т. п.
Если малая частота включения в клетку вектора означает, что вектор воспринимают лишь 0,01—0,1 % клеток, то легко представить, какое огромное количество культур надо проверить, чтобы обнаружить культуру, синтезирующую целевой продукт. Для обнаружения этого продукта по его функции надо предварительно его выявить, выделить, очистить и испытать in vitro или в опытах на животных. Однако анализировать таким образом тысячи культур практически невозможно. В связи с этим разработан метод предварительного отбора клонов, содержащих вектор.
Вводится понятие гена-маркера. Такой ген легко «заявляет о себе», т.е. маркирует клетку и, соответственно, клон. Ген-маркер также встраивается в вектор, но, разумеется, с помощью другой рестриктазы, выбирающей другую последовательность нуклеотидов, так что встраивание его в «рабочий» ген заранее исключено. Ген-маркер занимает «свое» место в векторе. Этот ген не будет иметь никакого значения в будущем биотехнологическом процессе, но он нужен для отбора продуцента целевого продукта, кодируемого «рабочим» геном. Примером маркера может быть ген, кодирующий фермент беталактамазу. Этот фермент инактивирует беталактамные антибиотики, катализируя гидролиз их беталактамного кольца.
Клетки Е. coli микроорганизма, часто используемого при производстве белков человека генно-инженерным путем, проверяются на проникновение в них вектора с двумя генами — «рабочим» и «маркером»; затем их высевают на твердую питательную среду с ампициллином (антибиотиком широкого спектра действия). Так как исходная культура Е. coli чувствительна к ампициллину, то ее появление на среде в виде выросшей колонии означает, что ампициллин был разрушен беталактамазой; в свою очередь эта беталактамаза может кодироваться только геном, находящимся в векторе, так как в исходных клетках такого гена нет. Это означает, что в вектор помимо гена-маркера был включен и ген, кодирующий целевой продукт.
Далее культуру проверяют на наличие способности образовывать человеческий видоспецифический белок. Количество культур, подлежащих прямой, длительной и трудоемкой проверке, уменьшается с помощью гена-маркера в сотни раз. В результате вся работа по отбору рекомбинантных продуцентов значительно упрощается. Иногда в вектор вводятся два разных гена-маркера. Это еще более повышает результативность и точность отбора клонов с геном, кодирующим целевой продукт.
Гены у микроорганизмов соответствуют «первоначальному» или классическому представлению о гене, т. е. структурный ген — участок ДНК, переписывающийся на информационную РНК. Последняя по порядку расположения кодонов отражается на аминокислотной последовательности белка.
У эукариот большинство структурных генов в плане передачи информации функционируют иначе. Сравнительно недавно была открыта прерывистость или дискретность генов у млекопитающих и, соответственно, у человека. Эта гены содержат перемежающиеся экзоны и интроны. И те, и другие переписываются, т.е. в информационной РНК как первичном транскрипте отражены и экзоны, и интроны. Интроны из первичного транскрипта выбрасываются, а экзоны «стыкуются» один с другим. Возникает зрелая информационная РНК, которая и становится компонентом рибосомальной матричной системы. Это явление, свойственное только эукариотам, называется сплайсинг.
Таким образом, нуклеотидные последовательности нитронов информации на белки не передают. Поскольку сплайсинга в микробных клетках прокариот нет, то генные инженеры, чтобы добиться синтеза человеческого белка в клетках прокариот, должны переписать зрелую информационную РНК человеческого гена с помощью фермента обратной транскриптазы на ДНК. После этого такую укороченную ДНК (без интронов) можно использовать для включения в вектор.
Даже отдельные направления генетической инженерии составляют в настоящее время содержание фундаментальных монографий. Объем знаний в этой отрасли стремительно растет, а ее возможности быстро расширяются.