Практическая химия белка - А. Дарбре 1989
Определение С-концевой последовательности аминокислот
Определение С-концевых групп
Определение С-концевых аминокислот в виде альдегидов
О-Пивалоилгидроксиламин количественно реагирует с активированными карбодиимидом карбоксилсодержащими кислотами, образуя О-пивалоилпептидогидроксаматы (рис. 18.7) [61].
Ионизация гидроксаматной связи N-H (рKа 6,7—7,4) инициирует в пептидах перегруппировку Лоссеня, приводящую к образованию пептидилизоцианата, который в свою очередь превращается в смесь пептидилмочевин. Из раствора отбирают аликвоту, гидролизуют 6 М соляной кислотой, определяют С-концевую аминокислоту дифференциальным методом; при этом С-концевая аминокислота превращается в альдегид. Альдегид можно получить и другим путем: доводят pH до 1—2 и нагревают реакционную смесь в течение 2 ч при 50 °С.
Эту методику успешно применяли для определения С-концевых аминокислот восемнадцати ди-, три-, тетра- и пентапептидов, а также А- и В-цепей инсулина. При этом С-концевую аминокислоту определяли дифференциальным методом, хотя в некоторых случаях альдегид количественно определяли методом хроматографии на бумаге в виде 2,4-динитрофенилгидразона.
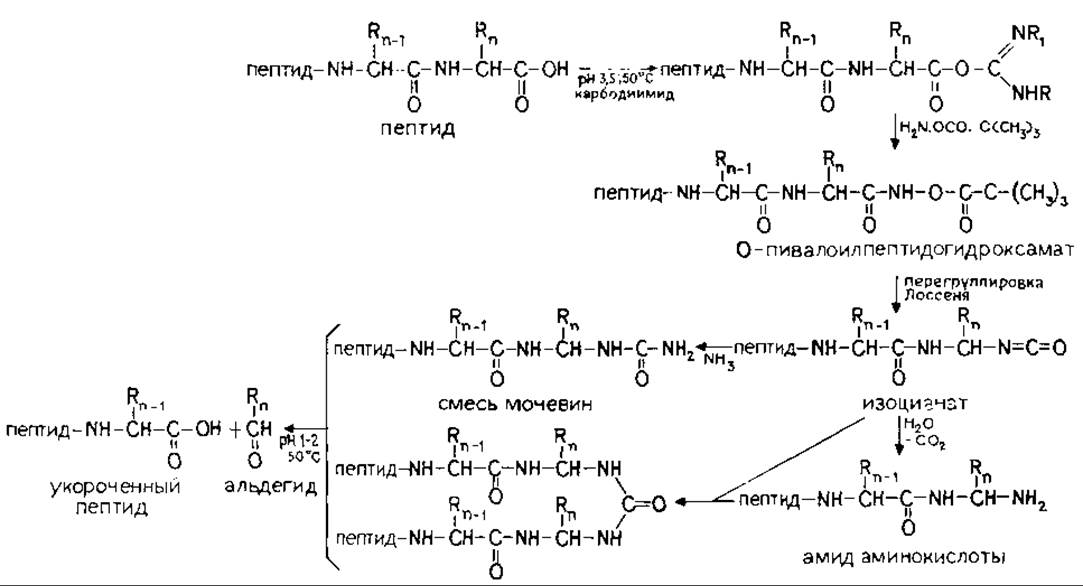
РИС. 18.7. Реакции, происходящие при С-концевом анализе с образованием альдегида. О-Пивалоилгидроксиламин количественно реагирует с С-концевой аминокислотой, активированной карбодиимидом, образуя гидроксамат. Ионизация связи N—Н гидроксамата инициирует перегруппировку Лоссеня с последующим превращением С-концевой аминокислоты в альдегид [61].
К достоинствам описанного метода можно отнести возможность использования водных растворов (и при необходимости мочевины), высокие выходы (для большинства аминокислот 70—100%) и успешное определение С-концевых Pro, Asn и, возможно, Gln. Однако для Asp и Glu наблюдаются низкие выходы (может быть, из-за образования циклических ангидридов при активации карбодиимидом), что приводит к повторному образованию исходных аминокислот при гидролизе. Кроме того, до настоящего времени метод применялся по отношению к небольшим пептидам, для которых только и имеет смысл проводить дифференциальный аминокислотный анализ.
18.3.4.1. О-Пивалоилгидроксиламин [61]. Гидрохлорид О-пивалоил гидроксил - амина (ОПГА-НСl, 154 мг, 1 ммоль) растворяют в 4 мл воды, доводят pH до 3,5 при помощи 1 М едкого натра. Добавляют раствор пептида (1 мкмоль) в 2,0 мл воды с последующим немедленным внесением 0,4 мл 0,5 М водного раствора ЭДК; поддерживают (рН-стат) pH 3,5 путем добавления 0,1 М соляной кислоты. С интервалами 15 мин добавляют порциями раствор ЭДК (3 раза по 0,4 мл). Избыток ЭДК и ОПГА-НСl «гасят» 0,5 мл 5 М формиатного буфера (pH 3,5) при перемешивании в течение 20 мин. Перегруппировка Лоссеня начинается при увеличении pH до 8,5 и температуре 50 °С. pH 8,5 поддерживается в течение 20 ч при помощи 1 М NaOH. Процесс контролируют по расходу щелочи для поддержания pH (pH-стат). Пробу (аликвоту) гидролизуют 6 М НС1 и проводят аминокислотный анализ; С-концевой статок определяют дифференциальным методом.