ЕКОЛОГІЧНА БІОХІМІЯ - Навчальний посібник - В. М. Ісаєнко 2005
Розділ 3.АЛЕЛОПАТИЧНА ВЗАЄМОДІЯ ВИЩИХ РОСЛИН
3.1. Хімічна будова алелопатнчно активних речовин
Біохімічні захисні механізми одних рослин від інших використовуються насамперед так, коли рослини одного типу конкурують із рослинами іншого. Прикладом такої взаємодії є конкуренція дерев і чагарників із трав’янистими рослинами. Водночас можлива алелопатія між рослинами одного типу, а також між окремими особинами того самого виду. Таке явище між рослинами одного виду називають автотоксичністю, або автоалелопатією.
До алелопатнчно активних належать речовини, які синтезуються рослинами чи є продуктами їх біотрансформації та метаболізму сапрофітів, що руйнують органічні речовини рослин (табл. 3.1).
Алелопатнчно активні сполуки за своєю будовою є переважно низькомолекулярними. Серед них — гідроген, синильна кислота, етерні олії, вуглеводи (ізопрен, етилен, бутилен тощо), альдегіди (оцтовий, масляний, мурашковий, пропіоновий та ін.), жирні кислоти, кетони, органічні кислоти, цитогенні та інші глікозиди, тер- пеноїди, феноли й фенольні кислоти, кумарини, хінони, флавоноїди тощо.
Таблиця 3.1.
ОСНОВНІ СПОСОБИ УТВОРЕННЯ АЛЕЛОПАТИЧНИХ РЕЧОВИН
Джерело алелопатичних речовин |
Способи утворення |
Речовини, утворені рослинами |
Леткі речовини, які випаровуються з наземних частин рослин; речовини, які виділяються корінням (ексуданти кореневих виділень); змиви з наземних частин рослин; змиви з опадів листя |
Продукти біотрансформації речовин рослин |
Продукти біотрансформації речовин опаду листя та частин рослин, які розкладаються; продукти розпаду ексудатів кореневих виділень |
Метаболіти сапрофітів (бактерій, грибів), ризоплани ризосфери тощо |
Токсини; стимулятори росту; інші різноманітні біологічно активні речовини |
Основні класи алелопатичних речовин наведено в табл. 3.2, а структурні формули деякі з них — на рис. 3.1.
Таблиця 3.2
КЛАСИ ПРИРОДНИХ РЕЧОВИН,
ДО ЯКИХ НАЛЕЖАТЬ АЛЕЛОПАТИЧНО АКТИВНІ РЕЧОВИНИ (за Телитченко, Остроумовим, 1990, зі змін.)
Клас речовин |
Алелопатичні речовини |
Органічні кислоти |
Оцтова та масляна кислота; солі оцтової, масляної та пропіо нової кислот |
Прості лактони |
Протоанемонін |
Хінони |
Юглон, плюмбагін |
Прості феноли, фенольні сполуки |
n-Оксибензойна, ванілінова, n-кумарова, ферулова кислоти |
Кумарини |
Кумарин, ескулин, псоралени, умбеліферон, скополетин |
Флавоноїди |
Флоризин, кварцетин |
Терпеноїди |
Монотерпени: лімонен, α-лінен та ін.; сесквитерпени: каріофілен тощо |
Амінокислоти |
5 -Окси-L-триптофан |
Алкалоїди |
Кофеїн |
Цианогідрини |
Дурін |
Глікозиди |
Глікозиди гірчичних олій |
Пурини |
Теофелін, параксантин, теобрамін |
Інші |
Жирні кислоти, поліацетилени, таніни |
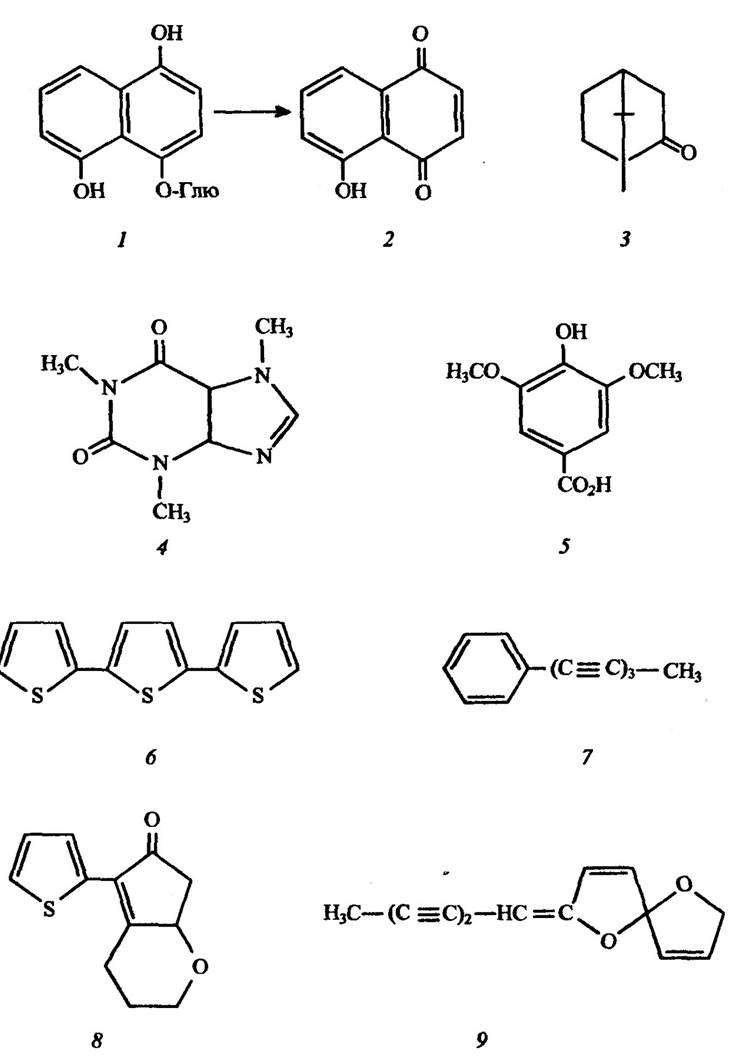
Рис. 3.1. Структура деяких алелопатичних речовин:
1 — 4-глюкозид-1,4,5-тригідрооксинафталін (зв’язана форма токсину горіха Tuglans regia); 2 — юглон; 3 — камфора; 4 — кофеїн; 5 — бузкова кислота; 6 — α-тертненил;
7 — фенілгептатриїн; 8 — хрикорин; 9 — спіран; Глю — глюкоза
Основні можливі способи утворення алелопатично активних речовин наведено на рис. 3.2.
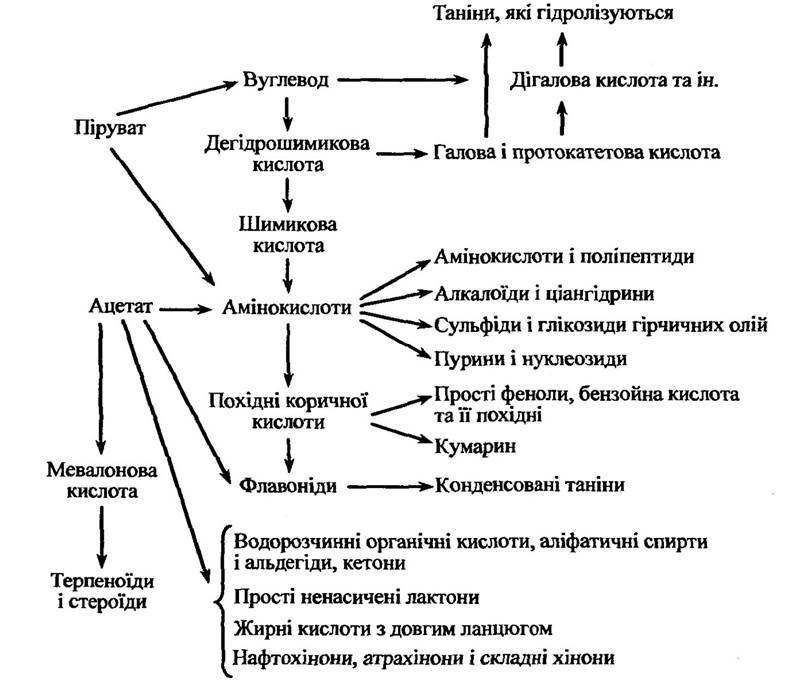
Рис. 3.2. Основні способи синтезу різних груп алелопатично активних речовин (за Райс, 1978)
Типовим прикладом алелопатії є пригнічення росту та загибель ряду рослин (томати, люцерна, картопля, злакові рослини, сосна, яблуня та ін.), які були посаджені біля європейського чорного горіха Tuglans regia. Зона токсичної дії визначається площею крони дерева та здатністю виділень із листя, погонів і гілок насичувати навколишній ґрунт. Крім цього, ця зона може бути розширена на довжину коренів горіха за рахунок виділення ними токсичних речовин.
Установлено, що горіх виділяє 4-глюкозид-1,4,5-тригідрокси- нафталін, який під час гідролізу та окиснення перетворюється в юглон (рис. 3.1). Ця сполука є водорозчинним пігментом, який зумовлює коричневий колір рук при очищенні горіхів. Оскільки її розподіл обмежений зеленими частками рослин, вона зникає в зрілих горіхах.
Юглон є не тільки інгібітором росту ряду рослин, а й проростання насіння. Особливістю дії юглону як токсину є те, що він міститься в рослині в безпечній нетоксичній формі (у вигляді попередника) і лише після його виділення з листя та пагонів і надходження в грунт він перетворюється в токсичну форму. Щоб проявляти активність, цей токсин має перебувати у ґрунті протягом певного часу навколо дерева.
Токсин юглон (його попередник) продукується не тільки Tuglans regia, але також іншими горіхами, зокрема північноамериканським чорним горіхом Juglans nigra.
Як і в інших випадках алелопатії, юглон токсичний для більшості конкуруючих видів, але не для всіх. Так, хоча більшість широколис- ткових трав і вересових кущів гине від юглону, види роду Rubus і лучний тонконіг Роа pratensis здатні рости під горіхом.
Крім юглону, існують також інші сполуки, які відіграють роль алелопатичних речовин, здатних утворюватися в результаті біотран- сформації речовини-попередника. Приклади таких речовин наведено в табл. 3.3.
Таблиця 3.3
ДЕЯКІ АЛЕЛОПАТИЧНІ РЕЧОВИНИ, ЯКІ УТВОРЮЮТЬСЯ ВНАСЛІДОК ТРАНСФОРМАЦІЇ АКТИВНИХ ПОПЕРЕДНИКІВ (за Телитченко, Остроумовим, 1990, зі змін.)
Рослина |
Попередник |
Реакція в біотрансформації |
Алелопатично активніший продукт |
Сорго |
Дурин |
Ферментативний гідроліз |
HCN, n-оксибензальдегід |
Пшениця |
Ферулова кислота |
Декарбоксилювання |
2-Метил-4-етинил-фенол |
Персик |
Амігдалін |
Ферментативний гідроліз |
HCN, бензальдегід |
Інший типовий приклад алелопатії— пригнічення кущами трав’янистих рослин в арідних і напіварідних ландшафтах. Пригнічення трав’янистих рослин у цьому разі визначається конкуренцією за воду.
Однією з таких рослин є Enceslia farinosa, що росте в пустелі Мохаве в Центральній Каліфорнії. Токсин, який викликає загибель однолітніх рослин під покровом цього чагарнику та поблизу нього, виділяється листям — це 3-ацетил-6-метоксибензальдегід (рис. 3.3).
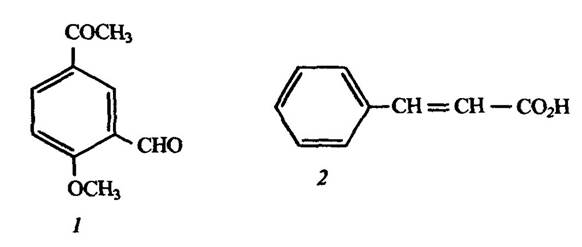
Рис. 3.3. Токсини пустельних чагарників:
1 — 3-ацетил-6-метоксибензальдегід Euceslia farinosa; 2 — корична кислота Parthenium argentatum
Водночас установлено, що чагарники Franseria dumosa та Tham- nosma montana виділяють водорозчинні токсини, які не виявляють алелопатичну дію на сусідні однолітні рослини. Це, мабуть, відбувається тому, що ці токсини розпадаються під впливом грунтових мікроорганізмів, а токсини Enceslia farinosa стійкіші до цієї дії.
Найважливішими чагарниками чапараля Південної Каліфорнії, який становить собою зону рослинності з низькою нормою опадів уздовж вузької берегової смуги, є чагарники шавлії Salvia leucophylla та полину Artemisia californica. Біля кожного з них або групи чагарників існує зона голого ґрунту від 1 м до 2 м завширшки. За цією зоною розміщена зона пригніченого росту, де обмежено ростуть лише деякі трави. Після неї тягнуться луки з характерною для них рослинністю.
Установлено, що чагарники чапаралю продукують леткі терпенові токсини (рис. 3.4), до яких належить також камфора (рис. 3.1).
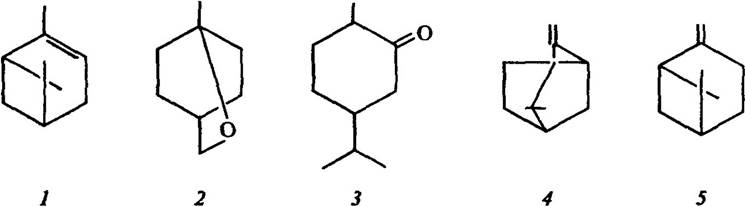
Рис. 3.4. Структура летких алелопатичних терпенів:
1 — α-пінен; 2 — 1,8-цинеол; 3 — туйон; 4 — камфен; 5 — β-пінен
У цих чагарників терпени постійно синтезуються в листі та виділяються в повітря. Вони осідають на навколишній грунт і залишаються там доти, доки дощі не активують грунтові мікроорганізми, які їх руйнують. Ці терпени здатні потрапити в клітини рослин- конкурентів через воскові покриви коренів і насіння.
У шавлії Salvia leucophylla серед різних терпенів найефективнішим є 1,8-цинеол і камфора, придатні також α- і β-пінени, камфен (рис. 3.4). У полину Artemisia californica також найефективнішими токсинами є 1,8-цинеол і камфора, містяться також туйон, ізотуйон та артемізиакетон.
Цинеол, α-феландрен, α- і β-пінен виділяють також Eucalyptus camaldulensis. Сесквитерпенові інгібітори p-кариофилен, бісаболен і хамазулен продукуються Artemisia absinthium. Альтернарієва кислота, яка продукується Altemaria solani, спричиняє буру альтернариозну плямистість різних видів пасльонових.
До стероїдів з алелопатичною та антимікробною дією належать дигітоксигенин — аглікан дигаланидів А, В і С, що синтезується Digitalis purpurea, і строфантвдин — аглікан конвалотоксин, який синтезується Convallaria majalis. Перелік наведених терпеноїдів і стероїдів, які утворюються з мевалонової кислоти (рис. 3.2) або її попередника, далеко не вичерпують усі сполуки, що проявляють алелопатичну дію.
Двома домінуючими в Каліфорнії чагарниками є також Adenos- toma fasciculatum і Arctostaphylos glandulosa, які теж проявляють алелопатичну дію на трав’янисту рослинність. Листя цих рослин не містить значної кількості терпенів. Водночас у листках продукується велика кількість водорозчинних фенольних сполук. Серед них найефективнішими інгібіторами проростання трав’янистих рослин є гідробензойна та гідроксикорична кислоти (рис. 3.5):
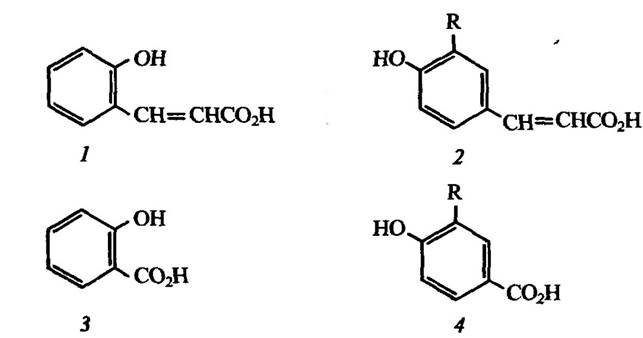
Рис. 3.5. Деякі водорозчинні алелопатичні речовини рослин:
1 — о-кумарова кислота; 2 — n-кумарова (R = Н) або ферулова (R = ОСН3) кислота;
3—саліцилова кислота; 4 — гідробензойна (R = Н) або ванілінова (R = ОСН3) кислота
Для клімату Каліфорнії характерні часті прибережні тумани, які викликають випадання вологи на листя чагарників і в навколишній ґрунт. Це сприяє регулярному перенесенню водорозчинних алелопатичних речовин з листя в ґрунт.
Алелопатичні речовини, що переносяться водою, було виявлено і в інших рослинах різних районів Землі. У дерев Quercus falcata і Liguidambar styraciflua (ростуть у Південній Каліфорнії) ідентифіковано токсини (зокрема, саліцилова кислота), які пригнічують ріст підліска в місцях надходження води з крон.
У папороті орляка звичайного (Pteridium aquilinum) продукуються водорозчинні феноли (зокрема, кавова і ферулова кислоти), які пригнічують ріст трав’янистої рослинності. У цієї рослини спостерігаються також ефекти авалелопатії, тобто пригнічення росту рослин цього самого виду.
Пригнічення росту та загибель рослин, що викликаються кореневими, а не листковими токсинами, спостерігається в каучуконоса гваюли сріблястої — Porthenium argentatum. Коріння цієї рослини виділяє токсин коричну кислоту (рис. 3.3), яка є автоалелопатичною речовиною.
До речовин, які проявляють алелопатичну дію та токсичні для рослин і інших організмів, належать небілкові амінокислоти, яких у вищих рослин знайдено понад 450. Їхня токсичність пов’язана з тим, що аміноацил-тРНК-синтетази, чутливі до цих токсинів, активують небілкові амінокислоти та не відрізняють їх від білкових. Наслідок цього — зниження синтезу білків або синтез ушкоджених білків.
Подібний вплив здійснює аналог проліну — азетидин-2-карбоксикислота, яка, як і небілкові амінокислоти, токсична не тільки для рослин, а також для інших організмів, зокрема фітофагів.
Ризобітоксин — 2-аміно-4 (2-аміно-3-оксипропокси)-транс-бут-3-єнова кислота інактивує β-цистотионазу, заважає перетворенню метіоніну в етилен і викликає хлороз молодого листя. Серед поліпептидних алелопатичних інгібіторів можна виокремити вікторин, який синтезується збудником гельмінтоспоріозу вівса Helminthosporium victoriae; карбоксин Helminthosporium carbonum; мікомаразмін Fusalium oxyspomm, який викликає прив’ядання листя томатів, та ін.
З насіння Pinus resinosa виділено малонову, цитринову і фумарову кислоти, які пригнічують проростання зооспор і ріст Pythium afertile. Листя буряку, томата, редису, корінці моркви виділяють леткі інгібітори росту, серед яких альдегіди оцтової та пропіонової кислот, ацетон, метанол і етанол. При розкладі залишків жита ідентифіковано оцтову та масляну кислоти.
Знайдено ще велику кількість рослинних інгібіторів, які проявляють алелопатичну дію найрізноманітнішої хімічної природи (див. також розд. 4). Одними з таких речовин є лактони. До простих лактонів належать и-сорбітонова кислота, яка пригнічує проростання насіння, ріст проростків, життєдіяльність деяких мікроорганізмів. Деякі види жовтцю (курячої сліпоти) Ranunculus продукують ранункулин і протоанемонін, які теж інгібують проростання насіння та ріст багатьох бактерій. Простими лактонами є також ряд антибіотиків, зокрема патулін і пеніцилова кислота гриба Penicillium сусlоріum. Патулін утворюється рядом грибів і інгібує також ріст вищих рослин.
Вищі рослини та гриби синтезують різноманітні антрахінони. Прикладом таких сполук можуть бути гельмінтоспорин Helmintho- sporium graminium, скірин Endothia parasitica та ін.
Велику групу алелопатично активних речовин становлять терпеноїди та стероїди, які утворюються з мевалонової кислоти (рис. 3.2) або її попередника. Монотерпеноїди є основними компонентами етерних олій рослин.
З дегідрошикимової кислоти утворюються галова та протокатехолова кислоти (рис. 3.2), які є фенолами. Узагалі прості феноли, бензойна й корична кислоти та їхні похідні відносяться до найпоширеніших алелопатично активних речовин. Флорогліцин і n-оксибензойна кислота утворюються при розчепленні флоридзину під час гниття залишків коріння яблуні.
У змивах колоній Arctostaphylos glandulosa виявлено гідрохінон, галову, протокатехову, ванілінову, н-оксибензойну, бузкову кислоти, арбутин.
З фенілаланіну, або тирозину, синтезуються корична кислоти та її похідні, поширені в рослинах алелопатично активними речовинами. Кумарини є лактонами о-оксикоричної кислоти з різними бічними ланцюгами. Типовими прикладами є кумарин і ескулин. Деякі похідні коричної кислоти (хлорогенова, ферулова плодів Camellia alyssum тощо) пригнічують ріст і проростання насіння. У листі яблунь знайдено n-кумарилхінну й хлорогенову кислоти. Серед інгібіторів рослин виявлено феранокумарини.
Велику групу алелопатично активних речовин становлять гідролізовані таніни, до складу яких входять талова, диталова, елагалова, хебулова, гексаоксидифенолова та інші кислоти, а також конденсовані таніни. До них належать також найрізноманітніші алкалоїди, ціангідрини, пурини й нуклеозиди, сульфіди і глікозиди гірчаної олії та ряд рослинних інгібіторів, структуру багатьох з яких ще не встановлено.
Дослідження алелопатії дає змогу виявити особливості структури рослинного світу. Так, наприклад, під час вивчення взаємодії водної
рослинності встановлено, що розкладання наземної частини ряду видів (рогозу широколистого Typha latifolia, ситнягу болотного Eleocharis palustsis, лепешняку великого Glyceriamaxima, лепехи звичайної Acorns calamus, куги озерної Schoenoplectus lacustris та ін.) пригнічує ріст паростків очерету звичайного Phragmites australis.
Алелопатичний вплив помічено також під час вивчення інших водних рослин. Так, наприклад, установлено пригнічення росту бульб Hydrilla verticillata саліциловою та галовою кислотами, інгібування росту Lemma minor флавоноїдами, похідними кумарину та іншими речовинами.
Екстракти Brasenia schreberi пригнічують розвиток ряду бактерій, а також паростків салату.
Певні алелопатичні впливи між рослинами можуть опосередковуватися тваринами. Типовим прикладом є вплив алелопатичних речовин листя евкаліпта Eucalyptus globosus (фенолів, терпенів та ін.) на ріст трав’янистої рослинності (Trifolium repers, Sinapis, Festuca rubra, Themeda australis). Ці речовини потрапляють у грунт з екскрементами жука Paropsis atomaria, який живиться листям евкаліпта.