БИОХИМИЯ И МОЛЕКУЛЯРНАЯ БИОЛОГИЯ - В. ЭЛЛИОТ - 2002
ГЛАВА 12. РЕГУЛЯЦИЯ МЕТАБОЛИЗМА УГЛЕВОДОВ И ЖИРОВ
Эта глава логически завершает все то, что было ранее изложено о метаболизме, в ней будет показано как отдельные метаболические пути пересекаются и функционируют вместе. До сих пор мы в основном изучали каждый их них отдельно. Первоначальное рассмотрение индивидуальных метаболических путей, на наш взгляд, оправданно, поскольку: 1) каждый из метаболических путей достаточно сложен, чтобы отягощать знакомство с ним еще и проблемами регуляции; 2) гораздо эффективнее изучать вопросы регуляции применительно ко всему ансамблю метаболических процессов; 3) всегда можно вернуться к уже прочитанным, изученным главам.
Хотя в регуляции нуждаются все звенья метаболизма, интеграция и управление превращениями углеводов и жиров имеют особое значение, поскольку по этим метаболическим путям идут особенно мощные потоки веществ, интенсивность и направление которых часто изменяются. Это связано с тем, что у животных периоды насыщения сменяются голодом, периоды отдыха - различными видами деятельности. Все это требует изменения направления потоков веществ, участвующих в метаболических превращениях. В то же время на примере обмена углеводов и жиров можно рассмотреть все основные принципы регуляции.
Поскольку все биохимические реакции катализируются ферментами, регуляция метаболизма в конечном итоге представляет собой регуляцию ферментативной активности. Поэтому основное внимание уделяется именно способам регуляции активности ферментов. После этого мы покажем, как регуляторные ферменты, активность которых зависит от уровня различных метаболитов, поддерживают баланс между метаболическими превращениями. Это далеко не все аспекты регуляции, ибо метаболическая активность отдельных клеток зависит от гормональных и нервных сигналов, поступающих в соответствии с нуждами всего организма. Поэтому в заключение мы разберем, как внешний по отношению к клетке сигнал регулирует метаболизм.
Зачем необходима регуляция?
Совершенно ясно, что все метаболические процессы, с которыми мы познакомились - синтез и распад гликогена, гликолиз и глюконеогенез, синтез и расщепление жиров, цикл лимонной кислоты, транспорт электронов и т. п. не могут одновременно протекать с максимальной для каждого из них скоростью. Если метаболические превращения протекают в одном направлении, то обратные превращения не должны иметь места. Скорость реакций каждого метаболического пути должна изменяться в широких пределах, в зависимости от текущих потребностей организма в энергии. Так, скорость основных реакций метаболизма у человека, играющего в теннис, увеличивается шестикратно, а при еще более тяжелой физической нагрузке - в пятнадцать раз.
Укажем на два наиболее важных момента, связанных с регуляцией реакций, ответственных за производство энергии:
✵ производство энергии должно согласовываться с постоянно меняющимися в ней потребностями;
✵ скорость и направление превращений должны подчиняться нуждам и жизненному ритму всего организма, который периодически принимает пищу и голодает, временами кормит детенышей молоком, а иногда болеет.
Еще одна, не столь очевидная необходимость регуляции - потенциальная опасность возникновения «холостых» (или субстратных) циклов.
Потенциальная опасность «холостых» циклов в метаболизме
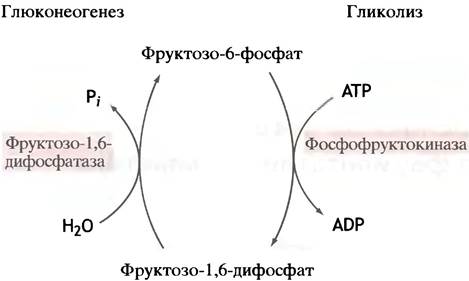
Данную проблему обсудим на примере глюконеогенеза и гликолиза. При гликолизе фруктозо-6-фосфат фосфорилируется фосфофруктокиназой во фруктозо-1,6-дифосфат, тогда как при глюконеогенезе дифосфатаза гидролизует фруктозо-1,6-дифосфат до исходного фруктозо-6-фосфата (рис. 12.1). Такая неуправляемая последовательность событий не приведет ни к чему, кроме бессмысленного перевода энергии АТР в тепло, подобно короткому электрическому замыканию (этим приемом пользуются шмели, чтобы холодным утром перед вылетом разогреть летательные мышцы).
Рис. 12.1. «Холостой» цикл на уровне гликолитической фосфофруктокиназы, который может возникнуть в отсутствие регуляторных механизмов
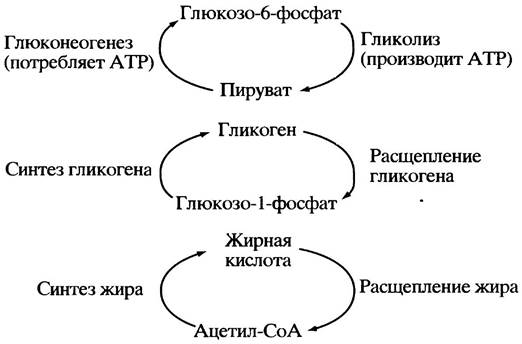
Аналогичный гигантский «холостой» цикл, занятый уничтожением АТР, мог бы объединить весь гликолиз и глюконеогенез, замыкая их друг на друга (рис. 12.2). В такие же циклы потенциально могут объединиться реакции, связанные с образованием и распадом гликогена и жиров, т. е. любые парные комбинации процессов синтеза и распада отдельных метаболитов.
Рис. 12.2. Крупномасштабные «холостые» циклы, потенциально возможные в отсутствие регуляции
Понятно, что расщепление и синтез метаболитов должны регулироваться противоположным образом: когда активируется один из этих процессов, другой должен ингибироваться. Такая регуляция возможна лишь в том случае, если синтез и расщепление протекают по разным метаболическим путям. Как мы уже отмечали, для этого оба пути должны включать по меньшей мере по одной необратимой стадии, которые катализируются разными ферментами и, следовательно, могут по-разному регулироваться. В случае же обратимых процессов прямые и обратные реакции катализируются одними и теми же ферментами, так что их раздельная регуляция невозможна.
«Холостые» циклы называют также субстратными циклами, что отражает их сущность: «объединение реакций» синтеза и распада субстрата. Хотя возникновение таких больших циклов в принципе неразумно, они, тем не менее, могут функционировать как элементы регуляторных систем. Предположим, например, что вещество А превращается в вещество С через промежуточное вещество В, причем возможна реакция В <-> А.
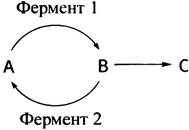
Скорость образования С можно снизить, либо ингибируя фермент 1, либо активируя фермент 2. Наибольший эффект будет достигнут, если одновременно произойдет и то, и другое. При этом для полной остановки реакции В —> С понадобится значительно меньше ингибитора фермента 1. Как будет показано ниже, именно такой тип регуляции характерен для реакции фруктозо-6-фосфат фруктозо-1,6-дифосфат.
Как регулируется активность ферментов?
Метаболическая регуляция есть не что иное, как регуляция скорости по меньшей мере одной из последовательных каталитических реакций, образующих в совокупности метаболический путь. При этом реакция необязательно должна быть химической, например, транспортные белки являются катализаторами переноса метаболитов через мембраны. Существуют два главных способа обратимо влиять на скорость ферментативных процессов в клетке.
1. Изменить количество фермента.
2. Изменить его каталитическую активность. Разумеется, существуют способы необратимой активации фермента. К ним можно отнести протеолитическое превращение трипсиногена в активный трипсин (см. с. 75). Однако в этой главе мы будем касаться только таких регуляторных механизмов, которые полностью обратимы, поскольку только они имеют существенное значение для эффективного управления метаболизмом.
Управление метаболизмом путем изменения количества ферментов
Уровень белка в клетке можно изменить, воздействуя либо на скорость его синтеза, либо на скорость его распада. Белки - короткоживущие компоненты клетки; время полураспада ферментов печени - от часа до нескольких дней.
У животных изменение количества ферментов вносит заметный вклад в регуляцию метаболизма. Такая долгосрочная регуляция реализуется в шкале часов и дней, но никак не секунд. Она используется при адаптации к новым физиологическим нуждам. Здесь можно привести множество примеров. Вспомним липопротеинлипазу кровеносных капилляров (см. с. 93). Ее количество коррелирует с потребностью ткани в липидах, увеличиваясь, к примеру, в молочных железах на период лактации. В ответ на смену диеты содержание ферментов в печени меняется в течение часов (если надо справиться с непривычной, очень жирной или изобилующей углеводами пищей). При богатом рационе в печени возрастает количество ферментов, участвующих в синтезе жиров, тогда как при голодании уже через несколько часов этот процесс обращается. При попадании в организм чужеродных химических веществ, например, лекарств, в печени быстро нарастает количество окисляющих их ферментов (см. с. 210). Еще раз подчеркнем, что у животных уровень ферментов в клетке меняется в течение нескольких часов, а то и дней, а для короткоживущих ферментов этот срок бывает меньшим. В общем случае такой способ регуляции (изменение количества фермента) используется животными лишь в тех случаях, когда возможное время ответа системы на внешнее воздействие достаточно велико.
У бактерий уровень ферментов изменяется гораздо быстрее. Если клетки Е. coli поместить в среду, где единственным источником углерода служит лактоза, то синтез фермента β-галактозидазы, гидролизующего этот сахар, начинается немедленно. Его количество становится ощутимым уже через несколько минут, а через несколько часов возрастает тысячекратно. Тем не менее это не самый быстрый ответ.
После того как потребность в ферменте пропадает, его концентрация в клетке уменьшается. Время ответа системы при этом определяется скоростью распада белков (у бактерий также разбавлением при делении), коррелируя со временем их полураспада в организме. Для оперативной автоматической регуляции метаболизма изменение количества ферментов - неподходящий способ, поскольку этот тип регуляции имеет дело только с теми ферментами, которые в данный момент присутствуют в клетке.
Управление метаболическими процессами путем изменения активности ферментов
При регуляции активности фермента изменяется не его количество, а скорость его работы. Главное в этом способе управления — его быстрота. Чтобы понять основные принципы такой регуляции, необходимо разобраться, какие факторы влияют на каталитические свойства фермента.
Основные сведения о ферментативной кинетике
Гиперболическая кинетика «классического» фермента
При ферментативном катализе субстрат (S) обратимо связывается в активном центре фермента (Е) с образованием фермент-субстратного комплекса (ЕS). После того как в пределах этого комплекса произошла химическая реакция, образовавшийся продукт (продукты, Р) высвобождается из активного центра фермента, оставляя его свободным для нового взаимодействия и реакционного цикла. Такое представление о работе фермента лежит в основе модели, предложенной Михаэлисом и Ментен для описания кинетики ферментативного катализа:
Е + S <-> ЕS —> Е + Р.
При низкой концентрации субстрата [S] скорость ферментативной реакции определяется лишь частотой столкновений молекул субстрата S и свободного фермента Е. В этой ситуации концентрация фермент-субстратных комплексов [ЕS] и скорость ферментативной реакции малы. Однако с ростом [S] количество молекул фермент-субстратного комплекса возрастает, а вместе с этим увеличивается и скорость реакции. Наступит момент, когда увеличение концентрации субстрата приведет к тому, что практически все молекулы фермента будут насыщены субстратом и превратятся в комплексы ЕS, после чего дальнейший рост [S] уже не будет сказываться на скорости ферментативной реакции. В этом случае говорят о насыщении фермента, а максимальную скорость реакции обозначают Vmах. Графически такая зависимость описывается гиперболической кривой (рис. 12.3). Такого рода кинетику называют кинетикой Михаэлиса-Ментен, а подчиняющиеся этой модели ферменты - ферментами Михаэлиса-Ментен. Долгое время они были единственными известными науке и потому получили название классических ферментов.
До сих пор мы использовали понятие низкая концентрация субстрата, что не вполне корректно, поскольку при одном и том же значении [S] один фермент будет насыщен субстратом, а другой - нет. Это зависит от прочности связывания субстрата ферментом или, как говорят, от степени сродства фермента к субстрату. Сродство может быть количественно выражено константой диссоциации фермент-субстратного комплекса или изменением свободной энергии при его образовании и зависит от природы реагирующих веществ и числа слабых связей, образующихся между ними.
Относительное сродство фермента к субстрату в большинстве случаев можно оценить, зная константу Михаэлиса Км. Этот параметр определяется как концентрация субстрата, при которой скорость ферментативной реакции составляет половину максимально возможной (см. рис. 12.3) и, как нетрудно понять, не зависит от количества фермента. (Заметим, однако, что истинное значение Км можно определить, когда скорость диссоциации комплекса ЕS на Е + S значительно выше, чем скорость распада ЕS на Е + Р.) Известно много графических методов преобразования модели Михаэлиса-Ментен, позволяющих просто и точно оценить величину Км, однако здесь мы ограничимся самым простым изложением основных принципов ферментативной кинетики, необходимых для понимания регуляторных механизмов.
Рис. 12.3. Влияние концентрации субстрата на скорость реакции (V), катализируемой ферментом, кинетика которого описывается моделью Михаэлиса-Ментен
KM- константа Михаэлиса. Пунктирная линия отражает свойства некатализируемой реакции, однако следует обратить внимание только на форму этой зависимости, но не на абсолютные значения скорости. Скорости реакций, протекаюших в клетке, были бы ничтожно малыми, если бы их не катализировали ферменты
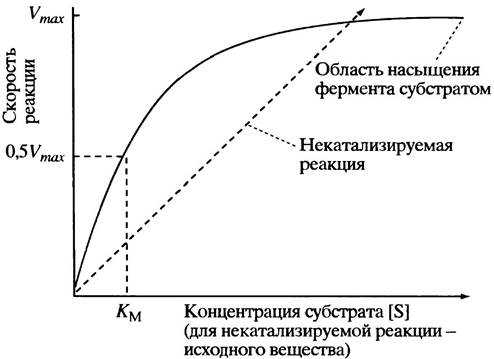
Чем больше величина KМ, тем ниже сродство фермента к своему субстрату. Следовательно, значения Км могут быть использованы для сравнения сродства различных ферментов к их субстратам. Величины Км могут варьировать в диапазоне от наномолярных до миллимолярных концентраций, но в целом они лежат в пределах 10-6--10 М. Внутриклеточная концентрация субстрата обычно соизмерима по порядку величины с Км, т. е. фермент полностью субстратом в клетке не насыщен.
Какие ферменты метаболического пути нужно регулировать?
Прямой ответ на данный вопрос таков: те ферменты, которым эволюция придала это свойство. Любой метаболический путь включает реакции, катализируемые специфическими регулируемыми ферментами. Обычно они расположены в стратегически важных местах, например, на необратимой стадии в целом обратимого процесса.
Как правило, стратегическим пунктом контроля является первый фермент метаболического пути. Рассмотрим такую последовательность реакций: А —> В —> С —> D —> Е, в которой метаболический путь заканчивается образованием нужного клетке вещества Е. Важно, чтобы Е не производился в количестве, превышающем текущие потребности в нем. Простейшей схемой автоматической регуляции этого каскада реакций будет торможение первого фермента, катализирующего превращение А —> В, конечным продуктом (Е):
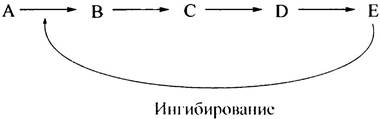
Такой эффект достигается двумя путями: ингибированием фермента и/или уменьшением его количества. Торможение именно первой стадии превращений позволяет избежать накопления промежуточных продуктов В, С и D, образующихся на последующих стадиях. Когда метаболит Е исчезает или его концентрация снижается, ингибирование прекращается, в результате чего синтез Е возобновится с новой силой. Такой тип регуляции в биохимии называется регуляцией по принципу обратной связи, или ингибированием конечным продуктом. Он часто встречается у бактерий (например, при синтезе аминокислот) и осуществляется у них с необыкновенной точностью. Однако этот тип регуляции слишком примитивен для таких сложных процессов, как метаболизм жиров или углеводов, где далеко не просто даже назвать конечный продукт. Тем не менее он позволяет регулировать метаболически разнесенные ферментативные реакции ключевыми интермедиатами (продуктами промежуточных реакций).
В ряде случаев регуляция осуществляется не конечным продуктом (по принципу отрицательной обратной связи), а исходным соединением (положительная прямая связь), которое активирует ферменты, участвующие в его превращении в данном метаболическом пути.
Природа регуляторных ферментов
Известны два основных способа регуляции каталитической активности ферментов (изменение их количества не рассматривается).
1. Аллостерическая регуляция.
2. Ковалентная модификация белка - обычно фосфорилирование и дефосфорилирование.
Рассмотрим оба эти способа.
Аллостерическая регуляция ферментов
Аллостерическая регуляция ферментов особенно важна при управлении метаболизмом. Приставка алло- означает другой. Она подразумевает, что на ферменте кроме участка связывания субстрата есть по меньшей мере еще один (их может быть несколько) участок связывания другого соединения (или соединений). Низкомолекулярные соединения, связываемые белком, принято называть лигандами; этот термин часто распространяют и на небольшие белки. Лиганды, связывающиеся с аллостерическими участками, называют аллостерическими эффекторами, или аллостерическими регуляторами. Они обычно не похожи на субстрат. Действие эффекторов, как правило, наблюдают при определенной концентрации субстрата. Положительные эффекторы при связывании с аллостерическим участком фермента увеличивают его активность, отрицательные - ее понижают. Иными словами, аллостерические эффекторы можно подразделить на активаторы и ингибиторы.
В некоторых случаях аллостерические ингибиторы снижают скорость ферментативной реакции, уменьшая Vmах. Чаще, однако, их действие проявляется в уменьшении сродства фермента к субстрату. Выше отмечалось, что ферменты в клетке обычно работают, когда концентрация субстратов ниже насыщающей. Поэтому уменьшение сродства субстрата к ферменту приводит к снижению активности последнего, а увеличение сродства, наоборот, к его активации. При насыщающих фермент концентрациях субстрата аллостерические эффекторы не изменяют Vmах, даже если сродство фермента к субстрату изменяется. Однако в реальных условиях,
когда концентрации субстратов в клетке по большей части далеки от насыщающих, эффекторы могут влиять на величину скорости реакции.
Механизм аллостерической регуляции ферментов
Мы обсудим сейчас природу аллостерических ферментов, для которых связывание эффектора отражается на сродстве фермента к субстрату (это основной тип аллостерической регуляции ферментов). Такие аллостерические ферменты состоят из нескольких каталитически активных белков, которые посредством нековалентных связей объединены в единый ферментный комплекс. Компоненты такого комплекса называют белковыми субъединицами, протомерами или мономерами. Хотя каждая из субъединиц обладает каталитической активностью, общая активность фермента зависит от их взаимодействия друг с другом. Типичные кривые зависимости скорости ферментативной реакции от концентрации субстрата представлены на рис. 12.4. Аллостерический фермент отличается от «классического» тем, что его кривая имеет не гиперболическую, а сигмоидную форму (ее также называют S-образной). Что из этого следует и почему так получается?
Рис. 12.4. Влияние концентрации субстрата на скорость реакции (1), катализируемой типичным аллостерическим ферментом. Пунктирной линией для сравнения показана соответствующая кривая для «классического» фермента, подчиняющегося кинетике Михаэлиса-Ментен. Поскольку понятие Км не имеет физического смысла вне модели Михаэлиса-Ментен, здесь используется обозначение К0,5
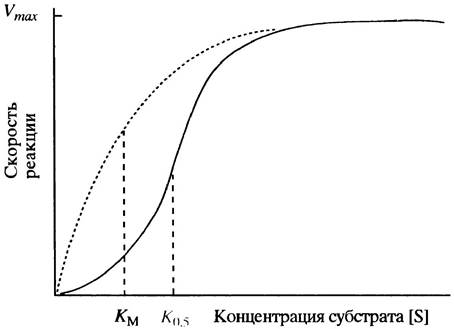
Ответим на первый вопрос. Когда аллостерический активатор связывается ферментом, сигмоидная кривая сдвигается влево, тогда как аллостерический ингибитор сдвигает ее вправо (рис. 12.5). Сдвиг кривой влево свидетельствует об увеличении сродства фермента к субстрату, а сдвиг вправо - о его уменьшении. Сигмоидная форма кривой, отражающей зависимость скорости ферментативной реакции от концентрации субстрата, указывает на то, что скорость реакции более чувствительна к изменению концентрации субстрата, чем при гиперболической зависимости, особенно в области скоростей, близких к 0,5 Vmах.
Рис. 12.5. Влияние концентрации субстрата на скорость реакции (V), катализируемой типичным аллостерическим ферментом. V1, V2 и V3 - скорости реакции соответственно без лиганда, в присутствии аллостерического активатора и аллостерического ингибитора при фиксированной концентрации субстрата S (К0,5)
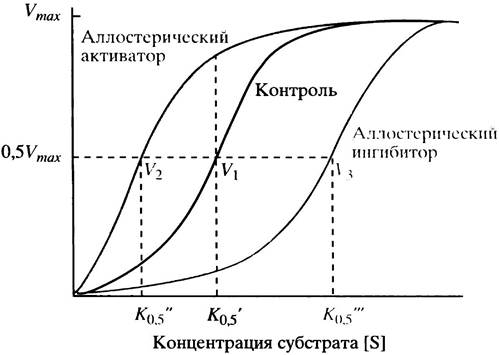
Почему зависимость скорости реакции от концентрации субстрата приобретает сигмоидную форму? Взаимодействие одной из субъединиц аллостерического фермента с субстратом способствует лучшему связыванию молекул субстрата другими субъединицами. Такой эффект называют гомотропным кооперативным связыванием субстрата.Термин гомотропный отражает то обстоятельство, что все субъединицы связывают один и тот же лиганд - субстрат. Поскольку в данном случае сигмоидная форма кривой обусловлена только связыванием субстрата, такую регуляцию не совсем верно интерпретировать как результат аллостерического конформационного изменения (предполагающего взаимодействие эффектора с участком, отличным от каталитического). Однако кооперативность часто относят к аллостерическим эффектам несмотря на то, что участки связывания лиганда и субстрата идентичны. По-видимому, кооперативное взаимодействие можно считать аллостерическим, так как связывание субстрата каждой из субъединиц зависит от присутствия лиганда на соседней субъединице.
Каков механизм взаимного влияния участков связывания различных субъединиц? Предложены две теоретические модели, согласно которым участок связывания субстрата может находиться в двух состояниях, различающихся по сродству к субстрату. Назовем их состояниями с высоким и низким сродством. Предполагается, что связывание субстрата увеличивает долю субъединиц с высоким сродством к субстрату. Обе модели различаются деталями распространения взаимовлияния субъединиц в пределах единого белкового комплекса.
В рамках согласованной модели, предложенной Моно, Уайменом и Шанже (рис. 12.6), все субъединицы могут одновременно находится либо в состоянии с высоким сродством, либо с низким. Обе формы белкового комплекса при этом находятся в динамическом равновесии, которое сдвинуто в сторону белка с низким сродством субъединиц. Связывание субстрата с любой субъединицей сдвигает это равновесие в противоположную сторону - к образованию белка с высоким сродством. Таким образом, с ростом концентрации субстрата все большее число молекул фермента переходит в состояние с высоким сродством.
Рис. 12.6. Модель «согласованного» кооперативного связывания субстрата. Согласно этой модели, фермент существует в двух состояниях - Т и R, находящихся в равновесии, которое, однако, в отсутствие субстрата сдвинуто в сторону формы Т. В случае связывания молекул субстрата с формой R равновесие сдвигается вправо, что увеличивает сродство к субстрату всех субъединиц в этой молекуле. Обозначения Н (High) и L (Low) указывают на сродство фермента к субстрату
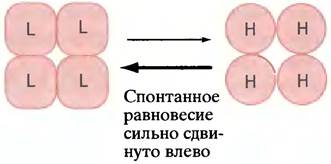
Заметим, что все сказанное относится к кооперативному связыванию субстрата, а не к аллостерическим модификаторам или эффекторам, регулирующим фермент. Это особый вопрос. Согласно данной модели, аллостерические регуляторы изменяют положение равновесия между состояниями молекулы с низким сродством (его обозначают буквой Т, от англ. tense - напряжение, т. е. напряженное состояние) и высоким сродством (обозначаемым буквой R, от англ. relaxed, т. е. расслабленное состояние). Если аллостерический регулятор более прочно связывается с ферментом в состоянии R, он будет смещать равновесие T <-> R вправо. Это приведет к активации фермента, так как большее число его молекул при данной концентрации субстрата будет в форме R. По мере увеличения концентрации положительного аллостерического регулятора все больше молекул фермента перейдет в состояние R (с высоким сродством), а кривая зависимости скорости реакции от концентрации субстрата станет гиперболической. Обратная ситуация возникает, когда регулятор отрицательного типа более прочно связывается с молекулами фермента в состоянии Т и переводит другие молекулы в это же состояние, уменьшая скорость ферментативной реакции в целом.
Последовательную модель разработали Кошланд, Немети и Филмер. Они предположили, что в отсутствие субстрата все молекулы фермента находятся в состоянии Т с низким сродством. Равновесия между состояниями Т и R нет (поскольку нет состояния R). Связывание молекулы субстрата с одной субъединицей вызывает изменение ее конформации (от Т к R), а также конформации соседней субъединицы, увеличивая ее сродство к молекуле субстрата, которому теперь легче с ней связаться. Связывание второй молекулы субстрата будет способствовать переходу третьей субъединицы в состояние R, и этот процесс будет повторяться до тех пор, пока все субъединицы фермента не перейдут в состояние R с высоким сродством (рис. 12.7).
Рис. 12.7. Модель «последовательного» кооперативного связывания субстрата аллостерическим ферментом. Связывание одной молекулы субстрата с субъединицей вызывает конформационное изменение последней. Это облегчает конформационную перестройку второй субъединицы при взаимодействии её со следующей молекулой субстрата и т. д. Суммарный эффект заключается в изменении общей конформации белка

Обе модели удовлетворительно объясняют наблюдаемые эффекты, их нельзя рассматривать как взаимоисключающие. Истинный механизм аллостерической регуляции вполне может оказаться промежуточным.
Некоторые ферменты, например, глицеральдегид- 3-фосфатдегидрогеназа (см. с. 112), проявляют кооперативность при связывании субстрата, однако для них неизвестны аллостерические регуляторы. Такие ферменты более чувствительны к изменениям концентрации субстратов, чем классические, и, возможно, именно это служит причиной кооперативного связывания. В дальнейшем мы встретимся с более сложным вариантом аллостерической регуляции, когда участок связывания
регулятора расположен на отдельной регуляторной субъединице, лишенной каталитических свойств. Связывание аллостерического регулятора с этим участком приводит к тому, что регуляторная субъединица покидает комплекс, а каталитические субъединицы изменяют сродство к субстрату. Такое управление ферментативной реакцией может показаться чрезмерно громоздким, но эволюция прежде всего заботится о надежности и работоспособности системы.
Обратимость аллостерической регуляции
Наиболее важной особенностью аллостерической регуляции является ее мгновенное действие. Аллостерический лиганд практически мгновенно связывается с регуляторным центром за счет нековалентных взаимодействий. Регулятор диссоциирует из комплекса с ферментом, когда его концентрация в среде уменьшается; при этом фермент возвращается в исходное состояние.
Аллостерическая регуляция - метаболическая концепция огромной мощности
Существенным в аллостерической регуляции является тот факт, что эффектор по своему строению может не иметь ничего общего ни с субстратом данного фермента, ни с любым другим веществом, образующимся в процессе метаболических превращений. Это означает, что любой метаболический путь может быть регуляторно связан с любым другим. Метаболит(ы) одного из каскадов биохимических превращений может(гут) быть регулятором(ами) другого. Более того, фермент может управляться не одним, а несколькими регуляторами, каждому из которых отведен специфический участок связывания, и получать таким образом регуляторные сигналы от нескольких метаболических путей, что увеличивает гибкость регуляции.
Мы уже познакомились с тем, как сложны и взаимозависимы метаболические пути, так или иначе связанные с производством и хранением энергии. В такой сложной системе каждый отдел должен «знать», как дела у «соседей», оценивая уровень ключевых метаболитов. Достаточно АТР или нет? Поставляется ли циклу лимонной кислоты нужное количество ацетил-СоА? Протекает ли гликолиз слишком быстро или недопустимо медленно? Представьте, какой химический хаос воцарится, если каждый метаболический путь не будет ежесекундно подстраиваться к текущей ситуации, исходя из информации, поступающей от других метаболических путей или различных участков собственного пути! Принцип аллостерической регуляции открыл для эволюции возможность создавать множество информационных каналов, которые позволяют ферментам получать сигналы из любой точки на метаболической карте. Как заметил Моно, один из первооткрывателей аллостерической регуляции, без нее просто невозможно существование столь сложной системы, как клетка. Он называл аллостерическую регуляцию «вторым секретом жизни» (первый - ДНК).
Роль фосфорилирования в регуляции ферментативной активности
Теперь приступим к рассмотрению второго метода регуляции ферментов - фосфорилирования. Строго говоря, следовало бы посвятить этот раздел более общей проблеме регуляции за счет ковалентной модификации ферментов. Однако фосфорилирование имеет настолько важное значение, что обсуждение этого процесса отдельно вполне оправданно.
Принцип предельно прост. Существуют ферменты, называемые протеинкиназами, которые переносят остаток фосфата с АТР на соответствующий белок. При этом изменяется конформация фосфорилированного белка и, как следствие, его каталитические свойства. Мишенью для фосфорилирования может быть не только фермент, но и регуляторный белок - ингибитор или активатор фермента. В этом случае фосфорилирование влияет на его регуляторные свойства. Нет ничего удивительного в том, что введение сильно заряженной группы отражается на структуре белковой молекулы. С другой стороны, фосфатные остатки легко отщепляются протеинфосфатазами (рис. 12.8).
Рис. 12.8. Регуляция активности фермента посредством его фосфорилирования. В разных случаях фосфорилированный фермент может быть либо более, либо менее активным, чем нефосфорилированный. Возможна также регуляция фермента с помощью ингибиторного белка, активность которого меняется при его фосфорилировании
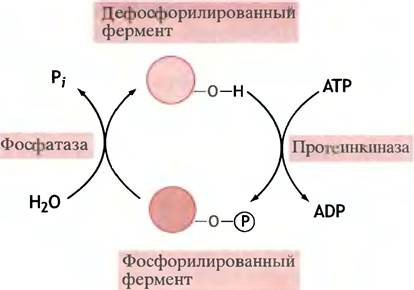
Фосфорилированию подвергаются гидроксильные группы отдельных остатков серина и треонина в полипептидной цепи фермента, которые киназа различает по их аминокислотному окружению (в главе 26 описано фосфорилирование тирозина, в данном разделе мы этого вопроса касаться не будем).
На схеме показана гидроксильная группа серина, подвергающаяся фосфорилированию:
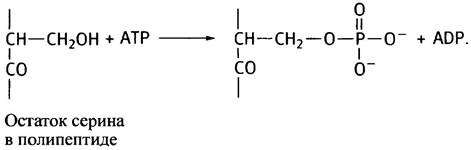
Итак, мы познакомились с двумя основными механизмами, регулирующими активность ферментов - аллостерической регуляцией и обратимым фосфорилированием. Теперь следует рассмотреть, как эти механизмы используются для регуляции метаболизма.
Регуляция отдельных метаболических путей
Два типа управления - внутреннее и внешнее, или внеклеточное
Аллостерическая регуляция ферментов осуществляется при непосредственном участии фермента и субстрата, тогда как при регуляции с помощью фосфорилирования активность фермента-мишени зависит от соотношения киназ и фосфатаз. Чем же определяется это соотношение? В большинстве случаев (хотя и не всегда) оно определяется гормональным сигналом, поступающим с наружной стороны клетки.
Управление метаболизмом - сложный комплексный процесс. Чтобы сделать его рассмотрение более доступным, разделим материал на два обширных раздела. Сначала мы расскажем о внутриклеточной регуляции, которая координирует взаимодействие метаболических путей и отдельных их участков внутри отдельной клетки, чтобы избежать дефицита или перепроизводства необходимых веществ. На этом уровне регуляторными сигналами служат сами метаболиты, а управление обычно (хотя далеко не всегда) осуществляется посредством аллостерической регуляции. В одних случаях при этом используется принцип обратной связи, который, например, не позволяет гликолизу производить больше пиру- вата, чем его способен переработать цикл лимонной кислоты. В других случаях, напротив, регуляция по принципу положительной связи позволяет удаленным по цепи превращений метаболическим звеньям справиться с нарастающим потоком субстратов.
Полностью изолированная клетка могла бы довольствоваться внутренним управлением метаболическими процессами. Однако в организме функционируют системы внешнего управления жизнедеятельностью клеток (разумеется, внешнего в отношении клеток, но не организма). Сигналы поступают к клеткам от гормонов или нейромедиаторов, заставляя их подчинять основные метаболические превращения интересам всего организма, например, запасать или сжигать топливо. Такая регуляция особенно необходима, если работа клетки важна для организма в целом. Клетки не могут сами принять решение о том, что нужно организму. Они должны получить сигнал извне, и лишь после этого внутриклеточная регуляция включится в поддержание необходимых процессов.
Основные моменты внутренней регуляции метаболизма углеводов и липидов
Внутриклеточная регуляция метаболизма гликогена
Метаболизм гликогена включает синтез этого полимера гликогенсинтазой и его расщепление гликогенфосфорилазой. Гликоген синтезируется в период хорошего питания, и этот синтез регулируется внешними сигналами (см. с. 169). Расщепление гликогена преследует две физиологические цели. Общей для всех тканей задачей является поставка гликолизу исходного материала - глюкозо-6-фосфата. Именно в него с помощью фосфоглюкомутазы превращается первичный продукт распада гликогена - глюкозо-1-фосфат, а гликогенфосфорилаза (фермент, расщепляющий гликоген) занимает ключевое место в метаболизме. Энергия, образующаяся в процессе гликолиза в виде АТР, необходима для всех тканей, но особое значение она имеет для мышц, сокращение которых сопровождается интенсивным потреблением АТР (см. главу 28). В печени распад гликогена происходит с целью поддержать на должном уровне концентрацию глюкозы в крови.
Механизмы регуляции гликогенфосфорилазы, которая является примером «классического» регуляторного фермента, подробно изучены (это особенно касается фермента из мышц). В покоящейся мышце она находится в виде неактивной фосфорилазы b, которая частично активируется АМР, действующим в качестве аллостерического эффектора (максимальную активацию вызывают внешние сигналы). Почему именно АМР выступает в данном случае в роли аллостерического сигнала? Гликогенфосфорилаза должна быть активирована, когда резерв энергии в клетке достаточно мал, т. е. в клетке мало АТР. Поскольку аденилаткиназа катализирует реакцию:
2ADP <-» АМР + АТР,
АМР служит индикатором накопления ADP, который образуется при гидролизе АТР и, следовательно, отражает уменьшение концентрации последнего. Расчеты показывают, что даже незначительный расход АТР приводит к относительно большому увеличению концентрации АМР, активирующего гликогенфосфорилазу, чтобы обеспечить производство дополнительной энергии. С другой стороны, АТР и глюкозо-6-фосфат являются аллостерическими ингибиторами гликогенфосфорилазы (рис. 12.9). Если их достаточно, зачем производить еще? Простая внутриклеточная регуляция контролируется извне и зависит от физиологического режима всего организма (см. с. 169).
В печени ситуация та же: АМР активирует фосфорилазу b до ~20% от максимального уровня, а внешние сигналы имеют приоритет над внутренними, хотя здесь они преследуют достижение иных физиологических целей (см. с. 169).
Итак, и в мышцах, и в печени в отсутствие внеклеточных регуляторов (о них мы поговорим чуть позже) фосфорилаза находится в неактивной форме b. АМР акивирует фермент, а АТР и глюкозо-6-фосфат ингибируют активность фосфорилазы.
Гликолиз и глюконеогенез
Из общей схемы регуляторных путей, изображенных на рис. 12.9, следует, что:
✵ рост концентрации АМР указывает на увеличение отношения ADP/ATP;
✵ АМР активирует гликогенфосфорилазу и фосфоф- руктокиназу;
✵ АМР ингибирует фруктозо-1,6-дифосфатазу;
✵ активация распада гликогена сопровождается увеличением уровня фруктозо-6-фосфата;
✵ фруктозо-6-фосфат активирует фосфофруктокиназу;
✵ активация фосфофруктокиназы приводит к увеличению концентрации фруктозо-1,6-дифосфата;
✵ фруктозо-1,6-дифосфат активирует пируваткиназу. Из перечисленного видно, что система аллостерической регуляции гликолиза включает как отрицательные и положительные обратные связи, так и положительные прямые связи. Эволюция редко ограничивается каким-то одним способом регуляции. Так, в данной системе фосфофруктокиназа активируется АМР, но ингибируется АТР. Это позволяет гликолизу точно реагировать на изменения соотношения ATP/ADP (через концентрацию АМР).
С ростом уровня АТР замедляется цикл лимонной кислоты и происходит накопление цитрата. Последний выходит из митохондрий в цитоплазму и аллостерически ингибирует фосфофруктокиназу. Таким способом процесс гликолиза приостанавливается. Та же цель достигается и другим путем: ацетил-СоА аллостерически ингибирует пируваткиназу.
Особо следует остановиться на активации пируват- карбоксилазы посредством ацетил-СоА, в результате чего образуется оксалоацетат (см. рис. 12.9). Накопление ацетил-СоА происходит при торможении цикла лимонной кислоты (вследствие дефицита оксалоацетата). Вполне естественно, что при этом автоматически запускается анаплеротическая реакция (см. с. 122). Эта регуляторная связь существенна также для глюконеогенеза.
Рис. 12.9. Главные пути аллостерической регуляции метаболизма гликогена, гликолиза и глюконеогенеза. Цветом выделены активирующие звенья регуляции, а пунктиром - ингибирующие. UDPРG - уридиндифосфатглюкоза
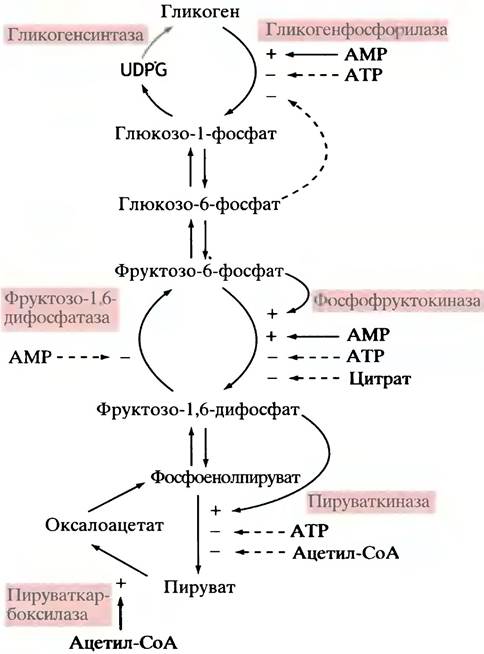
Внутриклеточная регуляция пируватдегидрогеназы, цикла лимонной кислоты и окислительного фосфорилирования
Пируватдегидрогеназа (см. с. 116) занимает стратегически важное положение в метаболизме, катализируя необратимую реакцию превращения пирувата в ацетил-СоА, который поступает в цикл лимонной кислоты, а также используется при синтезе жиров. Разные способы регуляции этого фермента показаны на рис. 12.10. Оба его продукта - ацетил-СоА и NADH, являются аллостерическими ингибиторами фермента, а субстраты - CoA-SH и NAD+ - активаторами. Таким образом, активность пируватдегидрогеназы определяется соотношениями ацетил-СоА/СоА и NADH/NAD+. Логика очевидна. Если существует значительный избыток ацетил-СоА и NADH, значит их образование с помощью пируватдегидрогеназы должно быть приостановлено. И наоборот, если высока концентрация CoA-SH и NAD+, то фермент должен активно работать.
Рис. 12.10. Аллостерическая регуляция и обратимое фосфорилирование как способы управления активностью пируват- дегидрогеназного ферментного комплекса млекопитающих (ПДГ). Множественность способов контроля обусловлена стратегическим положением этого комплекса в общем метаболизме, так как ацетил-СоА далее поступает в цикл лимонной кислоты и используется для синтеза жиров. Все способы регуляции фактически призваны обеспечить ингибирование ПДГ продуктами его активности и активацию субстратами (АТР можно рассматривать как отдаленный продукт превращения ацетил-СоА в цикле лимонной кислоты). Регуляция посредством обратимого фосфорилирования обычно сопряжена с гормональной регуляцией, а ионы кальция, стимулирующие активность фосфатазы, накапливаются под действием катехоламинов
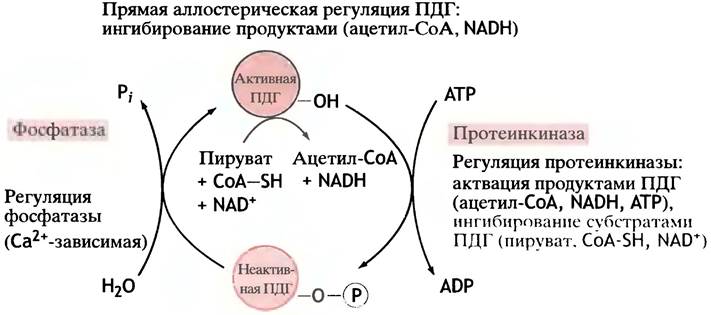
Особое значение имеет отрицательная регуляция фермента высокими концентрациями АТР. Накопление АТР свидетельствует о необходимости замедлить его производство. Регуляция активности фермента с помощью АТР - не прямой процесс. При увеличении молярного отношения ATP/ADP активируется протеинкиназа пируватдегидрогеназы, которая фосфорилирует фермент, тем самым ингибируя его (напомним, что фосфорилированию всегда противостоит дефосфорилирование, катализируемое фосфатазами) (см. рис. 12.10). Киназа входит в состав пируватдегидрогеназного комплекса. Помимо АТР она активируется также ацетил-СоА и NADH. Все эти регуляторные эффекты сводятся к одному: прикрыть «топливный кран», если вырабатывается избыток энергии.
Аллостерическая регуляция ферментов осуществляется также и в цикле лимонной кислоты, и в цепи переноса электронов. Однако в этих системах, расположенных в митохондриях, основные регуляторные механизмы связаны с изменениями концентрации таких ключевых субстратов, как NAD+ и ADP. Если большая часть NAD представлена восстановленной формой NADH, активность дегидрогеназ в цикле лимонной кислоты снижается. Поскольку NADH накапливается в том случае, когда не успевает окислиться в цепи переноса электронов (например, из-за недостатка кислорода), ингибирование некоторых реакций цикла лимонной кислоты можно рассматривать как регуляторный ответ. Точно так же при малом молярном соотношении ADP/ATP тормозится перенос электронов по митохондриальной цепи, поскольку процессы фосфорилирования и окисления в митохондриях тесно взаимосвязаны. Эта взаимосвязь носит специальное название - дыхательный контроль - и имеет огромное значение.
Наряду с NAD+ и ADP цикл лимонной кислоты регулируется на уровне цитратсинтазы (ингибируется АТР), изоцитратдегидрогеназы (ингибируется АТР, активируется ADP) и α-кетоглутаратдегидрогеназы (ингибируется NADH и сукцинил-СоА).
Все эти регуляторные звенья вполне логичны и помогают поддерживать баланс метаболитов в цикле лимонной кислоты, чтобы избежать их избытка или дефицита.
Внутриклеточная регуляция процессов окисления и синтеза жирных кислот
Схема регуляции этих процессов представлена на рис. 12.11. Смысл ее в том, чтобы избежать одновременного протекания в одной клетке окисления и синтеза жирных кислот.
Рис. 12.11. Основные места внутриклеточной регуляции при окислении и синтезе жиров. Поскольку при окислении жиров образуется ацетил-СоА, скорость его последующих превращений зависит от регуляции реакций цикла лимонной кислоты и т. д. Пунктиром показаны аллостерические воздействия. Цитрат активирует ацетил-СоА-карбоксилазу invitro, однако пока не ясно, имеет ли это какое-то физиологическое значение
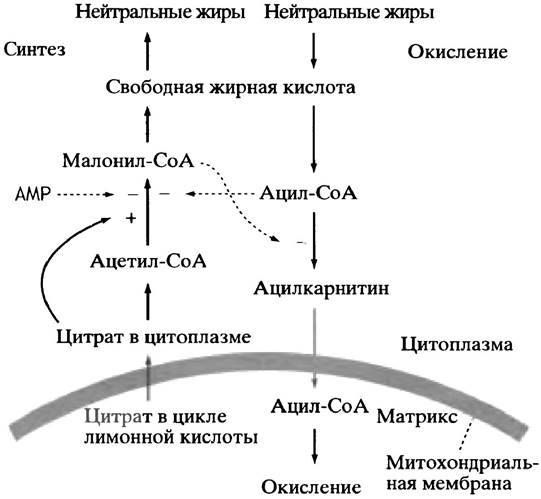
Эти два метаболических пути всячески подавляют друг друга. Исходные вещества окисления - СоА-производные жирных кислот (см. с. 132) - аллостерически ингибируют первый фермент синтеза жирных кислот - ацетил-СоА-карбоксилазу. Напротив, ключевой метаболит системы синтеза жиров - малонил-СоА (см. с. 138) — аллостерически ингибирует перенос ацильных остатков на карнитин (см. с. 133). Из-за этого жирнокислотные остатки не могут попасть внутрь митохондрий и подвергнуться там окислению: если вы синтезируете жиры, вряд ли стоит одновременно сжигать их в митохондриальной топке. Ацетил-СоА-карбоксилаза in vitro активируется цитратом, превращение которого приводит к образованию ацетил-СоА - субстрата этого же фермента (см. с. 141). Цитрат выходит из митохондрий лишь в том случае, если его там много, т. е. при изобилии пищи, когда самое время накапливать жиры. Нет сомнений, что в пробирке цитрат активирует ацетил-СоА-карбоксилазу, однако пока не установлено, имеет ли место такая активация в клетке. В то же время бесспорно, что ацетил-СоА-карбоксилаза ингибируется при фосфорилировании. Оно осуществляется протеинкиназой, активность которой зависит от присутствия АМР, тогда как обратная фосфатазная реакция контролируется на гормональном уровне (см. с. 176).
Все, что было сказано выше о внутриклеточной регуляции метаболизма углеводов и жиров, разумеется, не претендует на исчерпывающее изложение накопленных сведений. Но этих данных более чем достаточно для понимания того, что метаболизм не является суммой последовательно протекающих реакций. Это сложный, вполне упорядоченный процесс, в котором все метаболические пути тесно взаимосвязаны между собой.
Чтобы понять, как клеточный метаболизм согласуется с физиологическими потребностями организма в целом, необходимо уяснить внеклеточную регуляцию гормонами и другими соединениями. Они часто контролируют те же реакции, что и внутриклеточные соединения, поэтому некоторые реакции подвергаются как внутри-, так и внеклеточной регуляции.
Регуляция метаболизма углеводов и жиров внеклеточными агентами
Особую роль среди внеклеточных агентов, участвующих в регуляции углеводного и жирового обмена, играют гормоны глюкагон, инсулин, адреналин и норадреналин.Гормоны действуют мгновенно, вызывая подчас сильный эффект. Они помогают организму приспособиться к периодическим чередованиям состояний насыщения и голода (см. с. 84).
В целом гормональная регуляция чрезвычайно сложна. Гормоны гипофиза, надпочечников, щитовидной железы и др. (см. табл. 26.1) воздействуют на метаболизм далеко не всегда понятным образом. Обычно их действие опосредовано множеством событий и растянуто во времени. Например, при избытке тироксина люди постепенно худеют и становятся легко возбудимыми, а его недостаток вызывает обратные и тоже медленно развивающиеся эффекты. Однако есть гормоны, которые проявляют себя направленно и быстро.
Как вы помните, глюкагон - это «гормон голода», который вырабатывается поджелудочной железой в ответ на снижение уровня глюкозы в крови. И наоборот, при повышении содержания глюкозы выделяется инсулин (см. с. 84). Адреналин и норадреналин образуются в мозговом слое надпочечников и вызывают активацию процессов, связанных с превращением пищевых веществ. Норадреналин выделяется также симпатическими нервными окончаниями. Симпатическая нервная система управляет непроизвольными сокращениями гладких мышц внутренних органов, а также иннервирует жировую ткань. Ее можно рассматривать как способ быстрой доставки дозированного количества гормона непосредственно к регулируемым клеткам и органам.
Как регулируется содержание в крови инсулина, глюкагона и адреналина?
Инсулин - небольшой белок, синтезируемый и секретируемый в кровь β-клетками островков Лангерганса поджелудочной железы. Время жизни инсулина в крови невелико, поэтому его действие затухает, как только прекращается секреция. β-Клетки очень чувствительны к изменениям концентрации глюкозы и начинают секретировать инсулин не позже чем через минуту после увеличения содержания глюкозы в крови в результате приема пищи. Важно отметить, что сродство глюкозы к транспортному белку, обеспечивающему ее поступление в клетки, очень мало, поэтому белок начинает функционировать лишь после того, как содержание глюкозы в крови превысит нормальный уровень - 90 мг в 100 мл, или 5 мМ. Зависимость скорости секреции инсулина от концентрации глюкозы описывается сигмоидной кривой; отсюда высокая чувствительность ответа на изменения ее содержания.
Глюкагон, напротив, секретируется поджелудочной железой при снижении концентрации глюкозы в крови. Адреналин же выделяется надпочечниками в ответ на нервный сигнал.
Как работают гормоны глюкагон, адреналин и инсулин?
Гормоны представлены веществами различной химической природы, поступающими в кровь. Они передают химические сигналы и доступны всем тканям. Избирательность их действия достигается тем, что не все клетки, а лишь клетки-мишени воспринимают эти сигналы.
Жирорастворимые гормоны (стероиды, тироксин) беспрепятственно проникают через плазматическую мембрану, тогда как водорастворимые гормоны (глюкагон, адреналин, инсулин) через нее пройти не могут. Их молекулы связываются рецепторными белками, специфичными для каждого гормона и расположенными на поверхности клеток. Избирательность связывания гормона с рецепторным белком имеет ту же природу, что и специфичность взаимодействия фермента с субстратами. Только клетки, предназначенные быть мишенью для гормона, имеют «настроенные» на него рецепторы. Остальные клетки присутствия гормона не ощущают, они как бы слепы по отношению к нему.
Гормоны быстро выводятся из крови, поэтому, как только железа перестает выделять гормон, его концентрация падает, гормон-рецепторные комплексы диссоциируют и сигнал исчезает. Однако, пока гормон связан с рецептором, его присутствие вызывает определенные химические изменения внутри клетки, которые и составляют гормональный ответ (рис. 12.12).
Рис. 12.12. Гормон, инициирующий химические реакции в цитоплазме, связывается рецептором на поверхности клетки
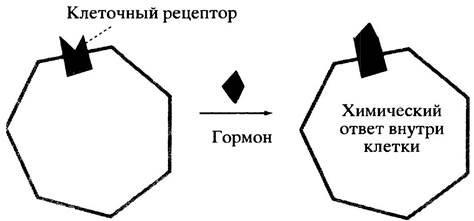
В основе современных представлений о природе гормонального ответа лежит концепция вторичного мессенджера (англ. messenger - гонец, посредник, посланец).
Что такое вторичный мессенджер?
Гормон можно рассматривать как первичный мессенджер: связываясь со своим клеточным рецептором, он передает гуморальный сигнал клетке. При этом изменяется уровень вторичного мессенджера - внутриклеточной молекулы, запускающей в клетке те или иные химические превращения в ответ на связывание гормона с рецептором.
Что служит вторичным мессенджером для глюкагона, адреналина и норадреналина?
В случае глюкагона и адреналина вторичным мессенджером служит циклический аденозин-3',5'-монофосфат, или циклический АМР (сАМР), который синтезируется из АТР ферментом аденилатциклазой (рис. 12.13).
Рис. 12.13. Синтез циклического АМР из АТР, катализируемый аденилатциклазой
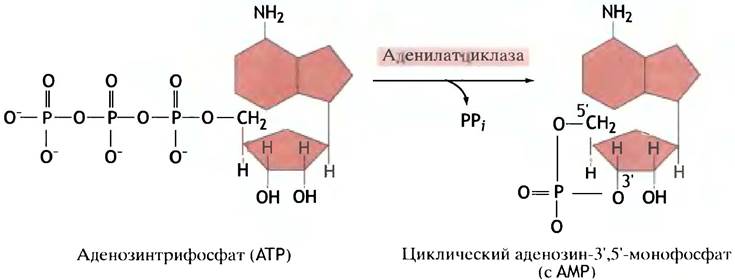
В свою очередь, сАМР аллостерически активирует сАМР-зависимую протеинкиназу, которая фосфорилирует гидроксильные группы серина или треонина белков-мишеней, изменяя активность последних. Каскад регуляторных реакций, передающих гормональный сигнал, представлен на рис. 12.14.
Рис. 12.14. Этапы гормональной регуляции метаболизма. Здесь не показано, что сАМР постоянно разрушается и дефосфорилирование белков осуществляется фосфатазами. Метаболический ответ поддерживается до тех пор, пока гормон связан с рецептором
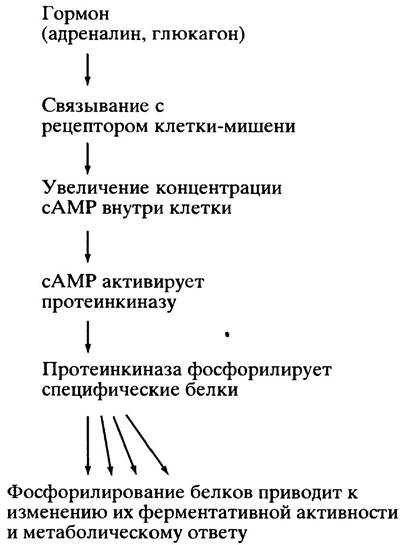
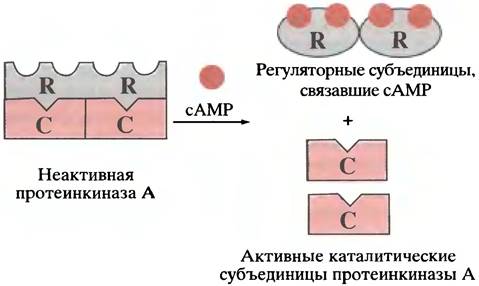
Механизм, посредством которого сАМР активирует протеинкиназу, показан на рис. 12.15. В отсутствие сАМР киназа представляет собой тетрамер, образованный двумя каталитическими и двумя регуляторными субъединицами. В составе тетрамера каталитические субъединицы неактивны. Когда сАМР связывается с регуляторными субъединицами, тетрамер распадается на мономеры с высвобождением каталитически активных субъединиц.
Рис. 12.15. Активация сАМР-зависимой протеинкиназы под действием сАМР. R и С — соответственно регуляторные и каталитические субъединицы протеинкиназы
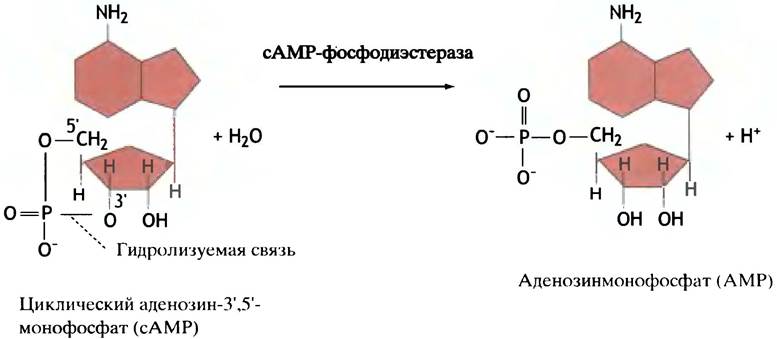
Фермент сАМР-фосфодиэстераза гидролизует сАМР до АМР (рис. 12.16). Поэтому активация протеинкиназы зависит от постоянного образования сАМР, которое прекращается, как только гормон покидает рецептор. Как уже упоминалось, гормоны в крови тоже постоянно разрушаются или удаляются, так что их присутствие в ней зависит от секреции. Таким образом, каждый этап передачи гормонального сигнала включает механизм его торможения. Когда уровень гормона падает, образование сАМР прекращается, фосфорилированные белки дефосфорилируются протеинфосфатазами и все возвращается в исходное состояние.
Рис. 12.16. Реакция, катализируемая сАМР-фосфодиэстеразой. Это название фермент получил за то, что он гидролизует фосфодиэфирную связь в молекуле сАМР
В этой главе мы не обсуждаем, как гормон запускает синтез сАМР и как этот синтез прекращается, когда гормон покидает рецептор. Вопросы передачи сигналов
через клеточные мембраны детально рассматриваются в главе 26. Пока достаточно понять, что связывание глюкагона и адреналина клеточными рецепторами приводит к увеличению внутриклеточной концентрации сАМР.
Управление числом рецепторов
Число специфических рецепторов на поверхности клетки может регулироваться. Продолжительный контакт клетки с агонистом (так называют любое соединение, которое связывается с рецептором и активизирует его) может привести к обратимому уменьшению числа рецепторов и к снижению чувствительности клетки к данному агонисту, а, следовательно, к более слабому ответу. Это явление называют даунрегуляцией (англ. downregulation). Кроме того, рецептор может быть инактивирован в результате его фосфорилирования цитоплазматической киназой, после чего связывание его с гормоном не будет приводить к синтезу сАМР. Поскольку такого рода фосфорилирование стимулируется сАМР, интенсивность клеточного ответа регулируется им по принципу отрицательной обратной связи.
Все эти виды регуляции имеют место в случае рецепторов адреналина, инсулина и глюкагона.
Как инсулин управляет метаболизмом?
Инсулин влияет на энергетический метаболизм диаметрально противоположно глюкагону (см. главу 5). Инсулин - белковый гормон, который известен довольно давно и изучен, пожалуй, тщательнее, чем какой-либо другой белок или гормон. Причиной тому является не только его ключевая роль в углеводном и жировом обмене, но и терапевтическое применение при лечении диабета. К сожалению, несмотря на все усилия, механизм действия инсулина еще во многом неясен. Установлено присутствие инсулиновых рецепторов на внешней поверхности клеток. Совсем недавно стало известно, что его рецепторы пронизывают плазматическую мембрану, а цитоплазматический домен является тирозиновой протеинкиназой. Она отличается от ранее описанных протеинкиназ и стимулируется при связывании с инсулином (см. главу 26). Эту киназу характеризует то, что она фосфорилирует тирозиновые остатки. Более подробно механизм действия инсулина обсуждается в главе 26.
Регуляция поглощения клетками глюкозы и жиров
Глюкоза не может пройти через липидный бислой, поэтому в клеточных мембранах присутствует специальный мембранный транспортный белок, ответственный за ее перенос. В пищеварительном тракте глюкоза всасывается за счет активного транспорта, во всех других тканях она поступает в клетки путем пассивного переноса. Такой тип трансмембранного переноса сводится к тому, что молекулы преодолевают мембранный барьер благодаря наличию градиента концентраций, и называется облегченной диффузией (см. с. 63).
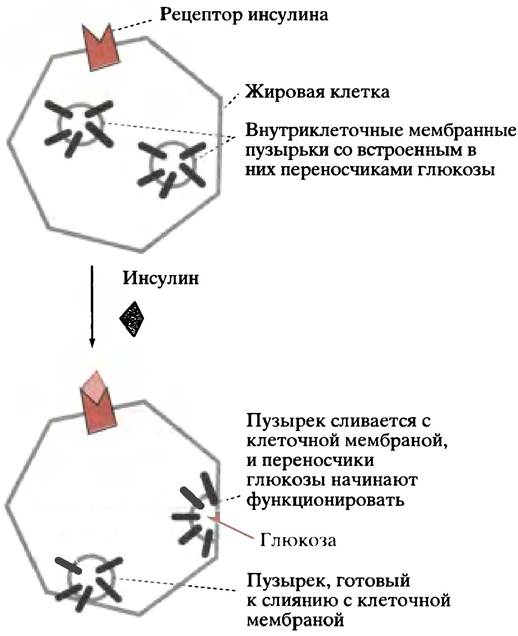
В мозге и в печени поглощение глюкозы клетками не зависит от инсулина, но в мышечных и жировых клетках оно ускоряется этим гормоном. Судя по всему, в цитоплазме таких клеток имеются неактивные транспортные белки. Инсулин стимулирует их переход в активную форму и встраивание в мембрану, что увеличивает пропускную способность мембраны для глюкозы (рис. 12.17). На жировых клетках было показано, что встраивание транспортного белка завершается уже через 7 минут после связывания инсулина с рецептором. После удаления инсулина процесс обращается, и через 20-30 минут транспортные белки выходят из мембраны в цитоплазму.
Рис. 12.17. Мобилизация переносчиков глюкозы под действием инсулина в жировых и некоторых других клетках. В клетках печени и мозга этого не происходит. Транспорт глюкозы через плазматическую мембрану осуществляется по типу облегченной диффузии
Механизм этого удивительного явления пока неизвестен. Возможно, инсулин стимулирует движение транспортного белка и встраивание его в мембрану или вызывает смещение динамического равновесия между мембранным и цитоплазматическим фондами этого белка.
Облегченная диффузия может лишь выровнять концентрации глюкозы в крови и клетках. Однако внутри клеток глюкоза быстро исчезает, либо превращаясь в гликоген, либо расходуясь на метаболические нужды. Это препятствует выравниванию концентрационного градиента глюкозы и служит движущей силой ее транспорта внутрь клетки.
Первый этап внутриклеточных превращений глюкозы - ее фосфорилирование. Он осуществляется в печени глюкокиназой, а в других тканях - гексокиназой:
Глюкоза + АТР —> глюкозо-6-фосфат + ADP.
Величина Км (для глюкозы) глюкокиназы по сравнению с гексокиназой гораздо выше, т. е. сродство первого фермента к субстрату меньше (см. с. 91). Глубокий смысл этого различия становится понятным, если вспомнить о глюкостатической функции печени. Ей не нужно поглощать глюкозу, если последняя в крови не присутствует в избытке. Если глюкозы в крови мало, печень ее производит и направляет в кровоток. Было бы нелогично одновременно выводить глюкозу в кровоток и поглощать ее оттуда. Этого и не происходит, поскольку глюкокиназа не фосфорилирует глюкозу, если концентрация последней мала по сравнению с Км.
Для глюкокиназы предусмотрен еще один регуляторный механизм. Этот фермент индуцируется инсулином. Под термином индукция понимают ускорение биосинтеза под влиянием индуктора, в данном случае инсулина. Механизм, посредством которого инсулин это делает, пока неизвестен.
Метаболизм жиров начинается с поступления в клетки не самих триглицеридов, а жирных кислот. Последние легко проходят через мембраны без участия каких бы то ни было транспортных систем, поскольку липидный бислой не служит для них барьером. Поэтому необходимо контролировать поступление жирных кислот в клетку. При этом следует регулировать их содержание в крови. Такая регуляция осуществляется глюкагоном, адреналином, норадреналином и инсулином, действующими на жировые клетки.
Получив общие представления о внеклеточной регуляции, мы можем перейти к рассмотрению действия гормонов на отдельные метаболические пути.
Регуляция синтеза и расщепления гликогена внеклеточными агентами
Регуляция расщепления гликогена
Мы уже познакомились с регуляцией гликогенфосфорилазы b в покоящихся мышцах и в печени, в основе которой лежит активация фермента под действием АМР. Эта регуляция обеспечивает постоянный контроль уровня глюкозы на фоне стабильного режима ее расходования. Существует, однако, совершенно иная регуляторная система, основанная на превращении фосфорилазы b в фосфорилазу а, чья активность не зависит от АМР. Такое превращение происходит в результате фосфорилирования фермента протеинкиназой, которая переносит фосфатный остаток АТР на гидроксильную группу одного из сериновых остатков, вызывая тем самым конформационные изменения молекулы фермента и его активацию. Важно помнить о разнице между фосфорилированием, когда на гидроксильную группу серина протеинкиназой переносится фосфатный остаток АТР, и фосфоролизом - катализируемым фосфорилазой процессом расщепления гликогена с участием неорганического фосфата. В мышечных клетках протеинкиназа активируется адреналином. Этот гормон, циркулирующий в крови, распознается и связывается рецепторами на поверхности мышечной клетки, запуская при этом внутриклеточный синтез сАМР. Мы еще вернемся к рассмотрению механизма, посредством которого сАМР стимулирует фосфорилирование фосфорилазы b, а пока обсудим физиологические аспекты всего процесса.
Адреналин образуется в надпочечниках в ответ на нервный сигнал, идущий из мозга при возникновении экстремальной ситуации, требующей мгновенной и активной мышечной деятельности (в англоязычной литературе такую ситуацию называют fight or flight - бегство или борьба). Адреналин как бы нажимает кнопку «тревога». Мышечной клетке некогда дожидаться, когда в ней накопится индикатор сниженной концентрации АТР-АМР - и сработает внутриклеточная положительная обратная связь. Клетка должна мгновенно обеспечить неограниченный поток топлива для генерации АТР, чтобы организм успел справиться с грозящей опасностью. Далее мы поясним, почему в такой ситуации оптимальным топливом является глюкозо-6-фосфат, образующийся из продукта фосфоролиза гликогена- глюкозо-1-фосфата. Здесь отметим только, что из-за низкого выхода АТР для продолжения гликолиза нужно иметь про запас большое количество топлива. Эту задачу решает мгновенная активация гликогенфосфорилазы.
Адреналин также стимулирует высвобождение глюкозы из печени в кровь. Его цель - быстро снабдить мышцы топливом в экстремальной ситуации. И здесь эффект адреналина обусловлен быстрым фосфорилированием гликогенфосфорилазы.
Любопытно, что в картофельных клубнях тоже есть фосфорилаза, расщепляющая крахмал. Степень гомологии растительной и мышечной фосфорилазы очень высока: их аминокислотные последовательности наполовину идентичны. Тем не менее картофельная фосфорилаза не активируется фосфорилированием, возможно потому, что картофелю не нужен ответ типа «бегство или борьба» и не нужно контролировать уровень глюкозы в крови.
Добавим, что печень выбрасывает в кровь глюкозу также в ответ на связывание глюкагона рецепторами. Этот гормон выделяется поджелудочной железой при снижении уровня глюкозы в крови и, подобно адреналину, вызывает увеличение содержания внутриклеточного сАМР и активацию гликогенфосфорилазы. Мышечные клетки не реагируют на присутствие глюкагона, поскольку на их поверхности нет специфичных к нему рецепторов.
Механизм регуляции синтеза и расщепления гликогена с помощью сАМР
Гликогенфосфорилаза существует в двух формах: в форме а сериновый гидроксил фосфорилирован, а в форме b нет. Схема взаимопревращений обеих форм представлена на рис. 12.18.
Рис. 12.18. Взаимопревращения гликогенфосфорилаз а и b под действием киназы и фосфатазы. сАМР влияет на эти превращения лишь опосредованно. Гидроксильная группа принадлежит сериновому остатку белка
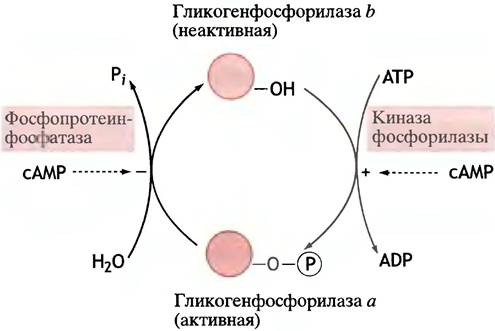
Активация под действием сАМР киназы фосфорила- зы, осуществляющей фосфорилирование гликогенфосфорилазы, не является прямой. сАМР сначала активирует протеинкиназу А (ПКА; А - от сАМР), которая, в свою очередь, фосфорилирует киназу фосфорилазы, переводя ее в активное состояние. А та уже фосфорилирует гликогенфосфорилазу b. Полная последовательность событий, разворачивающихся после контакта клетки с гормоном, представлена на схеме:
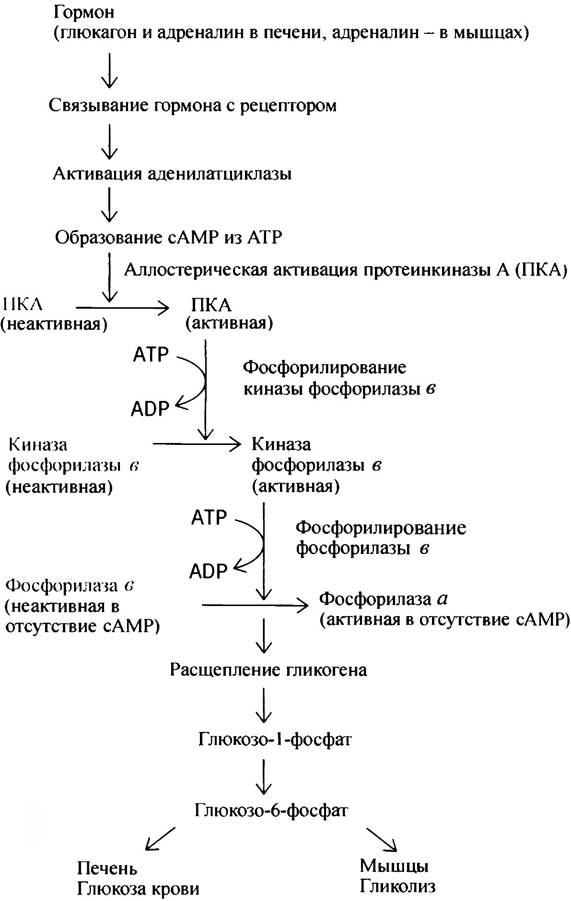
К чему такой сложный механизм регуляции? Каждая клетка связывает небольшое число молекул гормона. Между тем ее ответ, особенно в экстремальной ситуации, должен быть быстрым и мощным. Напомним, что клетка печени содержит примерно 1 мкмоль остатков глюкозы (180 мкг), т. е. ~ 6,02 • 1017 молекул. Связывание нескольких молекул гормона с рецепторами должно заставить клетку переработать астрономическое число молекул глюкозы, при этом очень быстро. Так же
обстоит дело и с образованием глюкозо-6-фосфата в ходе генерации энергии в мышцах.
Следовательно, слабый сигнал - связывание гормона с рецептором - должен быть усилен до такой степени, чтобы вовлечь в ответ максимально возможное число исполнителей команды - молекул фермента. Таким образом, рассмотренная выше схема есть не что иное, как мощный регуляторный каскад. Предположим, 1 молекула гормона активирует 1 молекулу аденилат- циклазы, которая образует 100 молекул сАМР в минуту. Это уже стократное усиление. Если каждая молекула сАМР активирует 1 молекулу протеинкиназы А, которая с такой же производительностью фосфорилирует киназу фосфорилазы b, то усиление составит 100 • 100 и т. д. В действительности гормональная активация гликоген- фосфорилазы включает четыре ступеньки усиления. Каскадное усиление сигнала - общий принцип действия гормонов.
Каждая молекула гликогенфосфорилазы атакует конец одной из олигосахаридных цепей гликогена. Если бы гликоген, подобно амилозе, представлял собой длинные линейные цепи, гормональная стимуляция стала бы бессмысленной, поскольку множеству молекул активированной гликогенфосфорилазы не хватило бы мишеней. Видимо, именно в этом причина крайней разветвленности гликогена (по сравнению с крахмалом), позволяющей в критической ситуации подвергнуться быстрому расщеплению. Неторопливые растения в этом не нуждаются и могут позволить себе хранить глюкозу в виде амилозы.
Обращение активации фосфорилазы
Все регуляторные метаболические процессы должны быть обратимыми. «Включение» и «выключение» открывает дополнительную возможность управления регулируемым процессом. В случае фосфорилазы форма а превращается обратно в форму b с помощью особой фосфатазы (так называемой протеинфосфатазы I), которая отщепляет фосфат от фосфорилированного остатка серина:
![]()
В печени эта реакция стимулируется свободной глюкозой благодаря ее аллостерическому действию, оказываемому на форму а.
На время развития гормонального ответа - превращения фосфорилазы b в фосфорилазу а - целесообразно подавить деятельность фосфатазы, чтобы она не препятствовала быстрому нарастанию числа активных молекул гликогенфосфорилазы. Оказывается, во многих клетках присутствует белок, который называют ингибитором фосфатазы I. Он фосфорилируется той же самой протеинкиназой А, что и киназа фосфорилазы, и ингибирует фосфатазу. Таким образом, в конечном итоге сАМР не только «включает рубильник», но и не дает его сразу «выключить».
При нормальном мышечном сокращении (т. е. в ситуации, не требующей участия сАМР в регуляции) киназа фосфорилазы аллостерически активируется ионами Са2+, концентрация которых при сокращении мышц в ответ на сигнал от двигательного нерва резко возрастает (см. главу 28). Поскольку такая активация киназы фосфорилазы никак не связана с фосфорилированием, она исчезает, как только поступает первый сигнал к расслаблению. Активация фермента с помощью ионов Са2+ опосредована регуляторным белком кальмодулином, который присутствует почти во всех эукариотических клетках. Этот небольшой растворимый белок в случае киназы фосфорилазы является прочносвязанной субъединицей фермента. Кальмодулин действует как детектор концентрации Са2+: связывание кальмодулином этих ионов вызывает в нем конформационные изменения, благодаря которым он взаимодействует с большим числом белков-мишеней, в том числе и с ферментами, активируя их.
Подведем итог основным фактам, изложенным выше, чтобы закрепить в памяти главные элементы этой сложной регуляторной системы (рис. 12.19).
Рис. 12.19. Регуляция киназы фосфорилазы мышц. Представлен также механизм активации киназы ионами кальция, который не зависит от сАМР. Ионы кальция не только инициируют мышечное сокращение, но также обеспечивают его энергией. Для каталитической активности фосфорилированной (активной) киназы необходимы ионы Са2+. Они связываются с кальмодулином, который является субъединицей этого фермента, вызывая активацию последнего
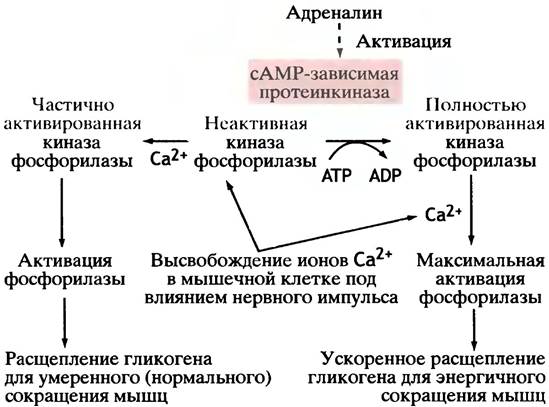
1. Фосфорилаза - фермент, катализирующий расщепление гликогена посредством фосфоролиза. Эта реакция не имеет ничего общего с фосфорилированием - переносом фосфата с АТР на гидроксильную группу серина или треонина, которое катализирует фермент протеинкиназа. Фосфатаза осуществляет гидролитическое отщепление фосфата от фосфорилированных белков.
2. В печени и в покоящихся мышцах фосфорилаза находится в виде неактивной и нефосфорилированной формы b, которую частично активирует сАМР. Эта активация не сопровождается фосфорилированием фермента.
3. Адреналин, воздействуя на клетки мышц и печени, а также глюкагон, воздействуя на клетки печени (но не мышц), вызывают увеличение внутриклеточной концентрации сАМР.
4. сАМР аллостерически активирует протеинкиназу, которая в свою очередь активирует киназу фосфорилазы, специфически активирующую фосфорилазу b. Последняя при этом превращается в активную форму а. Процесс в целом можно рассматривать как усилительный каскад.
5. При нормальном мышечном сокращении под влиянием нервного импульса в мышечных клетках увеличивается концентрация Са2+. Эти ионы аллостерически
активируют (частично) киназу фосфорилазы b. В результате происходит частичная активация фосфорилазы. В отличие от сАМР-индуцированной активации киназы фосфорилазы, активация Са2+ не сопряжена с ее фосфорилированием.
6. Превращение активной фосфорилазы а обратно в неактивную форму b катализирует фермент протеин- фосфатаза I. Его активность регулирует ингибитор про- теинфосфатазы I - белок, который проявляет свои ингибирующие свойства только после того, как будет фосфорилирован. Это фосфорилирование осуществляется той же самой сАМР-стимулируемой протеинкиназой, которая фосфорилирует киназу фосфорилазы b. Таким образом, активация фосфорилазы сопровождается ингибированием фосфатазы. В печени превращение формы а фосфорилазы в форму b активируется глюкозой.
Как регулируется гликогенсинтаза?
Синтез и распад гликогена должны управляться таким образом, чтобы эти два процесса не могли протекать одновременно, ибо в противном случае возникает холостой цикл. В предыдущем разделе говорилось о том, что активация гликогенфосфорилазы является следствием активации протеинкиназы А под влиянием сАМР. Гликогенсинтаза непосредственно фосфорилируется протеинкиназой А, но в этом случае фосфорилирование инактивирует фермент. Регуляторный каскад активации гликогенсинтазы короче, что вполне понятно, поскольку синтез гликогена проходит в более спокойных для организма условиях, чем его расщепление в экстремальных ситуациях.
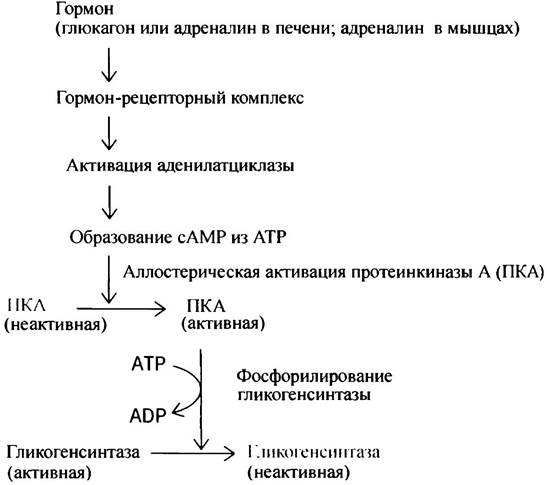
Мы уже видели, как происходит инактивация фосфорилазы а. Ее осуществляет фосфатаза, которую в свою очередь ингибирует белок (ингибитор протеинфосфатазы), фосфорилируемый протеинкиназой А. Нечто похожее происходит при регуляции гликогенсинтазы. Однако есть существенные отличия двух регуляторных путей: 1) дефосфорилирование синтазы приводит к ее активации; 2) протеинкиназа не активирует, а напротив, инактивирует белковый ингибитор фосфатазы. Эта протеинкиназа не идентична протеинкиназе А и, в отличие от последней, активируется не сАМР, а инсулином. Таким образом, инсулин активирует фосфатазу I, которая в свою очередь активирует гликогенсинтазу.
Удивительно, что один и тот же белковый ингибитор участвует в регуляции и синтеза, и расщепления гликогена; однако протеинкиназа А его активирует, а инсулинзависимая киназа - инактивирует.
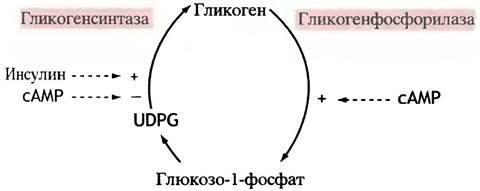
Механизмы регуляции гликогенсинтазы представлены на рис. 12.20, а общая схема регуляции метаболизма гликогена - на рис. 12.21.
Рис. 12.20. Схема взаимной регуляции гликогенфосфорилазы и гликогенсинтазы. Цветными кружками обозначены молекулы ферментов: активные - темнее, неактивные - светлее
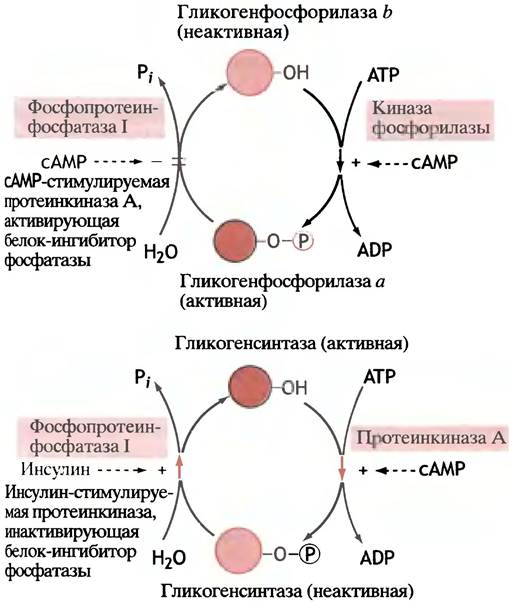
Рис. 12.21. Регуляция метаболизма гликогена. Действие инсулина и сАМР на активность ферментов является опосредованным. UDРG - UDР-глюкоза
Регуляция гликолиза и глюконеогенеза внеклеточными агентами
Эти два метаболических пути логично рассматривать вместе, так как в них вовлечены, по большей части, одни и те же ферменты. Глюкагон сигнализирует печени
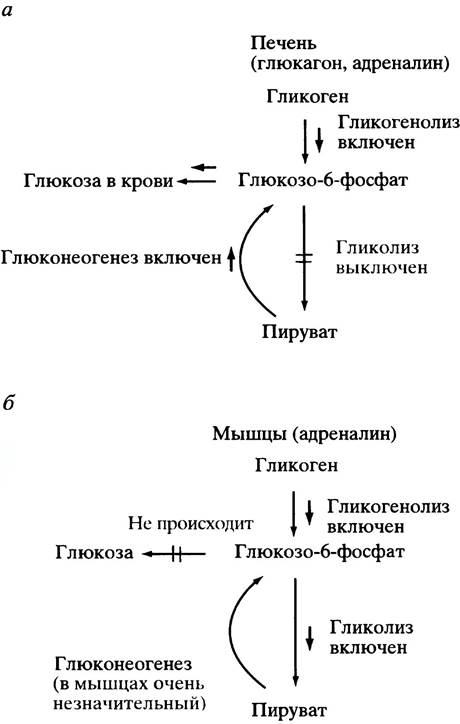
о необходимости выделения в кровь глюкозы либо за счет гликогенолиза (расщепления гликогена), либо - глюконеогенеза. Поэтому логично, что в печени сАМР включает расщепление гликогена и глюконеогенез (рис. 12.22, а). Было бы странно, если сАМР включал бы при этом в печени гликолиз - процесс, обратный глюконеогенезу.
В мышцах ситуация совершенно иная. Там стимуляция синтеза сАМР адреналином является командой к увеличению генерации энергии. Поэтому логично, что сАМР в мышцах включает расщепление гликогена и активирует гликолиз (в отличие от печени), поскольку именно в ходе этого процесса образуется глюкозо-6-фосфат (рис. 12.22, б), дальнейшее превращение которого приводит к синтезу АТР.
Рис. 12.22. Различия в регуляции ответа на сигнал глюкагон и /или адреналин в печени (а) и мышце (б). Оба гормона используют сАМР в качестве вторичного мессенджера. Термин гликогенолиз здесь означает расщепление гликогена
Таким образом, в печени сАМР должен ингибировать, а в мышцах активировать гликолиз. Наиболее важной регуляторной стадией является реакция, катализируемая фосфофруктокиназой (см. рис. 8.7). В печени сАМР (в ответ на действие глюкагона) вызывает ингибирование фосфофруктокиназы, подавляя тем самым гликолиз, тогда как в мышцах сАМР (в ответ на действие адреналина) ускоряет гликолиз.
Влияние сАМР на фосфофруктокиназу в печени заслуживает отдельного обсуждения.
Как сАМР регулирует активность фосфофруктокиназы?
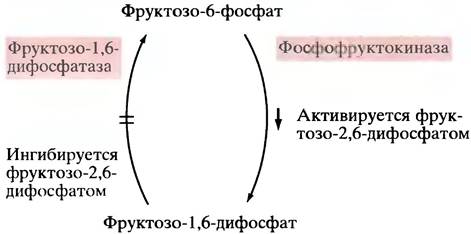
Этот регуляторный механизм хорошо известен для печени, и в нем не так уж трудно разобраться. Если уровень глюкозы в крови низок, то высоко содержание глюкагона, в результате в печени увеличивается внутриклеточная концентрация сАМР. Благодаря этому в клетке уменьшается содержание фруктозо-2,6-дифосфата. (Нет, здесь не опечатка!) Речь идет именно об этом, ранее не встречавшемся нам соединении, а не о хорошо знакомом фруктозо-1,6-дифосфате, который образуется в процессе гликолиза при участии фосфофруктокиназы. Фруктозо-2,6-дифосфат - чрезвычайно мощный аллостерический активатор фосфофруктокиназы, а вместе с ней и всего гликолиза. Это настоящая регуляторная молекула. Стоит увеличить его концентрацию - гликолиз ускоряется, если ее уменьшить - замедляется. Существенно, что фруктозо-2,6-дифосфат не только активирует фосфофруктокиназу, но также ингибирует фруктозо-1,6-дифосфатазу (рис. 12.23)-один из ключевых ферментов глюконеогенеза.
Рис. 12.23. Регуляция гликолиза фруктозо-2,6-дифосфатом
Нетрудно догадаться, что в печени сАМР должен снижать уровень 2,6-дифосфата: при этом блокируется гликолиз и активируется глюконеогенез. Как это достигается?
Образование фруктозо-2,6-дифосфата катализируется особой фосфофруктокиназой - ФФК2. После ее открытия ранее описанную фосфофруктокиназу стали сокращенно называть ФФК1.
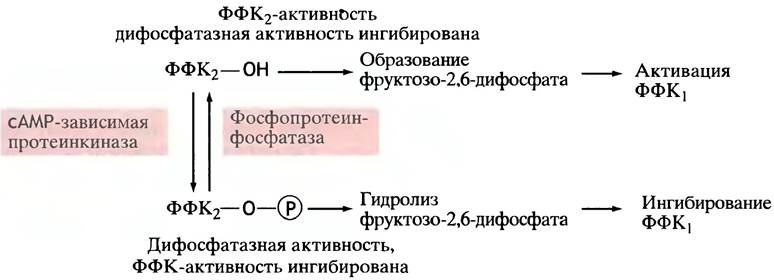
сАМР вызывает ингибирование ФФК2 (рис. 12.24). Происходит это так: сАМР активирует протеинкиназу, которая фосфорилирует ФФК2 (рис. 12.25). Фосфорилированная ФФК2не только перестает синтезировать фруктозо-2,6-дифосфат, но напротив, активно его гидролизует (нефосфорилированная ФФК2 не гидролизует фруктозо-2,6-дифосфат). Таким образом, фосфорилирование меняет не просто скорость, а направление катализируемой реакции.
Рис. 12.24. Синтез фруктозо-2,6-дифосфата второй формой фосфофруктокиназы (ФФК2) и ингибирование фермента в печени при участии сАМР. Это ингибирование опосредованное: сАМР активирует протеинкиназу, которая фосфорилирует ФФК1, подавляя тем самым синтез фруктозо-2,6-дифосфата. Фосфорилированная ФФК, гидролизует фруктозо-2,6-дифосфат. Таким образом сАМР снижает уровень фруктозо-2,6-дифосфата в печени
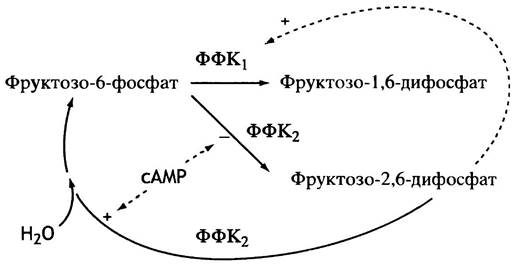
Рис. 12.25. Регуляция активности ФФК2 в печени посредством фосфорилирования сАМР-зависимой протеинкиназой. ФФК2 - бифункциональный фермент: в нефосфорилированной форме он синтезирует фруктозо-2,6-дифосфат, а после фосфорилирования гидролизует его
Что хорошо для печени, то плохо для мышц, поскольку там нельзя подавлять гликолиз, поставляющий топливо при экстренных нагрузках; и, следовательно, фосфофруктокиназа не может быть ингибирована. Известно, что под влиянием адреналина в мышцах возрастает уровень фруктозо-2,6-дифосфата. Возможно, это объясняется тем, что сАМР ускоряет расщепление гликогена, благодаря чему увеличивается содержание фруктозо-6-фосфата - субстрата и активатора ФФК2. Однако этот механизм регуляции требует дальнейшего изучения.
Глюкагон регулирует активность не только фосфофруктокиназы, но также и пируваткиназы, катализирующей заключительную стадию гликолиза. Индуцированный глюкагоном рост внутриклеточной концентрации сАМР приводит в клетках печени (но не мышц) к фосфорилированию пируваткиназы, которое сопровождается ее инактивацией.
Смысл этого совершенно ясен. Если требуется насытить кровь глюкозой, в печени нужно стимулировать глюконеогенез и блокировать гликолиз. Ингибирование пируваткиназы, так же, как и фосфофруктокиназы, решает вторую из этих задач.
Мышцы, как уже не раз отмечалось, заняты не синтезом, а исключительно расщеплением глюкозы, поэтому сАМР здесь не должен подавлять гликолиз. Действительно, увеличение уровня сАМР не приводит к фосфорилированию пируваткиназы.
Стимулируемое глюкагоном ингибирование пируваткиназы печени важно также и с точки зрения регуляции глюконеогенеза. Синтез глюкозы из пирувата включает две промежуточные реакции:
Пируват + ATP + НСО3- —> Оксалоацетат + ADP + Pi + H-, (1)
Оксалоцетат + GTP <-> Фосфоенолпируват + GDP + СO2 (2)
Нетрудно понять, что существует потенциальная опасность возникновения холостого цикла, поскольку пируваткиназа катализирует реакцию:
Фосфоенолпируват + ADP —> Пируват + АТР.
Такой потенциальный холостой цикл можно было бы описать следующей схемой:
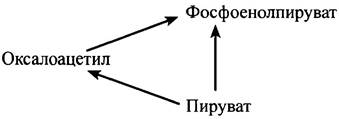
Во избежание холостого цикла необходимо, чтобы в процессе глюконеогенеза пируваткиназа была инактивирована. Только тогда весь фосфоенолпируват будет
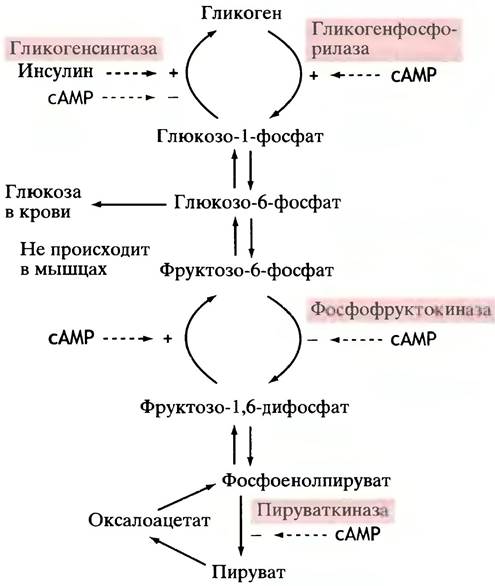
участвовать в реакциях глюконеогенеза. В печени инактивация фермента происходит при участии сАМР (рис. 12.26). Таким образом, глюкагон вызывает ингибирование фосфофруктокиназы и активацию фруктозо-1,6-дифосфатазы, тем самым стимулируя процесс глюконеогенеза, что приводит к увеличению уровня глюкозы в крови.
Рис. 12.26. Внешняя регуляция участка метаболизма углеводов в печени. Здесь под сАМР подразумевается воздействие гормонов: глюкагона и адреналина. Влияние сАМР на активность ферментов везде опосредовано
Регуляция метаболизма жиров внеклеточными агентами
У жировых клеток есть выбор: запасать триглицериды или расщеплять их запас до жирных кислот и выбрасывать последние в кровь. Инсулин служит сигналом для реализации первого варианта, а глюкагон - второго. Но у некоторых животных, в том числе и у человека, подобно глюкагону действуют адреналин и норадреналин. Жировые ткани иннервированы симпатическими нервами, окончания которых выделяют норадреналин; адреналин же секретируется надпочечниками.
Действие на метаболизм жировых клеток всех трех гормонов - глюкагона, адреналина и норадреналина - опосредовано участием общего для них вторичного
мессенджера - сАМР. Главной мишенью реакции служит чувствительная к гормонам липаза, которая катализирует реакцию:
триглицерид + Н2O —> диглицерид + свободная жирная кислота.
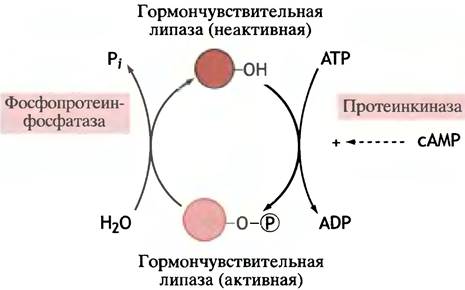
Диглицериды далее расщепляются до глицерина и жирных кислот. Эта гормончувствительная липаза активируется в результате фосфорилирования про- теинкиназой и инактивируется протеинфосфатазой (рис. 12.27). Связывание инсулина клеточными рецепторами блокирует эти эффекты.
Рис. 12.27. Активация гормоночувствительной липазы в жировых клетках путем ее сАМР-зависимого фосфорилирования. Инсулин служит антагонистом катехоламинам и глюкагону, которые способствуют росту концентрации сАМР. Глюкагон и адреналин ингибируют синтез жира соответственно в печени и в жировых клетках, предотвращая дефосфорилирование ацетил-СоА-карбоксилазы. Инсулин активирует карбоксилазу
Стимулируемое инсулином поглощение глюкозы способствует превращению ее избытка жировыми клетками в жиры. Ключевым ферментом синтеза жиров служит ацетил-СоА-карбоксилаза, катализирующая необратимую реакцию. Она инактивируется при фосфорилировании протеинкиназой, аллостерическим активатором которой служит АМР (не сАМР), и реактивируется фосфатазой, которая отщепляет фосфатную группу. В свою очередь, эта фосфатаза ингибируется сАМР - вторичным мессенджером глюкагона и адреналина.
Таким образом, если уровень АТР в клетке низок, АМР вызывает инактивацию карбоксилазы. При низком уровне глюкозы в крови карбоксилазу в неактивном состоянии поддерживает глюкагон. Инсулин вызывает обратный эффект: он несколько стимулирует активность карбоксилазы, тем самым способствуя синтезу жиров.
Вопросы к главе 12
1. Каковы два главных способа обратимого изменения активности ферментов?
2. Как сказываются изменения концентрации субстрата на скорости реакций, катализируемых неаллостерическими и аллостерическими ферментами?
3. Почему зависимость скорости реакции от концентрации субстрата у аллостерических ферментов в области Vmах/2 круче, чем у обычных?
4. Как влияют аллостерические эффекторы на скорость ферментативной реакции при насыщающих концентрациях субстрата?
5. Опишите две модели, объясняющие гомотропное кооперативное связывание субстрата ферментом.
6. Почему в клетках так широко используется аллостерическая регуляция?
7. Каковы основные принципы внутриклеточной и внеклеточной регуляции?
8. Пользуясь схемой, разъясните смысл аллостерической регуляции метаболизма гликогена, гликолиза и глюконеогенеза.
9. Пируватдегидрогеназа - ключевой регулируемый фермент. Как правило, продукты реакции ингибируют ее. Какие три механизма используются для регуляции активности пируватдегидрогеназы?
10. Как происходит внутриклеточная регуляция синтеза и окисления жиров?
11. Чем определяется секреция инсулина и глюкагона поджелудочной железой?
12. Что такое вторичный мессенджер? Назовите вторичный мессенджер для адреналина и глюкагона. Как вторичному мессенджеру удается влиять на клеточный метаболизм?
13. Как инсулин регулирует скорость поступления глюкозы в жировые клетки?
14. Как сАМР активирует процесс расщепления гликогена?
15. Глюкагон посредством с АМР активирует фосфорилазу печени. Адреналин точно так же активирует фосфорилазу в мышцах. Объясните, почему сАМР по-разному влияет на процесс гликолиза в печени и мышцах.
16. Некоторые гормоны, вызывающие в клетках разные эффекты, используют в качестве вторичного мессенджера сАМР. Как одно вещество может регулировать разные процессы?
17. Фосфофруктокиназа - ключевой регуляторный фермент. Назовите главный аллостерический регулятор этого фермента. Как осуществляется контроль за его содержанием в печени?
18. Для синтеза глюкозы в печени необходим фосфо- енолпируват. Однако его образование в печени окажется очень неэффективным, если фосфоенолпируват будет дефосфорилироваться под действием пируваткиназы с образованием пирувата. Как избежать этого холостого цикла? Почему этот механизм не подходит для мышц?
19. Как глюкагон вызывает высвобождение жирных кислот из жировых клеток?