БИОХИМИЯ И МОЛЕКУЛЯРНАЯ БИОЛОГИЯ - В. ЭЛЛИОТ - 2002
ГЛАВА 17. ЗАЩИТНЫЕ ФЕРМЕНТАТИВНЫЕ МЕХАНИЗМЫ ОРГАНИЗМА
Иммунная система - главный механизм, защищающий нас от воздействия болезнетворных патогенов (см. главу 25). Однако организму приходится защищаться и от многого другого. В этой главе речь пойдет о защитных механизмах, которые связаны со своеобразными ферментативными реакциями. У них мало общего между собой, и при сопоставлении они выглядят случайным набором превращений. Но все это жизненно важные реакции, и выполняют они общую задачу - защиту организма.
Свертывание крови
Свертывание (или коагуляция) крови имеет целью образование сгустков, которые предотвращают кровотечение, затягивая раны в поврежденных сосудах. По понятным причинам такой физиологический ответ должен быть быстрым и массированным, хотя первоначальный сигнал, с химической точки зрения, очень слаб. Отсюда возникает необходимость эффективного усиления этого сигнала.
Мы уже видели, как биохимическое усиление сигнала достигается с помощью каскада реакций (см. с. 170). Суть такого усиления в том, что фермент, являющийся продуктом предыдущей ферментативной реакции, активирует другой фермент, а тот, в свою очередь, следующий и т. д. В результате лавинообразно нарастает число вовлеченных в работу ферментов и продуктов очередной реакции. Свертывание крови удобно рассматривать как совокупность двух процессов: каскадно развивающейся активации фермента, образующего сгусток, и образование самого сгустка. Каскадная активация основана на ограниченном протеолизе: неактивные предшественники протеиназ активируются после того, как в их молекулах произойдет разрыв определенных пептидных связей (ср. образование трипсина из трипсиногена; см. с. 75). Все необходимые белки-предшественники протеиназ исходно присутствуют в крови в ожидании сигнала о повреждении стенок сосудов. До этого момента они неактивны.
Что служит сигналом к образованию сгустка?
Свертывание крови осуществляется с помощью двух механизмов.
1. В нормальных условиях кровеносные сосуды изнутри выстланы слоем эндотелиальных клеток. Если этот слой будет нарушен, обнажатся лежащие под ним структуры, в том числе коллагеновые волокна. Когда свойства внутренней поверхности сосуда изменятся, первой реакцией на это будет «наложение временного пластыря» на поверхностный участок благодаря агрегации близлежащих кровяных пластинок (тромбоцитов). Пусковым механизмом для образования сгустка является адсорбция на поврежденной поверхности ряда белков крови, что приводит к взаимной аутокаталитической активации двух протеиназ. Одну из них называют фактором XII (здесь непросто разобраться в номенклатуре: фактор может оказаться либо ферментом, либо кофактором фермента, а нумерация вовсе не соответствует очередности участия в процессе). Фактор XII запускает трехэтапный каскад реакций, результатом которого является активация еще одной протеиназы - фактора X. А она, в свою очередь, активирует протромбин,превращая его в главный фермент свертывания крови - протеиназу тромбин. Именно тромбин непосредственно участвует в образовании сгустков крови, или тромбов. Тем, кто уже знает, что названия ферментов заканчиваются на -аза, напомним, что за давно известными протеиназами сохранены традиционные названия: пепсин, трипсин, химотрипсин и тромбин.
2. Все компоненты описанного выше внутреннего механизма запуска свертывания крови находятся в ней самой. Поэтому кровь свертывается даже вне организма: достаточно налить ее в стеклянную пробирку, поверхность которой для крови будет как бы поврежденной стенкой сосуда.
Существует, однако, и другой, внешний механизм свертывания крови, при котором сигнал приходит от поврежденных тканей. Таким сигналом служит белковый комплекс, называемый тканевым фактором. Суть его действия заключается в том, что он активирует протеиназу, которая затем активирует фактор X, а дальше все развивается по уже описанному сценарию. Оба способа инициации свертывания показаны на рис. 17.1.
Рис. 17.1. Внутренний и внешний механизм свертывания крови. Для простоты не приводятся названия многочисленных протеиназ и других факторов, вовлеченных в этот процесс (их всего тринадцать). Все эти протеиназы строго специфичны. Недостаток фактора VIII приводит к заболеванию - гемофилии А
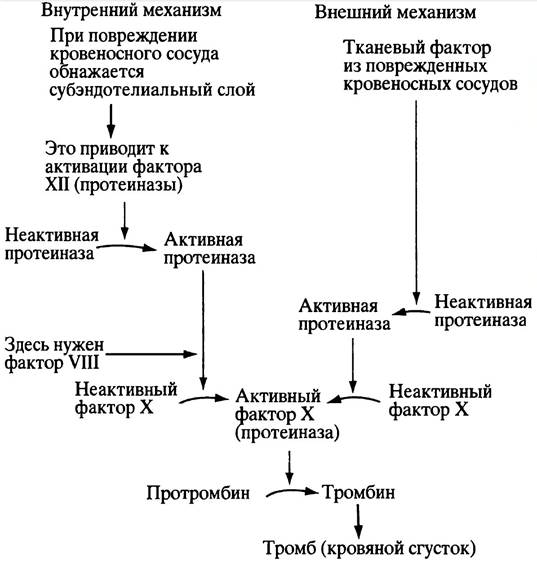
В лабораторных условиях (in vitro) кровь свертывается быстрее по второму из этих механизмов. Известно, однако, заболевание гемофилия А, при котором внутренний механизм свертывания крови нарушается из-за отсутствия фактора VIII, необходимого для протеолитической активации фактора X. Казалось бы, этот дефект может быть компенсирован внешним механизмом, в котором фактор VIII не принимает участия. Но в физиологических условиях оба механизма работают слаженно и взаимозависимо, как единое целое.
Как тромбин вызывает образование тромбов?
В крови присутствует белок фибриноген. Его молекула состоит из двух палочкообразных субъединиц, каждая из которых образована тремя полипептидными цепями. В области N-концевых участков цепей субъединицы соединены тремя дисульфидными мостиками. Поблизости от них в двух цепях из трех содержатся отрицательно заряженные пептидные фрагменты - фибринопептиды, препятствующие ассоциации мономеров фибриногена (рис. 17.2). Тромбин превращает фибриноген в фибрин, отщепляя фибринопептиды. Благодаря этому открывается возможность для спонтанной агрегации фибрина за счет межмолекулярных нековалентных взаимодействий. Участки на концах мономера фибрина связываются с комплементарными участками в середине соседнего мономера, так что в ходе полимеризации возникает неустойчивая структура, называемая мягким сгустком (рис. 17.3). После того как боковые группы соседних мономерных молекул фибрина скрепятся ковалентными сшивками, мягкий сгусток превращается в плотный нерастворимый твердый сгусток.
Рис. 17.2. Превращение мономеров фибриногена в мономеры фибрина. Каждая половинка мономерного фибриногена состоит из трех полипептидных цепей, две из которых содержат отрицательно заряженные фибринопептиды
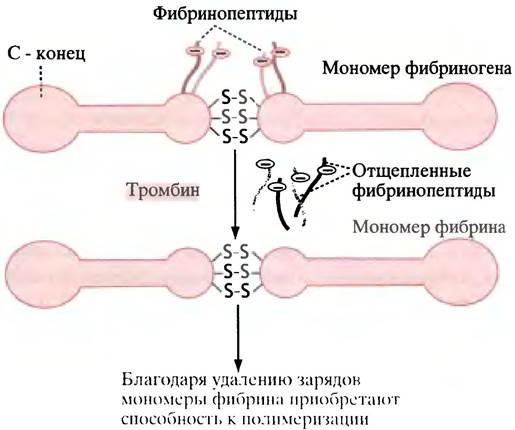
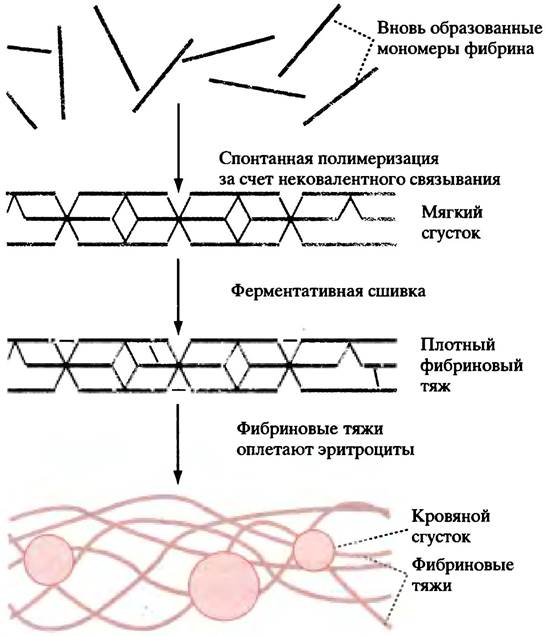
Рис. 17.3. Образование фибриновых тяжей. Тяжи образуются благодаря спонтанной полимеризации фибриновых мономеров и их последующей ферментативной сшивке (места и число сшивок в значительной мере произвольны). Мономеры фибриногена полимеризоваться не могут, поскольку несут значительный отрицательный заряд, а места потенциальной ассоциации экранированы фибринопептидами
Сшивками служат амидные связи, образующиеся в ходе реакции трансамидирования между остатком глутамина в одной полипептидной цепи и лизина в другой:
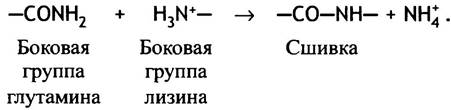
Образовавшийся сгусток объединяет в единое целое фибриновые тяжи и запутывающиеся в них клетки крови.
Регуляция свертывания крови
Если свертывание крови не ограничится областью повреждения сосуда, оно может нанести непоправимый ущерб организму, поскольку носит аутокаталитический характер и может распространиться на все кровяное русло. Однако существует целый ряд препятствующих этому защитных приспособлений. Во-первых, в крови
присутствуют ингибиторы протеиназ (в том числе антитромбин), которые тормозят процесс свертывания. Во-вторых, стенки сосудов содержат сульфополисахарид гепарин,усиливающий действие ингибиторов. В-третьих, имеется специальная протеиназа плазмин, растворяющая сгустки. Плазмин сам образуется из неактивного плазминогена под воздействием белка - тканевого активатора плазминогена ТРА (от англ. Tissue Plasminogen Activator), который выделяется из поврежденных тканей. В последнее время его используют в терапевтических целях. Хотя ТРА присутствует в тканях в ничтожном количестве, он стал вполне доступен, поскольку его научились получать с помощью методов генетической инженерии (см. главу 24). Все эти защитные механизмы препятствуют распространению свертывания крови, ограничивая его областью, непосредственно примыкающей к месту повреждения сосуда, послужившему инициатором образования сгустка. Регуляция свертывания крови очень сложна. Неудивительно, что нарушения в системе свертывания крови являются причиной гибели многих людей.
Крысиный яд, свертывание крови и витамин К
Широко распространенный крысиный яд варфарин предотвращает свертывание крови, благодаря чему грызуны погибают от внутренних кровотечений, вызванных ничтожными и в нормальных условиях неизбежными повреждениями кровеносных сосудов. В медицине варфарин используют для профилактики образования тромбов после инсульта. По своей структуре он похож на витамин К (от нем. Koagulation - коагуляция, свертывание) и действует как его конкурентный ингибитор (рис. 17.4).
Рис. 17.4. Структура витамина К (а) и варфарина (б). Витамин К необходим для свертывания крови, а варфарин является его антагонистом
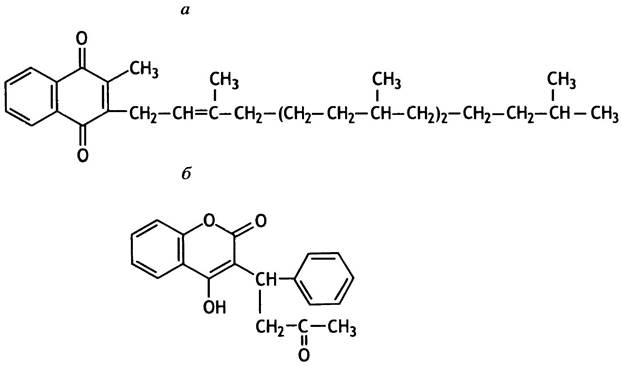
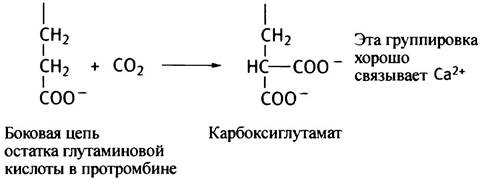
Витамин К необходим для превращения протромбина в тромбин. Он служит кофактором в необычной ферментативной реакции карбоксилирования остатка глутаминовой кислоты в протромбине.
Смысл такой модификации в том, что остаток карбоксиглутамина хорошо связывает ионы кальция, которые необходимы для активации тромбина. Аналогичным образом модифицируются и другие факторы, участвующие в каскаде.
Защита от попавших в организм чужеродных веществ
С крупными чужеродными молекулами имеет дело иммунная система (см. главу 25). Здесь же речь пойдет о низкомолекулярных соединениях, которые не являются продуктами жизнедеятельности патогенных организмов.
В организм современного человека попадает огромное число самых разных посторонних химических соединений, которые называют ксенобиотиками (от греч. ксено - чужой). Среди них лекарства, пестициды, гербициды и другие продукты химической промышленности, а также терпены, алкалоиды и дубильные вещества растительного происхождения. Многие из них плохо растворяются в воде, зато хорошо растворимы в жирах. Они накапливаются в углеводородном слое мембран, в вакуолях жировых клеток и не выводятся из организма с мочой. Чтобы избежать вредных последствий накопления таких веществ, необходимо сделать их растворимыми в воде. Существует несколько способов модификации ксенобиотиков, способствующих их выведению из организма, однако главную роль в этом процессе играют ферменты семейства цитохрома Р450 в печени. Наиболее типичной реакцией, которую катализируют эти ферменты, является гидроксилирование как алифатических, так и ароматических группировок в молекулах ксенобиотиков. Затем уже другие ферменты замещают водород в гидроксильных группах на высокополярные остатки (обычно глюкуроновой кислоты), после чего вещество становится достаточно растворимым, чтобы быть удаленным с мочой.
Перейдем теперь к более детальному рассмотрению этих процессов, начиная с системы цитохрома Р450.
Цитохром Р450
Как и цитохромы дыхательной цепи (см. с. 123), цитохром Р450 (для краткости просто Р450) представляет собой гемопротеин. Его название указывает на то, что он окрашен (от англ. Pigment) и что максимум поглощения комплекса Р450 с окисью углерода лежит в области 450 нм. Окись углерода не имеет никакого отношения к функции Р450; она добавляется лишь для того, чтобы облегчить определение содержания Р450 по интенсивности спектра поглощения. Р450 находится на внутренней стороне мембраны эндоплазматического ретикулума. Катализируемые им реакции обычно можно описать уравнением:
АН + О2 + NADPH + Н+ —> А-ОН + Н2О + NADP+.
Такие реакции называют монооксигеназными, потому что в модифицируемое вещество внедряется только один атом из молекулы кислорода (О2), второй же восстанавливается до воды с помощью NADPH. Р450 называют также оксигеназой смешанного действия, поскольку он не только гидроксилирует субстрат, но и восстанавливает О2 до Н2О. Перенос электронов от NADPH к Fe3+ в геме цитохрома осуществляется Р450-редуктазой, также связанной с мембраной эндоплазматического ретикулума.
Мы уже встречались с ферментом подобного типа при гидроксилировании фенилаланина (см. с. 197). Обратите внимание на разницу между окислением и оксигенированием. Окисление подразумевает удаление электронов, а оксигенирование - внедрение в молекулу субстрата атома кислорода из молекулы О2 (не путать с оксигенированием гемоглобина, когда молекула О2 обратимо связывается с атомом железа в геме).
Поразительно, что система Р450 справляется с окислением огромного числа соединений, с которыми живые организмы стали вступать в контакт только с развитием современной химической промышленности. Об эволюционной целесообразности этой системы можно только гадать, но она позволяет нам выжить в созданных нами новых условиях. Не исключено, что действие изначально было направлено на терпены, алкалоиды и другие вещества растений, которые защищают их от поедания животными. Разносторонность системы Р450 определяется двумя факторами: во-первых, каждый из ферментов этой системы обладает достаточно широкой субстратной специфичностью в пределах определенного класса соединений; во-вторых, спектры субстратной специфичности различных ферментов хотя и разные, но перекрывают друг друга.
Вторичная модификация: присоединение полярных остатков к продуктам реакций, катализируемых Р450
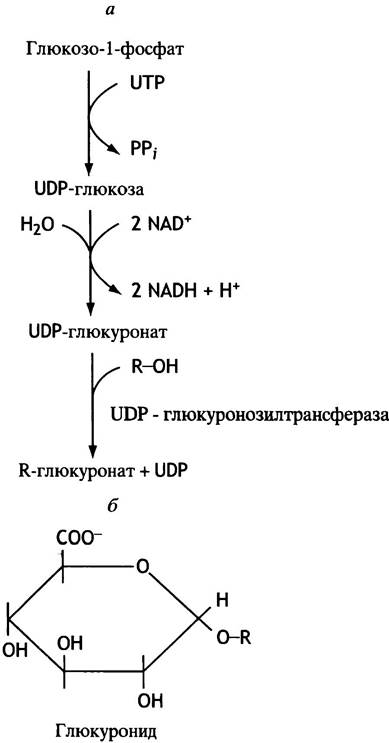
На рис. 17.5 представлена схема, показывающая, как продукты гидроксилирования гидрофобных ксенобиотиков приобретают способность к растворению в воде путем присоединения к ним остатка глюкуроновой кислоты. Этот остаток переносится с глюкуронил-UDР, который образуется при окислении в мембранах эндоплазматического ретикулума UDР-глюкозы (см. с. 87). Ферменты, осуществляющие вторичную модификацию ксенобиотиков, расположены там же.
Рис. 17.5 Система глюкуронилирования (а) и структура глюкуронида (б)
Реакция печени на ксенобиотики
При попадании ксенобиотика (например, фенобарбитала) в клетки печени начинается быстрое увеличение поверхности эндоплазматического ретикулума. Одновременно индуцируются системы глюкуронилирования и Р450: включаются соответствующие гены и синтез компонентов этих систем многократно усиливается. Когда ксенобиотик будет полностью удален, все возвращается к норме. Такая быстрая реакция позволяет избежать потенциальной опасности, связанной с попаданием в организм посторонних веществ. Однако она создает трудности для химиотерапии. Эффективность многих лекарств ограничена скоростью их метаболического разрушения, тем более что мощность детоксицирующих ферментных систем тем больше, чем дольше эти лекарства присутствуют в организме. К сожалению, у столь мощной системы детоксикации есть обратная сторона. Те же лекарства обычно химически инертны и связываются с молекулами, на которые направлено их действие, благодаря нековалентным взаимодействиям. Однако при окислении цитохромами Р450 они часто превращаются в реакционноспособные соединения, причиняющие массу неприятностей. И не только лекарства! Совершенно безвредный бензпирен, который присутствует в табачном дыме, попадая в печень и легкие курильщика, окисляется там, превращаясь в химически активные канцерогенные соединения, реагирующие с ДНК.
Мишенями для цитохромов Р450 служат не только ксенобиотики. Они участвуют также в разрушении гема и стероидных гормонов. В митохондриях надпочечников цитохромы Р450 катализируют отдельные стадии синтеза стероидных гормонов из холестерина.
Множественная защита
Защитить организм от ксенобиотиков можно, воспрепятствовав их накоплению в клетках. В плазматической мембране многих клеток, в том числе и разных тканей человека, присутствует гликопротеин, ответственный за выведение разнообразных веществ из клетки за счет энергии гидролиза АТР. Круг таких соединений весьма широк, и в него, в частности, попадает много лекарственных препаратов и цитотоксических веществ. О биологической важности этой транспортной системы можно судить по тому, что с ее помощью осуществляется транспорт стероидных гормонов из клеток надпочечников. Транспортируемые таким образом вещества могут различаться по строению, но все они обладают амфипатическими свойствами (содержат полярные и гидрофобные группы) и растворимы в жирах.
Защита организма от воздействия собственных протеиназ
В главе 4 рассказывалось, как пищеварительная система избегает разрушительного действия собственных протеолитических ферментов. Однако протеиназы в организме присутствуют повсюду, так что решение этой проблемы актуально и вне желудочно-кишечного тракта.
Здесь мы расскажем лишь об одном из ее аспектов, связанном с ферментом эластазой из нейтрофилов. Нейтрофилы - фагоцитирующие белые кровяные тельца, которые концентрируются вокруг инфицированных и воспаленных участков тканей. Здесь нейтрофилы начинают секретировать эластазу, которая разрушает прилежащие участки соединительной ткани. Действие эластазы направлено на один из ее главных компонентов - белок эластин.
В легких воздух попадает в пузырьковидные образования - альвеолы, с их помощью увеличивается поверхность газообмена между воздухом и кровью. Нейтрофилы присутствуют в альвеолах и выделяют эластазу, однако ее разрушительное действие на легочные структуры предотвращается белковым ингибитором α1-антитрипсином (α1-антипротеиназой), который секретируется в кровь печенью. Этот ингибитор подавляет активность многих протеиназ, в том числе и трипсина, но особенно он эффективен по отношению к эластазе. Антитрипсин прочно связывается с ферментом, блокируя его каталитический центр.
α1-Антитрипсина в крови вполне достаточно, чтобы защитить легочные альвеолы от эластазы. Известен, однако, генетический дефект, при котором содержание антитрипсина в крови существенно уменьшается. В результате эластаза может частично разрушать легочную ткань, что проявится в увеличении размера альвеол и уменьшении поверхности газообмена. У людей развивается эмфизема легких.
Эмфиземе подвержены и курильщики табака. Это происходит по двум причинам. Во-первых, раздражение, вызываемое табачным дымом, привлекает в легкие нейтрофилы, что способствует увеличению там содержания эластазы. Во-вторых, компоненты дыма инактивируют α1-антитрипсин, окисляя в нем функционально важный остаток метионина в сульфоксид (S —> S = 0). Этого достаточно, чтобы предотвратить инактивацию эластазы α1-антитрипсином и способствовать протеолизу легочной ткани, что ведет к эмфиземе. Существуют и другие антипротеиназы, но α1-антитрипсин имеет, пожалуй, самое важное значение.
Защита от активных форм кислорода
Молекулярный кислород служит конечным акцептором электронов в митохондриальной дыхательной цепи (см. главу 7). Его восстановление описывается уравнением:
O2 + 4е- + 4Н+ —> 2Н2O.
На первый взгляд, нет причин думать о какой-либо защите, поскольку и кислород, и вода вполне безвредны. Однако восстановление кислорода может привести к образованию не только воды, но и других продуктов, крайне опасных для организма. Переход от анаэробного метаболизма к использованию кислорода как акцептора электронов был важнейшим достижением эволюции. Опасность возникает при одноэлектронном восстановлении кислорода, которое приводит к появлению реакционноспособного анион-радикала - супероксида (радикалами называют молекулы с неспаренным электроном):
O2 + е- —> O2-.
Неспаренный электрон находит партнера, атакуя ковалентную связь другой молекулы.
Супероксид в организме образуется по нескольким причинам. В норме восстановление молекулярного кислорода в дыхательной цепи происходит только с помощью цитохромоксидазы, которая отдает ему все четыре электрона, необходимые для образования воды. Однако неизбежная утечка электронов с промежуточных переносчиков на кислород приводит к генерации некоторого количества O2-. Кроме того, мутации митохондриальной ДНК могут сопровождаться блокированием электрон- транспортных путей, и электроны будут использоваться на образование супероксида (например, прямое окисление убихинона кислородом). Такого рода мутации особенно опасны, потому что митохондрии лишены системы репарации ДНК (см. с. 259).
Другим источником супероксида может служить спонтанное окисление гемоглобина. В норме гемоглобин (Нb) обратимо связывает кислород: Нb + O2 —> + НbO2. Однако оксигемоглобин (НbO2) с некоторой вероятностью превращается в метгемоглобин (содержащий не Fе2+, а Fе3+) и супероксид O2-.
Известно также, что образование супероксида вызывает ионизирующая радиация.
Кроме супероксида, в организме образуется и такое опасное вещество, как перекись водорода (Н2O2). Это происходит при окислении некоторых метаболитов оксидазами (цитохромоксидаза дыхательной цепи к ним не относится).
Фагоциты, захватывая бактериальные клетки, потребляют много кислорода. Он восстанавливается с помощью NADPH с образованием супероксида. Последний, попав в вакуоль, превращается в перекись водорода, которая способствует разрушению бактериальной клетки. Нейтрофилы, в избытке собирающиеся в воспаленных суставах, также способны выделять супероксид, внося тем самым существенный вклад в развитие артритов.
Количество образующегося в организме супероксида ничтожно мало. Однако и этого достаточно, чтобы вовлечь в нежелательные превращения большое число других молекул. Дело в том, что супероксид - радикал, а это означает, что один из продуктов его реакций с обычными молекулами непременно должен быть тоже радикалом. А поскольку все радикалы, за редкими исключениями, крайне реакционноспособны, этот продукт, в свою очередь, вступит в какую-нибудь другую реакцию, порождая очередной радикал. Таким образом, процесс носит цепной характер и потенциально может продолжаться бесконечно. Остановиться он может либо вследствие рекомбинации радикалов с образованием обычных молекул (это маловероятно из-за низкой концентрации радикалов), либо из-за аномально низкой реакционной способности дочерних радикалов.
Какие дефекты в организме обусловлены протеканием таких цепных реакций, пока точно не известно, но полагают, что супероксид причастен к старению, образованию катаракты хрусталика, инфаркту миокарда и т. д. Существуют три основных способа защиты от супероксидов - один химический и два ферментативных.
Витамины С и Е как ловушки кислородных радикалов
Чисто химический подход к обезвреживанию супероксида и блокированию цепных реакций заключается в применении антиоксидантов. Так называют вещества, которые, вступая в реакции со свободными радикалами, превращаются в радикалы с малой реакционной способностью. На них цепной процесс прерывается. Главными природными тушителями цепных реакций являются аскорбиновая кислота (витамин С) и α-токоферол (витамин Е). Первая растворима в воде, а второй в жирах, так что в тандеме они способны защитить и компоненты цитозоля, и мембранные липиды. Эти два вещества не единственные антиоксиданты; аналогичной активностью обладают, например, β-каротин и мочевая кислота. Эффективным антиоксидантом служит также билирубин - продукт расщепления гема гемоксигеназой (см. с. 370). Интересно, что гемоксигеназа активируется продуктами частичного восстановления кислорода (их накопление называют окислительным стрессом; он может быть вызван, например, ионизирующим излучением). Пока неясно, однако, может ли образование билирубина рассматриваться как защитная реакция организма.
Ферментативное уничтожение супероксида супероксиддисмутазой
По-видимому, все ткани животных содержат фермент супероксиддисмутазу. Больше всего ее в митохондриях, есть она и в лизосомах, и в пероксисомах (см. главу 16). Супероксиддисмутаза присутствует не только в клетках, но и в плазме крови, лимфе, синовиальной жидкости. Этот фермент катализирует реакцию:
2О2- + 2Н+ —> Н2О2 + О2.
Перекись же водорода разлагает другой фермент - каталаза:
2Н2О2 —> 2Н2О + О2.
Перекись водорода появляется не только в результате дисмутации супероксида, но также благодаря действию оксидаз. FАD-содержащие оксидазы катализируют реакции, которые в обобщенном виде выглядят так:
АН2 + O2 —> А + Н2O2.
К их числу принадлежит, в частности, ксантиноксидаза, участвующая в метаболизме пуринов (см. главу 18).
Перекись водорода опасна тем, что в присутствии ионов тяжелых металлов (например, Fе2+) она распадается с образованием высокореакционноспособных гидроксильных радикалов (не путать с безобидными гидроксильными анионами), атакующих ДНК и другие биомолекулы:
H2O2 + Fе2+ —> Fе3+ + ОН- + ОН-.
Оба фермента - и супероксид дисмутаза, и каталаза - защищают ткани организма от атак радикалов. Однако есть еще один фермент, разрушающий перекись водорода, - глутатионпероксидаза. Его защитная функция важна для мозга, который содержит мало каталазы.
Стратегия защиты с помощью глутатиона
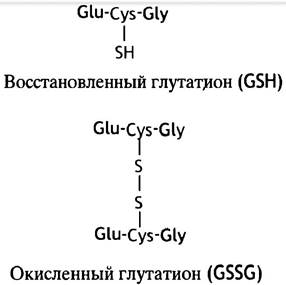
Глутатионом называется тиолсодержащий трипептид y-глутамил-цистеинил-глицин (GSН; рис. 17.6). Он присутствует в большинстве клеток и используется главным образом как восстанавливающий агент, например, для поддержания в восстановленном состоянии цистеиновых остатков в белках. Эту защитную функцию глутатион выполняет без участия ферментов. Другая защитная функция глутатиона связана с восстанавлением перекиси водорода (а также органических гидроперекисей R-O-OH).
Рис. 17.6 Структура восстановленной (GSH) и окисленной (GSSG) форм глутатиона Glu, Cys, Gly - трехбуквенное обозначение аминокислот глутамата, цистеина и глицина соответственно. Однобуквенная система используется для записи протяженных аминокислотных последовательностей
Эта реакция катализируется глутатионпероксидазой:
Н2O2 + 2GSH —> GSSG + 2Н2O.
Окисленный глутатион (GSSG) затем восстанавливается NADPH при участии глутатионредуктазы:
GSSG + NADPH + Н+ —> 2GSH + NADP+.
Целостность эритроцитов зависит от глутатиона, который восстанавливает ферригемоглобин (метгемоглобин) в феррогемоглобин и разрушает перекиси. Это объясняет целесообразность существования в эритроцитах пентозофосфатного метаболического пути, который поставляет NADPH (см. рис. 13.1), необходимый для восстановления глутатиона.
Людям с дефектной глюкозо-6-фосфатдегидрогеназой - первым ферментом пентозофосфатного пути - вполне хватает этой активности в обычных условиях. Однако при накоплении в их клетках перекисей (например, после приема антималярийного лекарства примахина) возникает дефицит NADPH, необходимого для восстановления GSSG. Это приводит к повреждению плазматической мембраны эритроцитов и гемолизу последних.
В этой главе мы уделили внимание защитным механизмам у животных. Однако они существуют и у растений, причем более разнообразные, возможно потому, что у них нет иммунной системы и они не могут ни убежать, ни прогнать хищника. Вот пример, взятый наугад, некоторые растения обладают ферментом хитиназой, который разрушает хитиновый покров насекомых.
Вопросы к главе 17
1. Свертывание крови - каскадный процесс. В чем его смысл?
2. Объясните, каким образом тромбин участвует в образовании кровяного сгустка.
3. Спонтанная полимеризация фибриновых мономеров приводит к образованию мягкого сгустка. Как он превращается в более стабильную структуру?
4. Какова роль витамина К в свертывании крови?
5. Какова функция цитохрома Р450?
6. Зачем нужен NАDРН в реакциях оксигенирования?
7. Какова функция глюкуронил-UDР при выведении из организма нерастворимых в воде соединений?
8. Что такое множественная защита?
9. Почему курение вызывает эмфизему легких?
10. Что такое супероксид?
11. Какие механизмы защищают организм от вредного действия супероксида?