БІОХІМІЯ - Лабораторний практикум - НАУ 2015
МОДУЛЬ I
БІОХІМІЧНІ КОМПОНЕНТИ КЛІТИНИ
Лабораторна робота 3
ЯКІСНІ РЕАКЦІЇ НА МОНОСАХАРИДИ, ВІДНОВЛЮВАЛЬНІ ДИСАХАРИДИ, КРОХМАЛЬ
Мета роботи: опанувати методи виявлення в розчинах моносахаридів (глюкози, фруктози) та відновлювальних дисахаридів окисно-відновними реакціями; уміти виявляти крохмаль у розчинах за допомогою йод-крохмальної реакції.
Основні теоретичні відомості
Прості вуглеводи (моносахариди, або монози, або прості цукри) — це полігідроксиальдегіди або полігідроксикетони. Вони класифікуються на альдози та кетози залежно від наявності альдегідної або кетогрупи. Інша класифікація залежить від кількості атомів карбону (тріози, тетрози, пентози, гексози, гептози і так далі). Ці дві класифікації зручно поєднувати. Найпоширенішими моносахаридами є альдогексози, альдопентози, кетогексози. Альдози можуть окиснюватися до відповідних кислот, одночасно відновлюючи солі металів. Ця властивість використовується для проведення якісних та кількісних реакцій для їх виявлення.
Складні вуглеводи у процесі гідролізу розпадаються на прості (прості вуглеводи не гідролізуються). Дисахариди — це найпростіші складні цукри. Вони складаються з двох моносахаридів, з’єднаних глікозидним зв’язком. Дисахариди поділяються на відновлювальні та невідновлювальні (редукуючі та нередукуючі). Відновлювальні дисахариди (наприклад лактоза, целобіоза чи мальтоза) можуть окиснюватися до відповідних кислот, відновлюючи солі металів. Таким чином, ці дисахариди беруть участь у реакціях, характерних для моносахаридів-альдоз. Але нередукуючі дисахариди (наприклад сахароза) в подібні реакції не вступають. Для їх виявлення найчастіше використовують методи, що ґрунтуються на гідролізі дисахаридів до моносахаридів із наступним виявленням продуктів гідролізу — моносахаридів.
Полісахариди розрізняться за довжиною ланцюга, хімічною природою мономерних одиниць, що повторюються (якщо мономери однакові, це гомополісахариди, якщо різні — гетерополісахариди), ступенем розгалуження (нерозгалужені, або лінійні, полісахариди мають однакові зв’язки між монозами; у розгалужених полісахаридах монози з’єднані різними зв’язками). Полісахариди не містять вільних редукуючих груп, тому вони не мають відновлювальної здатності. Продуктами повного гідролізу полісахаридів за наявності кислот чи специфічних ферментів є моносахариди, які мають редукуючі властивості.
Крохмаль — основний резервний вуглевод рослин. Він складається з двох гомополісахаридів — амілози та амілопектину, мономерними ланками яких є глюкоза. Амілоза має лінійну структуру, залишки глюкози з’єднані між собою α-1,4-глікозидними зв’язками. Вторинна структура амілози має вигляд спіралі, внутрішній діаметр якої відповідає розміру молекули йоду (0,5 нм). Тому за наявності молекулярного йоду в розчині він вбудовується в спіраль амілози з утворенням нестійких комплексів, що зумовлює синє забарвлення. Амілопектин має значно більшу молекулярну масу, ніж амілоза, він не дає позитивної йод-крохмальної реакції, під час нагрівання утворює клейстер. Основний тип зв’язку між залишками глюкози — α-1,4-глікозидний, так само, як і в молекулі амілози. Але через кожні 25—30 моноз зв’язок між ними —
α-1,6-глікозидний, це місця або точки розгалуження ланцюга.
Аналог рослинного крохмалю у тварин — глікоген. Він також є гомополісахаридом. Будова глікогену нагадує будову амілопектину — залишки глюкози з’єднані між собою такими самими зв’язками, але місця розгалуження частіші — через кожні 5—6 моноз. Кінцевим продуктом гідролізу як крохмалю, так і глікогену є глюкоза.
Обладнання: скляні палички, пробірки, піпетки градуйовані, крапельниці, штатив для пробірок, водяна баня, лабораторний термометр, лопаточка чи шпатель, годинник, пальник.
3.1. Реакція Троммера
Матеріали та реактиви: розчини глюкози, гідроксиду натрію, сульфату міді (всі 0,5 %—і).
Порядок виконання роботи
Розчини альдоз (наприклад глюкози) у лужному середовищі відновлюють під час нагрівання оксиду міді(II) у геміоксид міді, а самі окиснюються до альдонових кислот. Реакція за участю глюкози:
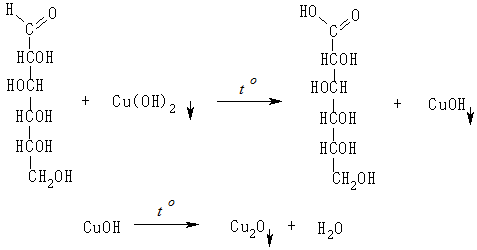
У пробірку до 0,5 мл розчину гідроксиду натрію додають дві краплі розчину сульфату міді. Випадає осад гідроксиду міді(II) блакитного кольору. Додають 1 мл розчину глюкози, вміст пробірки перемішують. Осад розчиняється, а розчин набуває синього забарвлення. Під час його обережного нагрівання в полум’ї пальника до кипіння спостерігається випадіння жовтого осаду гідроксиду міді(І) або червоного осаду геміоксиду міді.
3.2. Реакція Фелінга
Матеріали та реактиви: розчин глюкози (5 %-й), реактив Фелінга (див. лабораторну роботу 2).
Порядок виконання роботи
У пробірку додають 1 мл розчину глюкози та 1 мл реактиву Фелінга. В реактиві Фелінга іони міді(II) перебувають у вигляді комплексної сполуки з тартратами. Механізм реакції всіх редукуючих вуглеводів із реактивом Фелінга такий самий, як і в реакції Троммера. Перевагою реактиву Фелінга є те, що мідь у разі надлишку реактиву не випадає у вигляді оксиду міді(II):
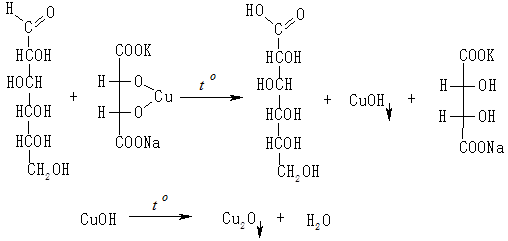 Уміст пробірки перемішують і нагрівають у полум’ї пальника до кипіння. Спостерігають утворення червоного осаду геміоксиду міді.
Уміст пробірки перемішують і нагрівають у полум’ї пальника до кипіння. Спостерігають утворення червоного осаду геміоксиду міді.
3.3. Реакція Селіванова на кетози
Матеріали та реактиви: кристалічний резорцин, 5 %-й розчин фруктози, 25 %-й розчин соляної кислоти.
Порядок виконання роботи
У пробірку наливають 1 мл розчину фруктози, 0,5 мл розчину соляної кислоти та додають кілька кристалів резорцину. Суміш нагрівають на водяній бані протягом 5—10 хв за температури 80 °С до появи вишнево-червоного кольору.
Під час нагрівання фруктози чи інших кетоз із соляною кислотою утворюється оксиметилфурфурол. Сполука, що утворюється під час конденсації оксиметилфурфуролу із резорцином, забарвлена у вишнево-червоний колір.
Рівняння реакції за участю фруктози має такий вигляд:
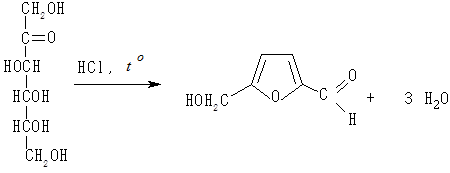
Спостерігають появу забарвлення.
3.4. Відновна здатність лактози та мальтози
Матеріали та реактиви: розчини лактози, мальтози, гідроксиду натрію, сульфату міді (всі 0,5 %-і).
Порядок виконання роботи
В одну пробірку наливають 2 мл розчину лактози, в іншу 2 мл розчину мальтози. В обидві пробірки потім додають по 1 мл розчину гідроксиду натрію і по п’ять крапель розчину сульфату міді. Пробірки обережно нагрівають у полум’ї пальника й спостерігають утворення червоного осаду геміоксиду міді.
Завдяки наявності вільної альдегідної групи в молекулі лактози, целобіози та мальтози ці дисахариди мають редукуючі властивості й можуть брати участь у реакціях відновлення, зокрема, дають позитивну реакцію Троммера.
3.5. Реакція крохмалю з йодом
Матеріали та реактиви: реактив Люголя (1 г йоду та 2 г йодистого калію розчиняють у 15 мл води й потім розводять водою до об’єму 300 мл); 0,1 %-й розчин крохмалю, 10 %-й розчин гідроксиду натрію чи калію.
Порядок виконання роботи
У пробірку наливають 2 мл розчину крохмалю, додають одну-дві краплі розчину Люголя. Уміст пробірки перемішують. Унаслідок взаємодії крохмалю з йодом утворюється комплексна адсорбційна сполука синього кольору. Переносять 1 мл рідини в іншу пробірку, куди додають 1 мл розчину гідроксиду натрію чи калію. Спостерігають знебарвлення вмісту пробірки, що свідчить про взаємодію молекулярного йоду з лугом.
Суміш, що залишилася в пробірці, нагрівають на водяній бані. Спостерігають зникнення синього забарвлення (розчин стає жовтим через вміст йоду). Синій колір знову з’являється під час охолодження. Зникнення забарвлення внаслідок нагрівання зумовлене руйнуванням вторинної структури амілози і вивільненям йоду, з охолодженням вторинна структура відновлюється, нестійкі комплекси крохмалю з йодом також відновлюються, тому колір знову стає синім.
Оброблення експериментальних даних
Побудуйте таблицю, у якій наведіть назви і формули моносахаридів та дисахаридів, класифікуйте їх. Напишіть реакції, якими вони виявляються. Схематично зобразіть вторинну структуру амілози, утворення йод-крохмального комплексу. Напишіть формули фрагментів амілози та амілопектину, назвіть зв’язки між залишками глюкози.
Контрольні запитання та завдання
1. Чому осад гідроксиду міді(II) розчиняється під час перемішування з розчином глюкози? Запишіть рівняння відповідної реакції. Наявність яких функціональних груп вона підтверджує?
2. Наявність якої функціональної групи доводять позитивні реакції Толленса, Троммера, Фелінга? Напишіть ці реакці з глюкозою.
3. До яких моносахаридів належить фруктоза (за кількістю атомів карбону та наявністю функціональних груп)?
4.Що називається таутомерією, мутаротацією? Чи завжди вони є у розчинах моносахаридів та редукуючих дисахаридів?
5. Напишіть таутомерні форми моносахаридів (глюкози, галактози, маннози, фруктози, рибози, дезоксирибози) та редукуючих дисахаридів — мальтози, лактози, целобіози. Дайте їм повні назви.
6. Напишіть реакції Толленса з лактозою, Троммера з целобіозою, Фелінга з мальтозою. Назвіть продукти реакції.
7. Напишіть реакцію гідролізу сахарози, назвіть продукти реакції. Чи будуть позитивними реакції Толленса, Троммера, Фелінга з негідролізованою сахарозою, з сахарозою після гідролізу? Що називається інверсією сахарози, інвертним цукром?
8.Чи властива сахарозі таутомерія? Чи зазнає мутаротації свіжовиготовлений розчин сахарози? Чому?
9. Яку будову має крохмаль? З яких полісахаридів він складається? Який полісахарид зумовлює позитивну йод-крохмальну реакцію, а який — утворення клейстеру? Побудуйте схему утворення клатратного комплексу йоду з амілозою.
10. Яку будову має глікоген? Напишіть фрагмент молекули глікогену.
11.Яку будову має клітковина (целюлоза)? Який моносахарид є її мономерною ланкою?
12. Які сполуки називаються гетерополісахаридами? Які біологічні функції вони виконують? Наведіть приклади.