ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ - 2014
ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
15. ПРИНЦИПЫ РЕГУЛЯЦИИ МЕТАБОЛИЗМА
15.3. Согласованная регуляция гликолиза и глюконеогенеза
У млекопитающих глюконеогенез происходит главным образом в печени и обеспечивает глюкозой остальные ткани при исчерпании запасов гликогена. Как мы отмечали в гл. 14, в глюконеогенезе участвуют многие ферменты гликолиза. Семь реакций гликолиза легко протекают в обратном направлении, а катализирующие их ферменты действуют и в глюконеогенезе (рис. 15-11). Три реакции гликолиза сопровождаются таким значительным уменьшением свободной энергии (табл. 15-3, данные для сердечной мышцы), что протекает необратимо: это реакции, катализируемые гексокиназой, РЕК-1 и пируваткиназой. В глюконеогенезе во всех трех случаях используются обходные пути; например, превращение фруктозо-1,6-бис- фосфата в фруктозо-6-фосфат катализирует фруктозо-1,6-бисфосфатаза (FВРаза-1). Заметьте, что каждая из обходных реакций также характеризуется большой отрицательной величиной ∆G′.
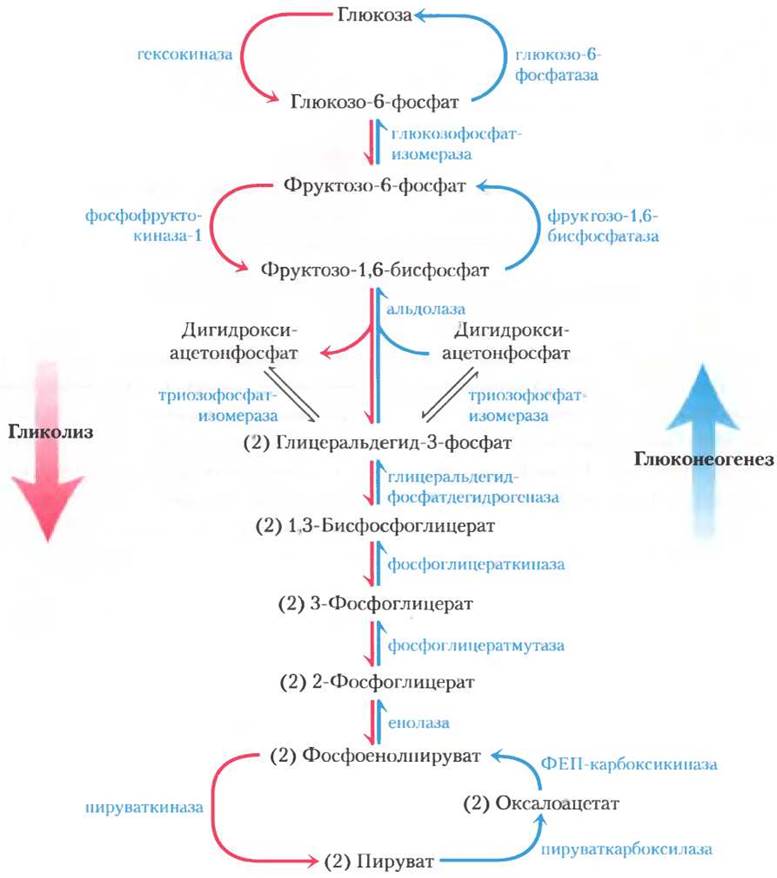
Рис. 15-11. Гликолиз и глюконеогенез. Гликолиз (показан розовым цветом) и глюконеогенез (синий цвет) в печени крысы. Эти процессы протекают в противоположных направлениях. Три стадии гликолиза и глюконеогенеза осуществляются под действием разных ферментов (обходные стадии глюконеогенеза); семь стадий катализируются в обоих направлениях одними и теми же ферментами. Чтобы не усложнять схему, кофакторы не указаны.
Дополнение 15-2. Изоферменты: разные белки, катализирующие одну и ту же реакцию
Четыре формы фермента гексокиназы, обнаруженные в тканях млекопитающих, представляют собой лишь один пример довольно распространенного биологического явления, когда одна и та же реакция катализируется двумя или несколькими различными молекулярными формами фермента. Эти формы, называемые изоферментами (изозимами), могут существовать у одного и того же вида, в одной и той же ткани или даже в одной клетке. Изоферменты обычно различаются по кинетическим свойствам и особенностям регуляции, по используемым кофакторам (например, NADH или NАDРН в случае изоформ дегидрогеназ), а также по внутриклеточной локализации (растворимые или мембраносвязанные). У изоферментов может быть близкая, но не идентичная последовательность аминокислот; во многих случаях эти белки имеют общего эволюционного предка.
Один из первых ферментов, у которого были обнаружены изоформы, — лактатдегидрогеназа (ЛДГ) (с. 91). В тканях позвоночных она существует по меньшей мере в виде пяти изоформ с различной электрофоретической подвижностью. Все формы ЛДГ состоят из четырех полипептидных цепей (каждая с Мr = 33500 Да), но имеют разное сочетание двух типов полипептидов. Полипептидные цепи М (мышечная форма) и Н (сердечная) кодируются двумя разными генами.
Изофермент, преобладающий в скелетных мышцах, состоит из четырех М-цепей, а изофермент, преобладающий в тканях сердца, содержит четыре Н-цепи. В других тканях встречаются изоферменты с различной комбинацией М- и Н-цепей.
Тип |
Состав |
Локализация |
ЛДГ1 |
НННН |
Сердце и эритроциты |
ЛДГ2 |
НННМ |
Сердце и эритроциты |
ЛДГ3 |
ННММ |
Головной мозг и почки |
ЛДГ4 |
НМММ |
Скелетные мышцы и печень |
ЛДГ5 |
ММММ |
Скелетные мышцы и печень |
Эти различия в содержании изоферментов можно использовать для оценки времени и обширности инфаркта миокарда. Повреждение сердечной ткани приводит к попаданию сердечной ЛДГ в кровь. Через короткое время после сердечного приступа общее содержание ЛДГ в крови повышается, причем содержание ЛДГ2 выше, чем ЛДГ1. Спустя 12 ч количества ЛДГ1 и ЛДГ2 почти равны, а через 24 ч наблюдается преобладание ЛДГ1. Такое изменение соотношения ЛДГ1/ЛДГ2 в сочетании с повышением концентрации в крови еще одного сердечного фермента — креатинкиназы — строгое доказательство недавнего инфаркта миокарда. ■
Изоферменты ЛДГ сильно различаются значениями Vmax и Км, особенно по отношению к пирувату. ЛДГ4 осуществляет быстрое превращение пирувата при очень низких концентраций в лактат в скелетных мышцах, тогда как ЛДГ1 вызывает быстрое окисление лактата в пируват в сердце.
В общем случае распределение различных изоформ любого фермента отражает по крайней мере следующие четыре особенности метаболизма.
1. Различие путей метаболизма в разных органах. Например, механизмы регуляции изоферментов гликогенфосфорилазы в мышцах и печени неодинаковы, что свидетельствует о разном назначении расщепления гликогена в этих двух тканях.
2. Локализация и метаболическая функция изоферментов в одной и той же клетке различаются. Пример — изоферменты изоцитратдегидрогеназы в цитозоле и митохондриях (гл. 16).
3. Развитие тканей плода или эмбриона и тканей взрослого организма протекает по-разному. Например, печень плода характеризуется определенным изоферментным составом ЛДГ, который изменяется по мере превращения органа в печень взрослого. Некоторые ферменты катаболизма глюкозы в опухолевых клетках присутствуют в виде форм, характерных для плода, а не для взрослого организма.
4. Различная реакция изоферментов на действие аллостерических модуляторов. Это различие весьма полезно при тонкой регуляции скоростей метаболизма.
Если бы любая из этих трех необратимых стадий протекала одновременно в направлении как гликолиза, так и глюконеогенеза, АТР расходовался бы без совершения какой-либо работы в клетке. Например, РЕК-1 и ЕВРаза-1 катализируют противоположно направленные реакции:

т. е. весь процесс состоит в гидролизе АТР, а никаких метаболических превращений не происходит. Понятно, что одновременное протекание в клетке этих двух процессов с высокими скоростями приводило бы к рассеиванию большого количества химической энергии в виде тепла. Такой тип процесса называют холостым циклом. Однако, как мы увидим позже, подобные циклы могут быть полезны для контроля метаболических путей, поэтому более правильно называть их субстратными циклами. Похожие субстратные циклы имеют место и в двух других участках глюконеогенеза/гликолиза, где используются обходные реакции (рис. 15-11).
Теперь мы более подробно остановимся на механизмах регуляции гликолиза и глюконеогенеза в тех трех участках, где эти пути расходятся.
Глюкозо-6-фосфат по-разному влияет на гексокиназы печени и мышц
Гексокиназа, катализирующая вовлечение свободной глюкозы в путь гликолиза, является регуляторным ферментом. Существуют четыре изофермента гексокиназы (от I до IV), которые кодируются четырьмя разными генами. Вспомните, что разные белки, катализирующие одну и ту же реакцию, называют изоферментами (доп. 15-2). Изофермент гексокиназы, преобладающий в миоцитах (гексокиназа II), имеет высокое сродство к глюкозе — полунасыщение достигается при концентрации глюкозы около 0,1 мМ. Поскольку при поступлении глюкозы из крови (где ее концентрация составляет 4-5 мМ) в миоциты создается довольно высокая внутриклеточная концентрация глюкозы, достаточная для насыщения гексокиназы II, этот фермент обычно действует практически с максимальной скоростью. Гексокиназы I и II из мышц подвержены аллостерическому ингибированию продуктом катализируемых ими реакций глюкозо-6-фосфатом. Как только концентрация глюкозо-6-фосфата превышает нормальный уровень, эти изоферменты подвергаются временному обратимому ингибированию, в результате чего скорость образования глюкозо-6-фосфата уравновешивается скоростью его утилизации, и восстанавливается стационарное состояние.
Гексокиназа IV печени (глюкокиназа) и изоформы гексокиназы в других тканях различаются по чувствительности к ингибирующему действию глюкозо-6-фосфата.
Различие между гексокиназами печени и мышц отражает разные функции этих органов в метаболизме углеводов: мышцы потребляют глюкозу, используя ее для получения энергии, в то время как печень поддерживает гомеостаз глюкозы в крови путем удаления или синтеза глюкозы в зависимости от ее текущей концентрации. В печени преобладает гексокиназа IV (глюкокиназа), которая отличается от мышечных гексокиназ I — III по трем основным параметрам. Во-первых, полу- насыщение гексокиназы IV происходит при более высокой концентрации глюкозы (~10 мМ), чем обычно содержится в крови. Поскольку эффективный переносчик глюкозы в гепатоцитах GLUT2 (на рис. 11-30 показана кинетика переносчика GLUT2 в эритроцитах) способствует быстрому установлению равновесия между концентрацией глюкозы в цитозоле и в крови, высокое значение Км для гексокиназы IV позволяет осуществлять ее регуляцию непосредственно через концентрацию глюкозы в крови (рис. 15-12). При высокой концентрации глюкозы в крови после употребления богатой углеводами пищи избыточная глюкоза переносится в гепатоциты, где гексокиназа IV превращает ее в глюкозо-6-фосфат. Поскольку при содержании глюкозы 10 мМ гексокиназа IV не насыщается, ее активность повышается по мере увеличения концентрации глюкозы до 10 мМ и более. При низкой концентрации глюкозы в крови концентрация глюкозы в гепатоцитах ниже Км для гексокиназы IV, так что образующаяся в ходе глюконеогенеза глюкоза выходит из клетки до того, как подвергается фосфорилированию.
Рис. 15-12. Сравнение кинетических свойств гексокиназы IV (глюкокиназы) и гексокиназы I. Обратите внимание на S-образную зависимость в случае гексокиназы IV и значительно более низкую величину Км в случае гексокиназы I. Когда концентрация глюкозы в крови превышает 5 мМ, активность гексокиназы IV повышается, однако гексокиназа I уже действует со скоростью, близкой к Vmax, и не может реагировать на повышение концентрации глюкозы. Гексокиназы I, II и II1 имеют сходные кинетические свойства.
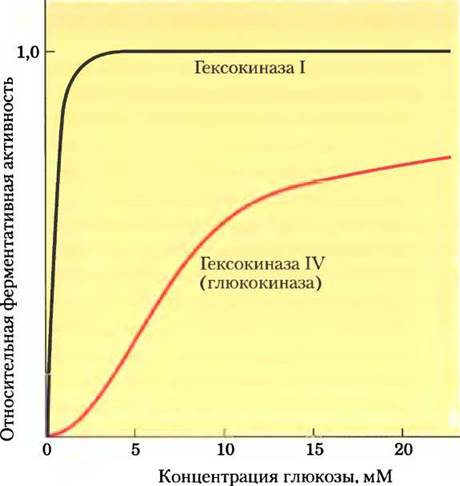
Во-вторых, гексокиназа IV не ингибируется глюкозо-6-фосфатом и продолжает работать, даже когда накопление глюкозо-6-фосфата полностью ингибирует гексокиназы I — III. Наконец, гексокиназа IV подвержена ингибированию специфическим белком печени путем обратимого связывания (рис. 15-13). Более прочное связывание происходит в присутствии аллостерического модулятора фруктозо-6-фосфата. Глюкоза конкурирует за связывание с фруктозо-6-фосфатом и вызывает диссоциацию регуляторного белка из комплекса с гексокиназой IV, снимая ингибирование. Вскоре после употребления богатой углеводами пищи, когда концентрация глюкозы в крови высокая, глюкоза проникает в гепатоциты при помощи GLUT2 и активирует гексокиназу IV по описанному механизму. При голодании, когда концентрация глюкозы понижается до 5 мМ и менее, фруктозо-6-фосфат вызывает ингибирование гексокиназы IV с помощью регуляторного белка, так что печень не конкурирует за глюкозу с другими органами. Интересен механизм ингибирования под действием регуляторного белка: этот белок, локализованный в ядре, связывает гексокиназу IV, благодаря чему она оказывается отделенной от других ферментов гликолиза, находящихся в цитозоле (рис. 15-13). При повышении концентрации глюкозы в клетке этот фермент начинает проникать из цитозоля в ядро до тех пор, пока не устанавливается равновесие. Глюкоза вызывает диссоциацию регуляторного белка из комплекса, гексокиназа IV вновь переходит в цитозоль и начинает фосфорилировать глюкозу.
Рис. 15-13. Регуляция гексокиназы IV (глюкокиназы) путем обособления в ядре. Белковый ингибитор гексокиназы IV локализован в ядре; он впускает гексокиназу IV в ядро при высокой концентрации фруктозо-6-фосфата в печени и высвобождает обратно в цитозоль при высокой концентрации глюкозы.
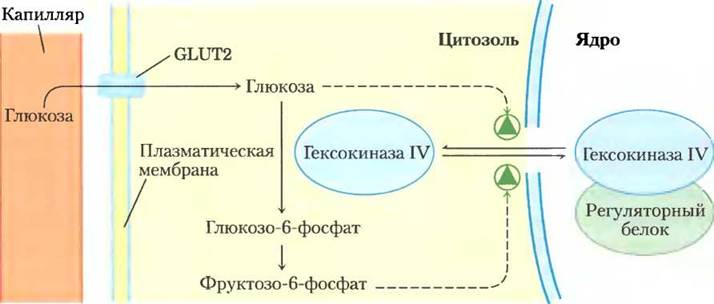
Регуляция гексокиназы IV (глюкокиназы) и глюкозо-6-фосфатазы осуществляется на уровне транскрипции
Регуляция гексокиназы IV осуществляется также на уровне синтеза белка. В тех условиях, когда требуется дополнительная энергия (низкая концентрация АТР, высокая концентрация АМР, активная мышечная деятельность) или происходит активное потребление глюкозы (например, при высокой концентрации глюкозы в крови), активизируется транскрипция гена гексокиназы IV. Регуляция фермента глю- конеогенеза глюкозо-6-фосфатазы с обходом гексокиназной стадии гликолиза осуществляется на уровне транскрипции под действием факторов, стимулирующих образование глюкозы (низкий уровень глюкозы в крови, сигнал глюкагона). Регуляция этих двух ферментов (а также других ферментов гликолиза и глюконеогенеза) на уровне транскрипции обсуждается ниже.
Фосфофруктокиназа-1 и фруктозо-1,6-бисфосфотаза взаимно регулируются
Как мы уже говорили, глюкозо-6-фосфат может вступать на путь гликолиза или участвовать в других метаболических превращениях, в том числе в синтезе гликогена и пентозофосфатном пути. Необратимая в условиях клетки реакция, катализируемая PFK-1, — это первая стадия превращения глюкозы на пути гликолиза. Кроме участка связывания субстрата данный сложный фермент имеет несколько регуляторных участков, в которых связываются аллостерические активаторы или ингибиторы.
АТР — это не только субстрат для PFK-1, но и конечный продукт гликолиза. Высокая концентрация АТР в клетке означает, что скорость его образования превышает скорость расходования; в подобной ситуации АТР начинает ингибировать PFK-1, связываясь в регуляторном участке и снижая тем самым сродство фермента к фруктозо-6- фосфату (рис. 15-14). Аллостерическое действие ADP и АМР, концентрации которых возрастают в тех случаях, когда расход АТР опережает его синтез, снимает ингибирование фермента под действием АТР. Сочетание этих эффектов позволяет достигать наибольшей активности фермента при накоплении ADP и АМР и снижать активность при накоплении АТР
Рис. 15-14. Фосфофруктокиназа-1 (PFK-1) и ее регуляция. а — ленточная модель фосфофруктокиназы-1 из Е. coli, с помощью которой показаны две из четырех идентичных субъединиц данного фермента (PDB ID 1PFK). Каждая субъединица имеет собственный активный центр, где ADP (синий) и фруктозо-1,6-бисфосфат (желтый) практически контактируют, а также свои центры связывания аллостерического регулятора ADP (синий), локализованные в зоне контакта субъединиц. б — зависимость активности фермента от концентрации субстрата демонстрирует наличие аллостерической регуляции мышечной PFK-1 под действием АТР. При низкой концентрации АТР К0,5 для фруктозо-6-фосфата имеет относительно низкое значение, поэтому при сравнительно низкой концентрации фруктозо-6-фосфата фермент работает с высокой скоростью. (В гл. 6 мы говорили о том, что константа К0,5, т. е. КМ, эквивалентна концентрации субстрата, при которой достигается половина максимальной активности фермента.) При высокой концентрации АТР К0,5 для фруктозо-6-фосфата резко возрастает, что видно из S-образной зависимости между концентрацией субстрата и активностью фермента. в — регуляторные факторы, влияющие на активность PFK-1.
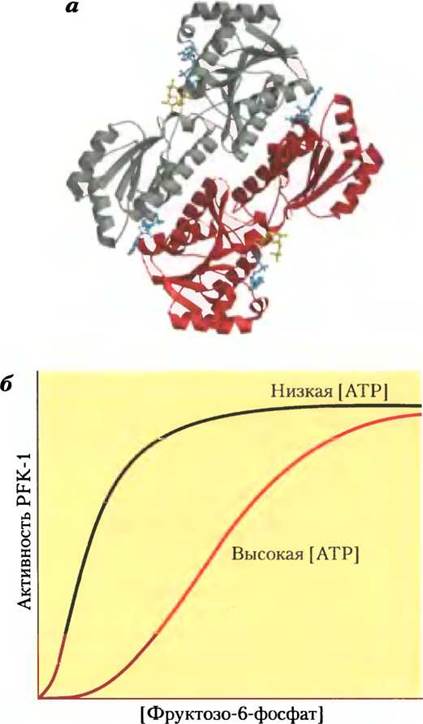
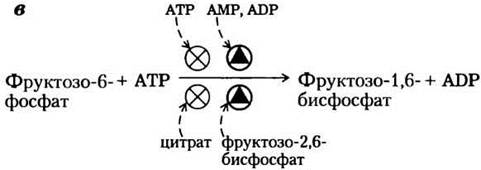
Цитрат (ионизованная форма лимонной кислоты) — ключевой интермедиат анаэробного окисления пирувата, жирных кислот и аминокислот; кроме того, он служит аллостерическим регулятором PFK-1. Высокая концентрация цитрата усиливает ингибирующее действие АТР, еще больше снижая интенсивность гликолиза. В данном случае, как и в некоторых других, которые мы обсудим позднее, цитрат служит внутриклеточным сигналом того, что клетка получает необходимое количество энергии путем окисления жиров и белков.
В процессе глюконеогенеза соответствующая стадия — превращение фруктозо-1,6-бис- фосфата в фруктозо-6-фосфат (рис. 15-15). Катализирующий эту реакцию фермент FBPa3a-l подвергается сильному ингибирующему действию со стороны АМР (аллостерическое ингибирование); при низком содержании АТР в клетке (что соответствует высокой концентрации АМР) замедляется синтез глюкозы, сопряженный с затратами АТР.
Рис. 15-15- Регуляция фруктозе-1,6-бисфосфатазы-1 (РВРазы-1) и фосфофруктокиназы-1 (РРК-1). Важная роль фруктозо-2,6-бисфосфата в регуляции этого субстратного цикла более подробно отражена далее на рисунках.
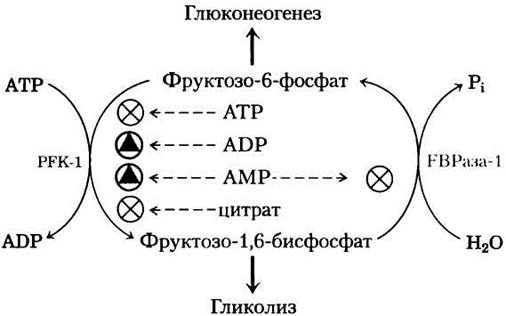
Таким образом, действующие в противоположном направлении ферменты гликолиза и глюконеогенеза (PFK-1 и FBPaзa-l) взаимно регулируются. Обычно при наличии достаточной концентрации ацетил-СоА или цитрата (образующегося при конденсации ацетил-СоА с оксалоацетатом) или тогда, когда значительная доля клеточного аденилата присутствует в форме АТР, преимущество получает процесс глюконеогенеза. При повышении уровня АМР происходит стимуляция PFK-1 и активация гликолиза (кроме того, как мы увидим в разд. 15.5, происходит стимуляция расщепления гликогена благодаря активации гликогенфосфорилазы).
Фруктозо-2,6-бисфосфат — мощный регулятор гликолиза и глюконеогенеза
Особая роль печени в поддержании постоянного уровня глюкозы крови требует наличия дополнительных регуляторных механизмов, управляющих синтезом и потреблением глюкозы. При снижении уровня глюкозы крови гормон глюкагон дает печени сигнал увеличить синтез и выделение глюкозы и прекратить использование ее для собственных нужд. Одним источником глюкозы служит запасенный в печени гликоген, другим — глюконеогенез, использующий в качестве исходного материала пируват, лактат, глицерин или некоторые аминокислоты. Когда концентрация глюкозы крови высокая, инсулин дает сигнал печени использовать глюкозу как топливо и как реагент для синтеза и запасания гликогена и триацилглицеринов.
Гормональная регуляция гликолиза и глюконеогенеза осуществляется при участии фруктозо-2,6-бисфосфата, который выступает в роли аллостерического эффектора ферментов PFK-1 и FBPaзы-1:
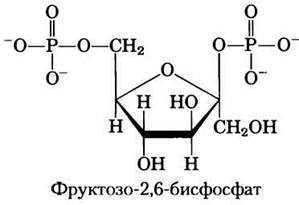
При связывании фруктозо-2,6-бисфосфата с участком аллостерической регуляции на молекуле РРК-1 происходит повышение сродства фермента к субстрату фруктозо-6-фосфату и снижение сродства к аллостерическим ингибиторам АТР и цитрату (рис. 15-16). При физиологических концентрациях субстратов (АТР и фруктозо-6-фосфата), а также других активаторов и ингибиторов (АТР, АМР, цитрата) в отсутствие фруктозо-2,6-бисфосфата фермент PFK-1 практически не проявляет активности. Фрук- тозо-2,6-бисфосфат активирует РРК-1 и стимулирует гликолиз в печени, а также ингибирует РВРазу-1, т. е. уменьшает ее аффинность к субстрату (рис. 15-16, в), ослабляя тем самым глюконеогенез.
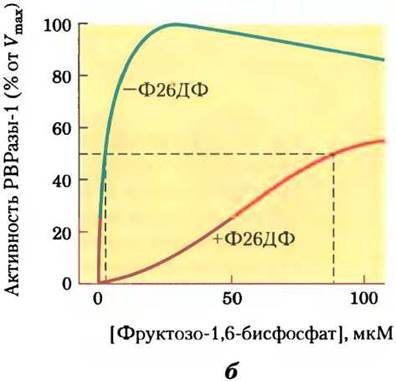
Рис. 15-16. Роль фруктозо-2,6-бисфосфата в регуляции гликолиза и глюконеогенеза. Фруктозо-2,6-бисфосфат (Ф26БФ) оказывает противоположное действие на активность гликолитического фермента фосфофруктокиназы-1 (РРК-1) и фермента глюконеогенеза фруктозо-1,б-дифосфатазы (РВРазы-1). а — без Ф26БФ (синяя кривая) активность РРК-1 достигает половины максимальной активности при концентрации фруктозо-6-фосфата 2 мМ (т. е. К0,5 - 2 мМ). В присутствии 0,13 мкМ Ф26БФ (красная кривая) К0,5 для фруктозо-6-фосфата составляет лишь 0,08 мМ. Таким образом, Ф26БФ активирует РРК-1 путем повышения ее сродства к субстрату (рис. 15-18). б — активность РВРазы-1 ингибируется уже в присутствии 1 мкМ Ф26ДФ, а значительное ингибирование наблюдается при концентрации 25 мкМ. В отсутствие ингибитора (синяя кривая) для фруктозо-1,6-бисфосфата К0,5 составляет 5 мМ, но в присутствии 25 мкМ Ф26ДФ (красная кривая) К0,5> 70 мМ. Фруктозо-2,6-бисфосфат, кроме того, повышает чувствительность РВРазы-1 к действию другого аллостерического ингибитора — АМР. в — суммарное влияние фруктозо-2,6-бисфосфата.
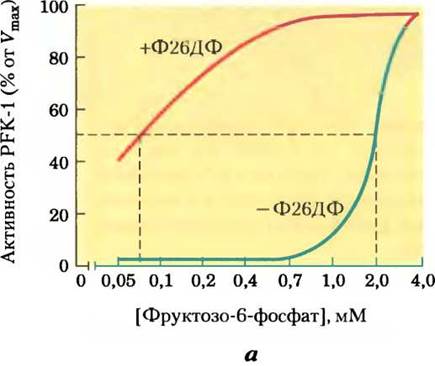
Концентрация фруктозо-2,6-бисфосфата в клетке определяется отношением скоростей его синтеза и распада (рис. 15-17, а); синтез происходит путем фосфорилирования фруктозо- 6-фосфата, катализируемого фосфофруктокиназой-2 (PFK-2), а распад — под действием фруктозо-2,6-бисфосфатазы (FBPaзы-2). Обратите внимание, что эти ферменты отличны от PFK-1 и FBPaзы-l, которые катализируют синтез и распад фруктозо-1,6-бисфосфата. Активностью PFK-2 и FBPaзы-2 обладает один и тот же бифункциональный белок. Соотношение между этими двумя активностями в печени, определяющее уровень фруктозо-2,6-бисфосфата в клетке, регулируется глюкагоном и инсулином (см. рис. 15-23, б).
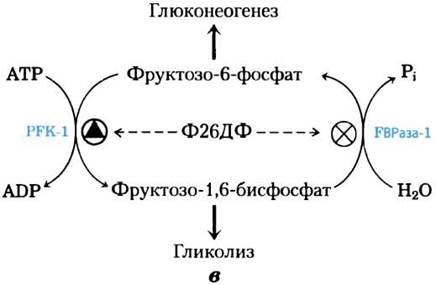
Рис. 15-17. Регуляция уровня фруктозо-2,6-бисфосфата. а — концентрация фруктозо- 2,6-бисфосфата (Ф26БФ) в клетке определяется скоростью его синтеза под действием фосфофруктокиназы-2 (РБК-2) и распада под действием фруктозо-2,6-бисфосфатазы (РВРазы-2). б — обе ферментативные активности принадлежат одному белку и подвержены согласованной регуляции инсулином и глюкагоном. Здесь и далее стрелками обозначено повышение (↑) и понижение (↓) уровня метаболита.
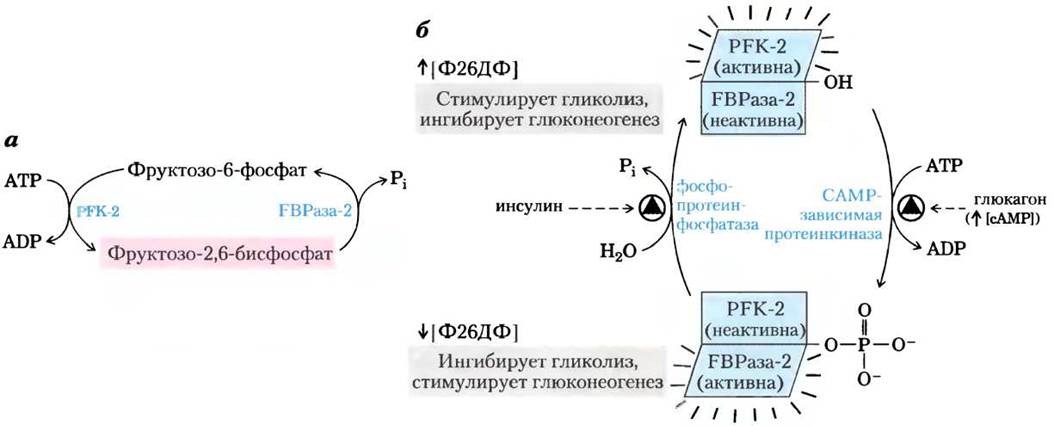
Как мы уже говорили в гл. 12, глюкагон стимулирует аденилатциклазу печени к синтезу 3',5'- циклического АМР (сАМР) из АТР. Затем сАМР активирует сАМР-зависимую протеинкиназу, которая переносит фосфорильную группу от АТР на бифункциональный белок PFK-2/FBPa3y-2. Фосфорилирование этого белка усиливает активность FBPaзы-2 и ингибирует активность PFK-2. Таким образом, глюкагон снижает уровень фруктозо-2,6-бисфосфата в клетке, ингибирует гликолиз и стимулирует глюконеогенез.
Увеличение синтеза глюкозы помогает поднять уровень глюкозы в крови в ответ на сигнал глюкагона. Инсулин оказывает противоположное действие, стимулируя активность фосфопротеин- фосфатазы, которая катализирует удаление фос- форильной группы от бифункционального белка с активностью РРК-2/РВРазы-2, что повышает активность РРК-2, поднимает уровень фруктозо- 2,6-бисфосфата, стимулирует гликолиз и ингибирует глюконеогенез.
Ксилулозо-5-фосфат — ключевой регулятор метаболизма углеводов и жиров
Еще один механизм регуляции также основан на контроле уровня фруктозо-2,6-бисфосфата. В печени млекопитающих продукт гексозомонофосфатного пути ксилулозо-5-фосфат (с. 109) способствует усилению гликолиза после приема богатой углеводами пищи. Концентрация ксилулозо-5- фосфата возрастает при превращении глюкозы, поступающей в печень, в глюкозо-6-фосфат и его вступлении на гликолитический или гексозомонофосфатный путь. Ксилулозо-5-фосфат активирует фосфопротеинфосфатазу РР2А (рис. 15-18), которая дефосфорилирует бифункциональный фермент с активностью РFК-2/FВРазы-2 (рис. 15-17).
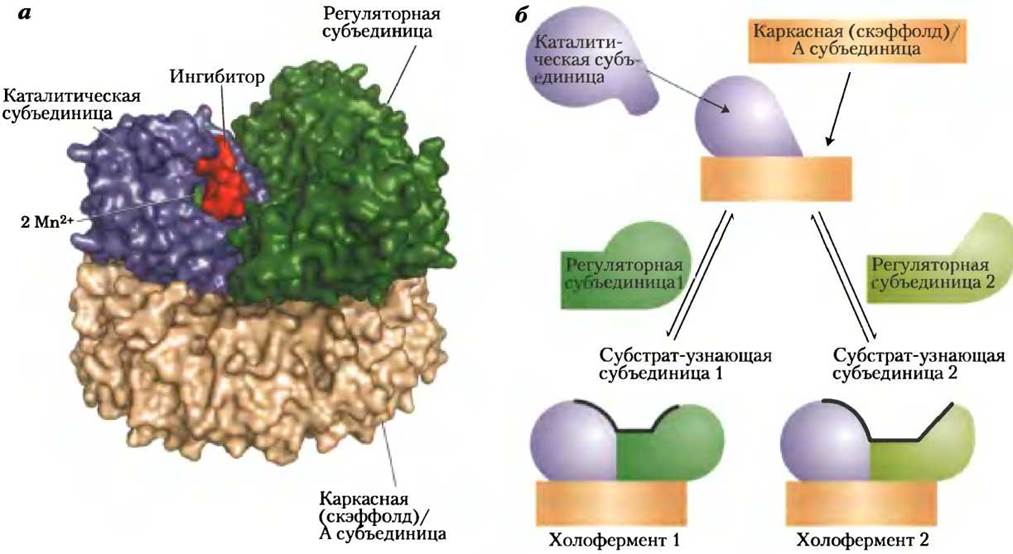
Рис. 15-18. Структура и механизм действия фосфопротеинфосфатазы 2А (РР2А). а — в активном центре каталитической субъединицы белка содержатся два иона Мn2+; активный центр расположен вблизи участка узнавания субстрата, находящегося на границе каталитической и регуляторной субъединиц (РDВ ID 2NРР). Микроцистин-LR(изображен красным цветом) — специфический ингибитор фермента. Каталитическая и регуляторная субъединицы соединены с каркасной (скэффолд-) субъединицей, которая позволяет им располагаться необходимым образом относительно друг друга и формировать участок узнавания субстрата. б — способность распознавать различные белки определяется вариабельной регуляторной субъединицей РР2А. Каждая регуляторная субъединица совместима с каркасной (скэффолд-) субъединицей и связанной на ней каталитической субъединицей, при этом каждая регуляторная субъединица создает свой уникальный субстратсвязывающий участок.
Дефосфорилирование активирует РЕК-2 и ингибирует FВРазу-2; увеличение в результате этого концентрация фруктозо-2,6-бисфосфата стимулирует гликолиз и ингибирует глюконеогенез. Усиление гликолиза способствует образованию ацетил-СоА, а увеличение потока гексозы по гексозомонофосфатному пути приводит к выработке NАDРН. Ацетил-СоА и NАDРН — исходные вещества для синтеза жирных кислот, концентрация которых, как известно, сильно повышается после употребления пищи с высоким содержанием углеводов. Ксилулазо-5-фосфат, кроме того, способствует синтезу всех ферментов, необходимых для образования жирных кислот; к этому механизму мы вернемся при обсуждении связи метаболизма углеводов и липидов (гл. 23).
Гликолитический фермент пируваткиназа подвержен аллостерическому ингибированию со стороны АТР
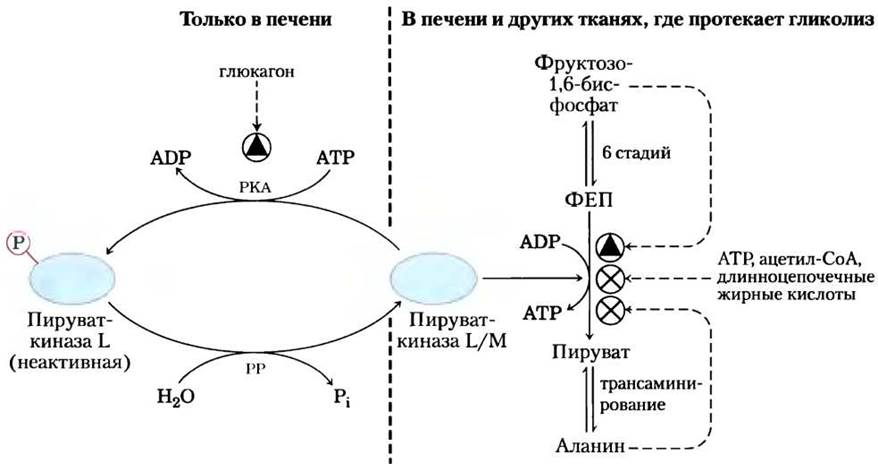
У позвоночных существуют как минимум три изоформы пируваткиназы, различающиеся тканевой локализацией и реакцией на действие модуляторов. Высокие концентрации АТР, ацетил-СоА и длинноцепочечных жирных кислот (что свидетельствует о достаточных энергетических запасах) ингибируют все изоферменты пируваткиназы (рис. 15-19). Изофермент из печени (L-форма), в отличие от М-формы из мышц, кроме того, регулируется фосфорилированием. Когда низкая концентрация глюкозы в крови приводит к появлению глюкагона, сАМР-зависимая протеинкиназа фосфорилирует L-форму пируваткиназы, тем самым инактивируя ее. Это тормозит расходование глюкозы в качестве топливной молекулы в печени, сохраняя ее для головного мозга и других органов. Повышение концентрации сАМР в мышцах оказывает совсем другое действие. В ответ на сигнал адреналина сАМР активирует распад гликогена и гликолиз, обеспечивая энергию, необходимую для реакции «борьбы или бегства».
Рис. 15-19. Регуляция пируваткиназы. Аллостерическими ингибиторами фермента являются АТР, ацетил-СоА и длинноцепочечные жирные кислоты (их наличие указывает на избыток энергии в клетке), а накопление фруктозо-1,6-бисфосфата способствует активации фермента. Аланин, который может синтезироваться из пирувата в одну стадию, выступает аллостерическим ингибитором пируваткиназы и замедляет образование пирувата в процессе гликолиза. Изофермент из печени (L-форма), кроме того, подвергается гормональной регуляции; глюкагон активирует сАМР-зависимую протеинкиназу (РКА; см. рис. 15-35), которая фосфорилирует L-форму пируваткиназы, инактивируя ее. При снижении уровня глюкагона протеинфосфатаза (РР) дефосфорилирует пируваткиназу, активируя ее. Этот механизм противодействует расходованию глюкозы в печени в процессе гликолиза при низкой концентрации глюкозы в крови; вместо этого глюкоза из печени попадает в кровь. Мышечная форма фермента (М-форма) не подвержена регуляции фосфорилированием.
Превращение пирувата в фосфоенолпируват в процессе гликолиза регулируется несколькими способами
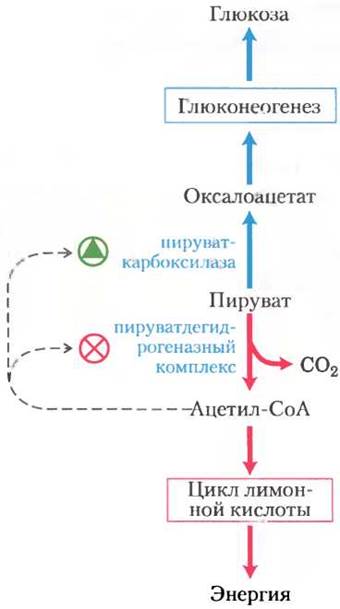
На пути превращения пирувата в глюкозу первый «контрольный пункт» определяет судьбу пирувата в митохондриях. Пируват может превратиться либо в ацетил-СоА (с помощью пируватдегидрогеназного комплекса; гл. 16) для использования в качестве источника энергии в цикле лимонной кислоты, либо в оксалоацетат (с помощью пируваткарбоксилазы) для запуска глюконеогенеза (рис. 15-20). В тех случаях, когда жирные кислоты легко доступны и могут использоваться в качестве источника энергии, их распад в митохондриях клеток печени приводит к образованию ацетил-СоА, что говорит об отсутствии необходимости окисления глюкозы с целью получения энергии. Ацетил-СоА служит аллостерическим активатором пируваткарбоксилазы и ингибитором пируватдегидрогеназы, поскольку стимулирует протеинкиназу, ингибирующую активность дегидрогеназы. В тех случаях, когда у клетки возникает необходимость в дополнительной энергии, окислительное фосфорилирование замедляется, концентрация NADHначинает превышать концентрацию NAD+, что ингибирует цикл лимонной кислоты, и накапливается ацетил-СоА. Увеличение концентрации ацетил-СоА ингибирует пируватдегидрогеназный комплекс, снижая скорость превращения пирувата в ацетил-СоА, и стимулирует глюконеогенез путем активации пируваткарбоксилазы, способствуя превращению избытка пирувата в оксалоацетат (а в итоге — в глюкозу).
Рис. 15-20. Два возможных пути превращения пирувата. Пируват может превратиться в глюкозу и гликоген в процессе глюконеогенеза или окислиться до ацетил-СоА для получения энергии. Первый фермент на каждом из этих путей подвержен аллостерической регуляции; ацетил- СоА, образующийся в результате окисления жирных кислот или под действием пируватдегидрогеназного комплекса, стимулирует пируваткарбоксилазу и ингибирует пируватдегидрогеназу.
Образующийся оксалоацетат превращается в фосфоенолпируват (ФЕП) в реакции, катализируемой ФЕП-карбоксикиназой (рис. 15-11). У млекопитающих регуляция этого важного фермента осуществляется главным образом на уровне его синтеза и распада в ответ на пищевые и гормональные сигналы. Голодание или высокая концентрация глюкагона, действуя через сАМР, повышают скорость транскрипции и стабилизируют мРНК фермента. Инсулин или высокий уровень глюкозы в крови оказывают противоположное действие. Ниже мы более подробно рассмотрим данный механизм. Эти изменения обычно запускаются внешними сигналами (пища, гормоны) и происходят во временном интервале от нескольких минут до нескольких часов.
Регуляция гликолиза и глюконеогенеза на уровне транскрипции изменяет количество фермента (число его молекул)
Большинство процессов регуляции, которые обсуждались до сих пор, осуществляются с помощью быстрых и легко обратимых механизмов: аллостерическое действие, ковалентная модификация фермента (фосфорилирование) или связывание регуляторного белка. Еще одна группа процессов регуляции основана на изменении количества фермента в клетке путем сдвига равновесия между синтезом и распадом его молекул. Далее мы рассмотрим регуляцию транскрипции при участии активируемых сигналом транскрипционных факторов.
В гл. 12 мы говорили о ядерных рецепторах и факторах транскрипции в связи с передачей сигнала инсулина. Инсулин действует через свой рецептор в плазматической мембране, включая как минимум два разных сигнальных пути, каждый сопряжен с активацией протеинкина- зы. Например, митогенактивированная киназа ERK фосфорилирует факторы транскрипции SRF и Elk1 (см. рис. 12-15), которые затем стимулируют синтез ферментов, необходимых для роста и деления клеток. Протеинкиназа В (также известная как Akt) фосфорилирует другой набор транскрипционных факторов (например, PDX1), что стимулирует синтез ферментов, ответственных за метаболизм углеводов и жиров, которые образуются и запасаются в организме при избыточном потреблении углеводов. В β-клетках поджелудочной железы PDX1 также стимулирует синтез инсулина.
На уровне транскрипции инсулин осуществляет регуляцию более 150 генов; у человека существует не менее семи основных типов инсулинреспонсивных элементов, каждый узнается группой факторов транскрипции, активируемых инсулином в различных условиях. Инсулин стимулирует транскрипцию генов, кодирующих гексокиназы II и IV, PFK-1, пируваткиназу и PFK-2/FBPaзy-2 (все эти ферменты участвуют в гликолизе и его регуляции), некоторые ферменты синтеза жирных кислот, глюкозо-6-фосфатдегидрогеназу и 6-фосфоглюконатдегидрогеназу, а также ферменты пентозофосфатного пути, генерирующего NADPH для синтеза жирных кислот. Кроме того, инсулин замедляет экспрессию генов двух ферментов глюконеогенеза — ФЕП-карбоксикиназы и глюкозо-6-фосфатазы (табл. 15-5).
Таблица 15-5. Некоторые гены, которые регулируются инсулином
Изменение генной экспрессии |
Метаболический путь |
Увеличение экспрессии |
|
Гексокиназа II |
Гликолиз |
Гексокиназа IV |
Гликолиз |
Фосфофруктокиназа-1 (РРК-1) |
Гликолиз |
Пируваткиназа |
Гликолиз |
РРК-2/ТВРаза-2 |
Регуляция гликолиза / глюконеогенез |
Глюкозо-6-фосфатдегидрогеназа |
Пентозофосфатный путь (NADPH) |
6-Фосфоглюконатдегидрогеназа |
Пентозофосфатный путь (NADPH) |
Пируватдегидрогеназа |
Синтез жирных кислот |
Ацетил- СоА-карбоксилаза |
Синтез жирных кислот |
Малат-фермент |
Синтез жирных кислот (NADPH) |
АТР-цитратлиаза |
Синтез жирных кислот (предоставляет ацетил-СоА) |
Комплекс синтазы жирных кислот |
Синтез жирных кислот |
Стеароил- Со А-дегидрогеназа |
Десатурация жирных кислот |
Ацил- СоА-глицеринтрансфераза |
Синтез триацилглицеринов |
Уменьшение экспрессии |
|
ФЕП-карбоксикиназа |
Глюконеогенез |
Глюкозо-6-фосфатаза (каталитическая субъединица) |
Высвобождение глюкозы в кровь |
Важную роль в метаболизме углеводов играет фактор транскрипции ChREBP (carbohydrate response element binding protein; рис. 15-21), экспрессирующийся в основном в печени, жировой ткани и почках. Он служит для координации синтеза ферментов, необходимых для образования углеводов и жиров. В неактивном состоянии
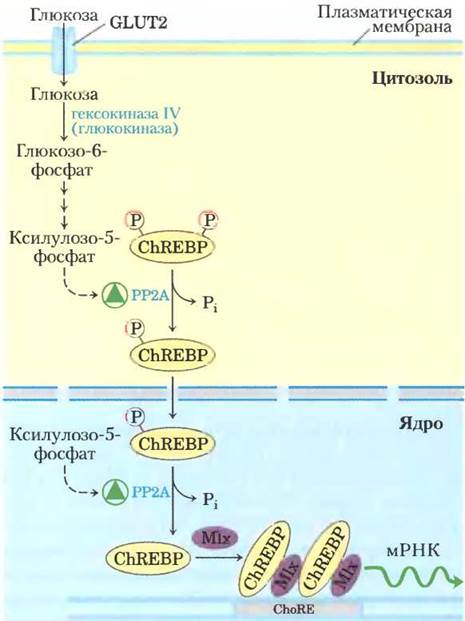
белок ChREBP фосфорилирован и локализован в цитозоле. После того как фосфопротеинфосфатаза 2А (РР2А; рис. 15-18) отщепляет от него фосфорильную группу, фактор транскрипции становится способным проникать в ядро. Здесь ядерная РР2А удаляет следующую фосфорильную группу, и ChREBP связывается с белком Mlx. Этот комплекс запускает синтез нескольких ферментов: пируваткиназы, синтазы жирных кислот, а также ацетил-СоА-карбоксилазы — первого фермента на пути синтеза жирных кислот (рис. 15-21).
Рис. 15-21. Механизм регуляции генов под действием фактора транскрипции ChREBP. Находящийся в цитозоле гепатоцитов белок ChREBP фосфорилирован по остаткам Ser и Thr и не может проникать в ядро. Удаление фосфорилъной группы остатка серина под действием фосфопротеинфосфатазы-2А позволяет белку войти в ядро, где происходит удаление фосфорилъной группы остатка треонина. Активированный таким образом ChREBP связывается с белком-партнером Mix. Далее комплекс ChREBP-Mlx связывается с углеводчувствительным элементом ChoRE в промоторе и стимулирует транскрипцию. Аллостерическую активацию РР2А осуществляет ксилулозо-5-фосфат, образующийся в качестве интермедиата пентозофосфатного пути.
Контроль активности РР2А (и, следовательно, регуляцию синтеза группы метаболических ферментов) осуществляет ксилулозо-5-фосфат — интермедиат не гликолиза или глюконеогенеза, а пентозофосфатного пути. При высокой концентрации в крови глюкоза поступает в печень и фосфорилируется под действием гексокиназы IV. Образующийся при этом глюкозо-6- фосфат может использоваться в гликолизе или в пентозофосфатном пути. В последнем случае в результате двух окислительных реакций сначала образуется ксилулозо-5-фосфат, появление которого свидетельствует о том, что использующие глюкозу пути в достаточной степени обеспечены субстратом. Передача сигнала осуществляется путем аллостерической активации РР2А, которая затем дефосфорилирует ChREBP, позволяя ему включить экспрессию генов ферментов гликолиза и синтеза жиров (рис. 15-21). В результате гликолиза получается пируват, а образующийся из пирувата ацетил-СоА служит исходным материалом для синтеза жирных кислот; ацетил-СоА- карбоксилаза превращает ацетил-СоА в малонил- СоА — первый специфический интермедиат на пути синтеза жирных кислот. Синтаза жирных кислот образует жирные кислоты для жировой ткани и для запасания в виде триацилглицеринов (гл. 21). Таким образом, избыток углеводов из пищи запасается в виде жира.
Другой фактор транскрипции в печени SREBP-1c (sterol response element binding proteins; см. рис. 21-43) включает синтез пируваткиназы, гексокиназы IV, липопротеинлипазы, ацетил- СоА-карбоксилазы, а также комплекса синтазы жирных кислот, превращающего ацетил-СоА (образуется из пирувата) в жирные кислоты для запасания в адипоцитах. Инсулин стимулирует синтез SREBP-1c, а глюкагон его подавляет. Кроме того, SREBP-1c подавляет экспрессию некоторых ферментов глюконеогенеза: глюкозо-6- фосфатазы, ФЕП-карбоксикиназы и FBPaps-1.
Фактор транскрипции CREB (cyclic АМР response element binding protein) включает синтез глюкозо-6-фосфатазы и ФЕП-карбоксикиназы в ответ на повышение концентрации сАМР, вызванное глюкагоном. Напротив, стимулированная инсулином инактивация других факторов транскрипции выключает синтез нескольких ферментов глюконеогенеза в печени: ФЕП-карбоксикиназы, фруктозо-1,6-бисфосфатазы, переносчика глю- козо-6-фосфата в эндоплазматическом ретикулуме, а также глюкозо-6-фосфатазы. Например, FOXO1 (forkhead box other) стимулирует синтез ферментов глюконеогенеза и подавляет синтез ферментов гликолиза, пентозофосфатного пути и синтеза триацилглицеринов (рис. 15-22).
Рис. 15-22. Механизм регуляции экспрессии генов при участии фактора транскрипции FОХО1. Инсулин запускает изображенный на рис. 12-16 сигнальный каскад, активируя при этом протеинкиназу В. Находящийся в цитозоле фактор транскрипции FОХО1 фосфорилируется протеин- киназой В и связывается с убиквитином для последующего распада в протеасоме. Оставшийся нефосфорилированным или дефосфорилированный фактор FОХО1 может проникать в ядро, связываться с респонсивным элементом и запускать транскрипцию соответствующих генов. Таким образом, инсулин обладает способностью выключать экспрессию генов ферментов, таких как ФЕП-карбоксикиназа и глюкозо-6-фосфатаза.
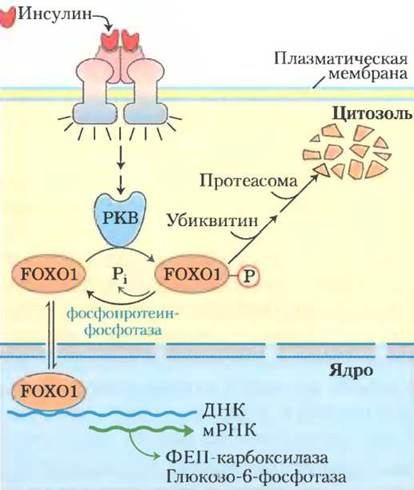
В нефосфорилированной форме FOХO1 действует как ядерный фактор транскрипции. В ответ на сигнал инсулина FOХO1 выходит из ядра в цитозоль, где фосфорилируется под действием протеинкиназы В и связывается с убиквитином, а затем расщепляется в протеасоме. Глюкагон предотвращает фосфорилирование под действием протеинкиназы В, в результате чего FOХO1 остается в активной форме в ядре.
Как мы видим, процесс регуляции генов ферментов, ответственных за метаболизм углеводов и жиров, достаточно сложный, причем в реальности он еще сложнее и гораздо тоньше, чем мы тут показали. Многие факторы транскрипции могут действовать на один и тот же промотор, многие протеинкиназы и фосфатазы могут активировать или инактивировать эти факторы транскрипции, кроме того, действие факторов транскрипции модулируется различными вспомогательными бел
ками. Рассмотрим в качестве примера ген ФЕП- карбоксикиназы, регуляция которого на уровне транскрипции достаточно хорошо изучена. В области промотора этого гена (рис. 15-23) обнаружено не менее 15 респонсивных элементов, распознаваемых 12 известных факторов транскрипции, причем вполне вероятно, что со временем обнаружатся и другие факторы транскрипции. Факторы транскрипции действуют на эту промоторную область и на сотни других промоторов, осуществляя тонкую регуляцию экспрессии сотен метаболических ферментов и координируя их активность в метаболизме углеводов и жиров. Важнейшая роль факторов транскрипции в регуляции метаболизма отчетливо видна при наличии мутаций соответствующих генов. Например, у молодых людей не менее пяти различных вариантов сахарного диабета взрослого типа (МODY) связано с мутациями специфических факторов транскрипции (доп. 15-3).
Рис. 15-23. Сложный механизм регуляции экспрессии генов на примере регуляции ФЕП-карбоксикиназы. Изображены факторы транскрипции (в виде пиктограмм, размер которых связан с последовательностью ДНК), регулирующие транскрипцию гена ФЕП-карбоксикиназы. Степень экспрессии гена зависит от совместного влияния всех факторов: доступность питательных веществ, уровень глюкозы в крови и другие параметры, определяющие потребность клетки в этом ферменте в данный момент времени. P1, Р2, P3I, Р3II и Р4 — участки связывания белка, идентифицированные методом футпринтинга с использованием ДНКазы I (см. доп. 26-1). Мотив ТАТА является местом сборки комплекса транскрипции РНК- полимеразы П (Pol II).
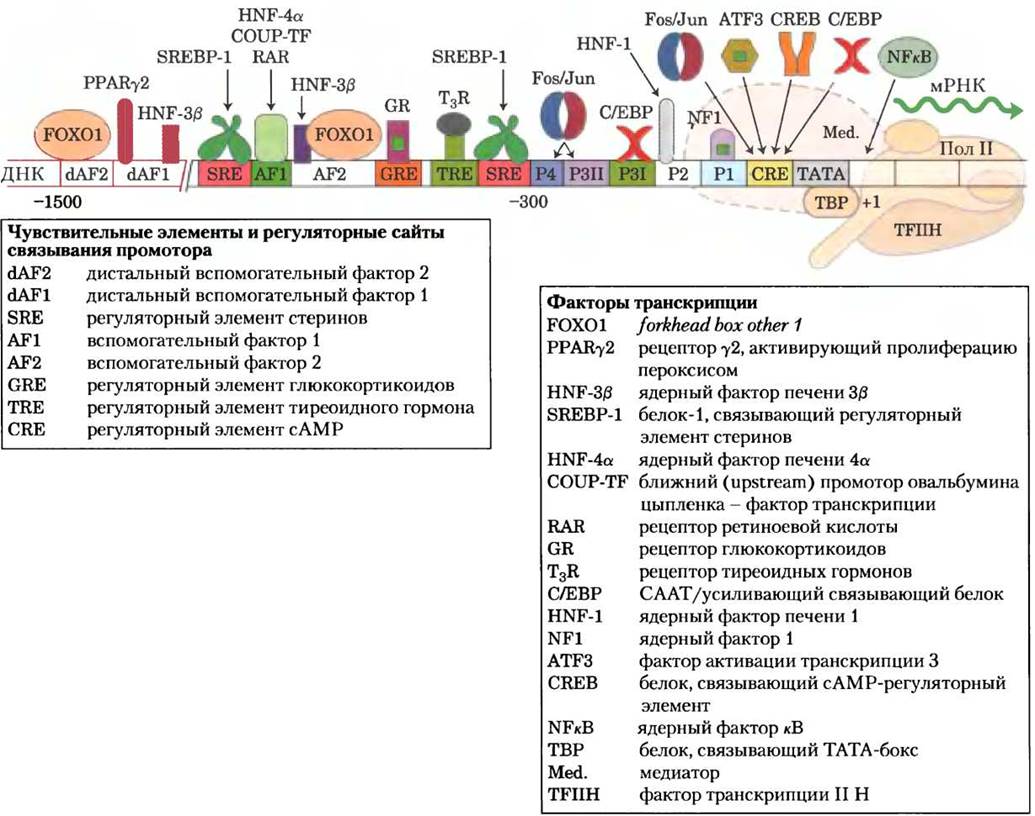
Дополнение 15-3. МЕДИЦИНА. Мутации, приводящие к возникновению редких форм сахарного диабета
Термин «диабет» охватывает целый ряд клинических состояний, общий признак которых — избыточное образование мочи. В доп. 11-2 мы рассмотрели такую форму заболевания, как несахарный диабет, при котором нарушение всасывания воды в почках вызывается мутацией гена аквапорина. Термин «сахарный диабет» относится к той форме заболевания, при которой нарушается метаболизм глюкозы — либо из-за неспособности поджелудочной железы продуцировать инсулин, либо по причине нечувствительности тканей к сигналу инсулина.
Выделяют две основные формы сахарного диабета. Причиной диабета I типа, также называемого инсулинозависимым сахарным диабетом (ИЗСД), является иммунная реакция организма, направленная против собственных β-клеток поджелудочной железы, производящих инсулин. Для компенсации недостаточной активности β-клеток больные с такой формой диабета должны получать инсулин в виде инъекций или ингаляций. Сахарный диабет I типа проявляется в раннем детстве и в подростковом возрасте, поэтому раньше эту форму заболевания называли юношеским диабетом. Диабет II типа, иначе называемый инсулинонезависимым сахарным диабетом (ИНЗСД), обычно возникает у людей старше 40 лет. Эта форма диабета встречается чаще, чем диабет I типа, и вероятность ее выше у людей с избыточной массой тела. В мире очень много людей с ожирением различной степени, что обусловило широкое распространение ИНЗСД и объясняет острую необходимость изучения связи между ожирением и этой формой заболевания на генетическом и биохимическом уровне. В последующих главах мы более подробно рассмотрим вопросы, связанные с метаболизмом жиров и белков, и в гл. 23 вернемся к обсуждению проблемы диабета, при котором происходят серьезные изменения метаболизма углеводов, жиров и белков.
Здесь мы рассмотрим другой вариант диабета, при котором нарушается метаболизм углеводов и жиров, — диабет взрослого типа у молодых (MODY), при котором происходит мутация гена фактора транскрипции, играющего важную роль в проведении сигнала инсулина в ядро, или фермента, участвующего в формировании ответа на сигнал инсулина. Например, при диабете MODY2 мутирован ген гексокиназы IV (глюкокиназы) в печени и поджелудочной железе, где преобладает именно эта изоформа фермента. Глюкокиназа β-клеток поджелудочной железы действует в качестве сенсора на глюкозу. В норме при повышении концентрации глюкозы в крови повышается также уровень глюкозы в β-клетках, а поскольку глюкокиназа имеет сравнительно высокую величину Км для глюкозы, ее активность возрастает с увеличением концентрации глюкозы. Метаболизм образующегося в этой реакции глюкозо-6-фосфата приводит к повышению уровня АТР в β-клетках, а это в свою очередь инициирует высвобождение инсулина по механизму, изображенному на рис. 23-28. У здорового человека выброс инсулина происходит при концентрации глюкозы в крови около 5 мМ. Однако у человека с инактивирующей мутацией в обеих копиях гена глюкокиназы пороговое значение концентрации глюкозы, при котором происходит выброс инсулина, очень высокое, и поэтому с самого рождения у них наблюдается тяжелая форма гипергликемии — так называемый перманентный неонатальный диабет. У человека с одной мутированной и одной нормальной копией гена глюкокиназы выброс инсулина происходит при концентрации глюкозы около 7 мМ. Если у больного уровень глюкозы в крови лишь немного превышает норму, наблюдается умеренная гипергликемия без симптомов заболевания. Такое состояние обычно выявляют случайно по результатам анализа крови.
Кроме того, известно не менее пяти других форм диабета MODY, каждая связана с инактивирующей мутацией того или иного фактора транскрипции, необходимого для нормального развития и функционирования β-клеток поджелудочной железы. У человека с такими мутациями в разной степени снижена продукция инсулина и нарушен гомеостаз глюкозы в крови. В вариантах MODY1 и MODY3 нарушения достаточно серьезные, чтобы вызвать осложнения, сопровождающие ИЗСД и ИНЗСД: проблемы в сердечно-сосудистой системе, почечную недостаточность и слепоту. Формы диабета MODY4, 5 и 6 менее тяжелые. Формы диабета MODY — лишь небольшая часть всех патологических состояний при ИНЗСД. Кроме того, очень редко встречаются люди с мутацией самого гена инсулина; у них наблюдается нарушение проведения инсулинового сигнала разной степени тяжести.
Краткое содержание раздела 15.3 Согласованная регуляция гликолиза и глюконеогенеза
■ Глюконеогенез и гликолиз имеют семь общих ферментов, катализирующих легко обратимые реакции этих двух метаболических путей. На трех других стадиях прямые и обратные реакции катализируются разными ферментами, и именно на этих стадиях осуществляется регуляция двух путей.
■ Кинетические свойства гексокиназы IV (глюкокиназы) связаны с ее особой ролью в печени: она высвобождает глюкозу в кровь при низком уровне глюкозы крови и связывает и метаболизирует глюкозу, когда ее в крови много.
■ Аллостерические ингибиторы PFK-1 — АТР и цитрат. В большинстве тканей млекопитающих, в том числе и в печени, аллостерическим активатором PFK-1 выступает фруктозо-2,6-бисфосфат.
■ Аллостерический ингибитор пируваткиназы — АТР, а изофермент из печени ингибируется в результате сАМР-зависимого фосфорилирования.
■ Регуляция глюконеогенеза осуществляется на уровне пируваткарбоксилазы (активируемой ацетил-СоА) и FBPaзы-1(ингибируемой фруктозо-2,6-бисфосфатом и АМР).
■ Для ограничения интенсивности субстратного цикла между гликолизом и глюконеогенезом эти два метаболических пути находятся под согласованным аллостерическим контролем, который главным образом осуществляется путем противоположного действия, оказываемого фруктозо-2,6-бисфосфатом на PFK-1 и FBPaзу-1.
■ Глюкагон и адреналин снижают концентрацию фруктозо-2,6-бисфосфата. Это действие гормонов достигается посредством повышения концентрации сАМР и фосфорилирования бифункционального фермента, осуществляющего синтез и расщепления фруктозо-2,6-бисфосфата. Фосфорилирование инактивирует PFK-2 и активирует FBPaзу3y-2, что приводит к распаду фруктозо-2,6- фосфата. Инсулин повышает концентрацию фруктозо-2,6-бисфосфата путем активации фосфопротеинфосфатазы, которая дефосфорилирует (и при этом активирует) PFK-2.
■ Ксилулозо-5-фосфат — интермедиат пентозофосфатного пути; он активирует фосфопротеинфосфатазу 2А, которая дефосфорилирует несколько белков, включая PFK-2/FBPa3y-2, сдвигая равновесие в сторону захвата глюкозы, синтеза гликогена и синтеза липидов в печени.
■ Факторы транскрипции, в том числе ChREBP, CREB, SREBP и FOXOl, регулируют экспрессию в ядре специфических генов, кодирующих ферменты гликолиза и глюконеогенеза. Инсулин и глюкагон действуют как антагонисты, активируя эти факторы транскрипции и тем самым включая и выключая экспрессию многих генов.