ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ - 2014
ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
17. КАТАБОЛИЗМ ЖИРНЫХ КИСЛОТ
17.3. Кетоновые тела
У людей и большинства других млекопитающих ацетил-СоА, образующийся в печени в процессе окисления жирных кислот, может либо поступить в цикл трикарбоновых кислот (стадия 2 на рис. 17-7), либо превратиться в «кетоновые тела», ацетон, ацетоацетат и D-β- гидроксибутират для экспорта в другие ткани. (Термин «тела» является историческим; изредка его используют в отношении нерастворимых частиц, однако данные соединения полностью растворимы в крови и моче.) Ацетон, образующийся в меньших количествах, чем остальные кетоновые тела, испаряется. Ацетоацетат и D-β-гидроксибутират переносятся кровью к тканям, везде, кроме печени, и в тканях они превращаются в ацетил-СоА и окисляются в цикле трикарбоновых кислот. Кетоновые тела дают энергию таким тканям, как скелетные и сердечная мышцы, корковое вещество почек. Мозг, который в качестве источника энергии использует преимущественно глюкозу, в условиях голодания может приспособиться к употреблению ацетоацетата или D-β-гидроксибутирата. Образование и экспорт кетоновых тел из печени во внепеченочные ткани позволяет жирным кислотам непрерывно окисляться в печени, если ацетил-СоА не окисляется в цикле трикарбоновых кислот.
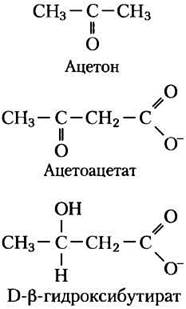
Кетоновые тела, образующиеся в печени, экспортируются в другие органы в качестве источников энергии
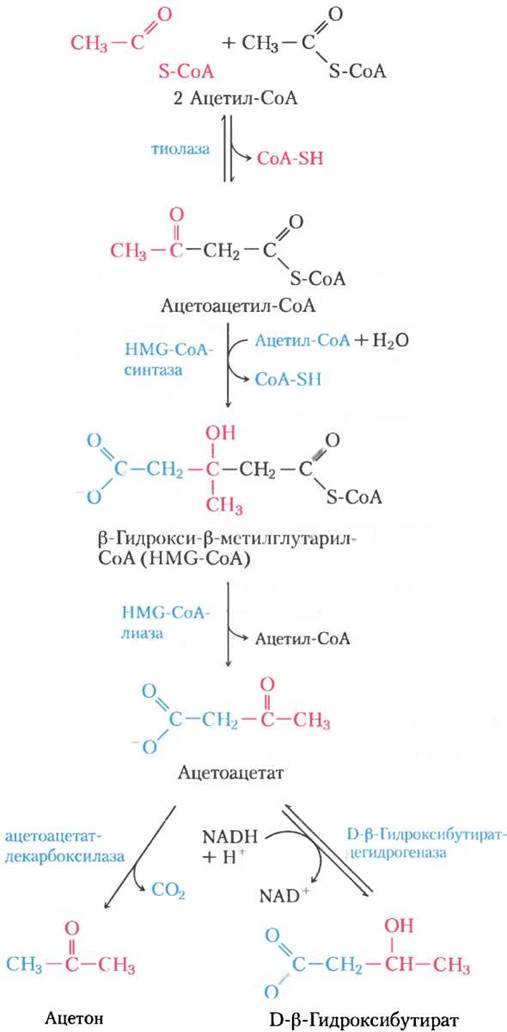
Первая стадия образования ацетоацетата происходит в печени (рис. 17-18) и заключается в ферментативной конденсации двух молекул ацетил- СоА, которую катализирует тиолаза; это просто обращение последнего шага β-окисления. Затем ацетоацетил-СоА конденсируется с ацетил- СоА, образуя β-гидрокси-β-метилглутарил-СоА (НМG-СоА, от англ. β-hydrоху-β-methylglutaryl- СоА), который распадается на свободный ацетоацетат и ацетил-СоА. Ацетоацетат обратимо восстанавливается митохондриальным ферментом D-β-гидроксибутиратдегидрогеназой до D-β-гидроксибутирата. Этот фермент специфичен к D-стереоизомеру; он не действует на L-β-гидроксиацил-СоА, и его не надо путать с L-β-гидроксиацил-СоА-дегидрогеназой β-окислительного пути.
Рис. 17-18. Образование кетоновых тел из ацетил-СоА. У здоровых нормально питающихся людей кетоновые тела образуются в незначительном количестве. При накоплении ацетил-СоА (например, при голодании или нелеченом диабете) тиолаза катализирует конденсацию двух молекул ацетил-СоА в ацетоацетил-СоА, исходное соединение для трех кетоновых тел. Реакции образования кетоновых тел происходят в матриксе митохондрий печени. Шестиуглеродное соединение β-гидрокси-β-метилглутарил-СоА (НМG-СоА) выступает также промежуточным соединением биосинтеза стеринов, однако на том пути фермент, образующий НМG-СоА, находится в цитозоле. НМG-СоА-лиаза есть только в митохондриальном матриксе.
У здорового человека из ацетоацетата в очень малых количествах образуется ацетон, который легко декарбоксилируется — либо спонтанно, либо под действием ацетоацетатдекарбоксилазы (рис. 17-18). Поскольку при нелеченом диабете образуется много ацетоацетата, в крови наблюдается высокое содержание токсичного ацетона. Ацетон летуч и придает дыханию характерный запах, что иногда помогает при диагностике диабета. ■
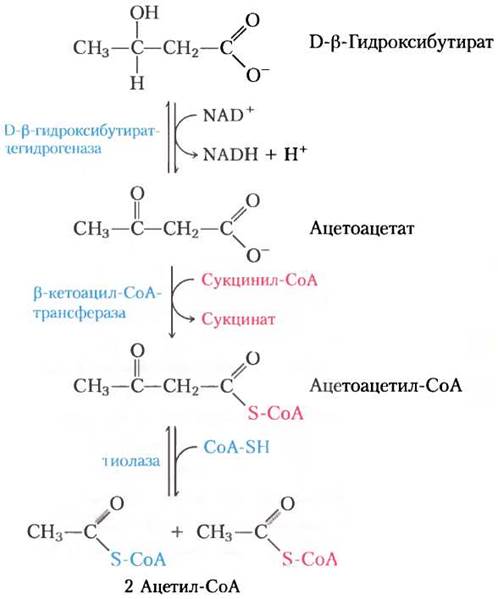
Во внепеченочных тканях D-β-гидрокси- бутиратдегидрогеназа окисляет D-β-гидроксибутират до ацетоацетата (рис. 17-19). Ацетоацетат активируется в реакции, катализируемой β-кетоацил-СоА-трансферазой. При переносе СоА с сукцинил-СоА, промежуточного соединения цикла трикарбоновых кислот (см. рис. 16-7), образуется сложный эфир кофермента А. Затем ацетоацетил-СоА распадается под действием тиолазы на две молекулы ацетил-СоА, которые поступают в цикл трикарбоновых кислот. Таким образом, кетоновые тела используются в качестве источника энергии во всех тканях, за исключением печени, в которой отсутствует тиолаза. Поэтому печень производит кетоновые тела для других тканей, но сама их не использует.
Рис. 17-19. D-β-Гидроксибутират в качестве источника энергии. D-β-Гидроксибутират, синтезируемый в печени, попадает в кровь и, таким образом, в другие ткани, где он превращается в три стадии в ацетил-СоА. Вначале он окисляется до ацетоацетата, который активируется коферментом А, полученным из сукцинил-СоА, а затем расщепляется тиолазой. Образовавшийся таким образом ацетил-СоА используется для получения энергии.
Образование и экспорт кетоновых тел печенью позволяет жирным кислотам непрерывно окисляться с минимальным окислением ацетил- СоА. Например, если промежуточные соединения цикла трикарбоновых кислот перекачиваются для синтеза глюкозы в процессе глюконеогенеза, окисление интермедиатов цикла притормаживается — а, следовательно, и окисление ацетил-СоА. Более того, печень содержит всего лишь ограниченные количества кофермента А, и если большая часть его связана в ацетил-СоА, β-окисление замедляется из-за нехватки свободного кофермента. Образование и экспорт кетоновых тел высвобождает кофермент А, делая окисление жирных кислот непрерывным.
При диабете и голодании кетоновые тела образуются сверх нужного количества
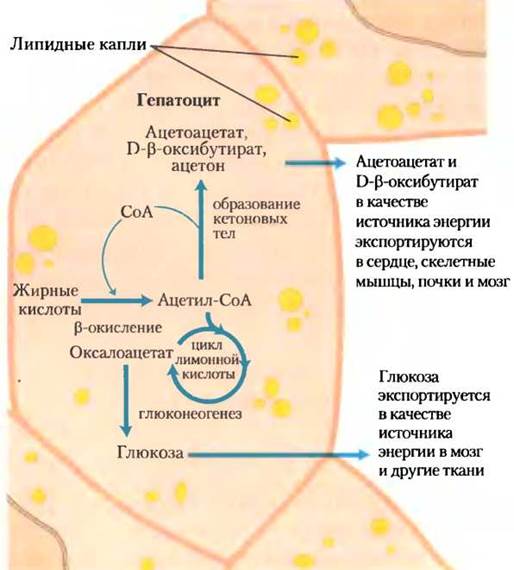
Голодание и нелеченые диабеты приводят к перепроизводству кетоновых тел, а вместе с этим и к некоторым медицинским проблемам. Во время голодания из-за глюконеогенеза количество промежуточных соединений цикла трикарбоновых кислот резко уменьшается, направляя ацетил-СоА в сторону образования кетоновых тел (рис. 17-20). При нелеченом диабете, когда содержание инсулина недостаточно, внепеченочные ткани не могут эффективно всасывать глюкозу из крови, как для получения энергии, так и для превращения ее в жиры. В этих условиях содержание малонил-СоА (стартовое вещество для синтеза жирных кислот) падает, ингибирование карнитинацилтрансферазы I ослабляется и жирные кислоты проникают в митохондрии для распада до ацетил-СоА, который, однако, не может пройти через цикл трикарбоновых кислот, поскольку промежуточные соединения цикла были переключены на использование в качестве субстратов в глюконеогенезе. В итоге накопление ацетил-СоА ускоряет образование кетоновых тел в таком количестве, которое превышает способность внепеченочных тканей окислить их. Повышенные уровни ацетоацетата и Б-р-гидроксибутирата в крови уменьшают ее pH, вызывая состояние, известное как ацидоз. В предельных случаях ацидоз может привести к коме, а в некоторых случаях — к смерти. Содержание кетоновых тел в крови и моче диабетиков может быть очень высоким — концентрация в крови 90 мг/100 мл (норма <3 мг/100мл), а в утренней моче 5000 мг/24 ч (норма ≤125 мг/24 ч). Такое состояние называется кетозом.
Рис. 17-20. Образование кетоновых тел и их экспорт из печени. Условия, способствующие глюконеогенезу (нелеченый диабет, чрезвычайно низкое потребление пищи) замедляют работу цикла трикарбоновых кислот (благодаря отведению оксалоацетата) и увеличивают превращение ацетил-СоА в ацетоацетат. Высвобождаемый кофермент А благоприятствует непрерывному β-окислению жирных кислот.
При очень низкокалорийной диете в качестве основного источника энергии используются жиры, запасенные в жировой ткани, у таких людей также повышено содержание кетоновых тел в крови и моче. Чтобы избежать опасности ацидоза и кетоза (кетоацидоза), надо следить за этими показателями. ■
Краткое содержание раздела 17.3 Кетоновые тела
■ Кетоновые тела — ацетон, ацетоацетат и D-β- гидроксибутират — образуются в печени. Последние два соединения служат в внепеченочных тканях «топливными» молекулами: они окисляются до ацетил-СоА и входят в цикл трикарбоновых кислот.
■ Перепроизводство кетоновых тел при неконтролируемом диабете или чрезвычайно ограниченном потреблении пищи может привести к ацидозу или кетозу.