ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ - 2014
ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
19. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ФОТОФОСФОРИЛИРОВАНИЕ
19.5. Митохондриальные гены: происхождение и мутации
В кольцевых двуспиральных молекулах митохондриальных ДНК содержится набор митохондриальных генов. В типичной клетке каждая из сотен или тысяч митохондрий имеет около пяти копий своего генома. Митохондриальные хромосомы человека (рис. 19-38) содержат 37 генов (16 569 п. н.), из которых 13 кодируют субъединицы ферментов дыхательной цепи митохондрий (см. табл. 19-6). Остальные 24 гена кодируют митохондриальные рРНК и тРНК, играющие важную роль в белковом синтезе в митохондриях. Подавляющее большинство митохондриальных белков — примерно 900 различных типов — кодируются генами ядерной ДНК и синтезируются цитоплазматическими рибосомами, а затем переносятся и собираются в митохондриях. Эти вопросы подробно излагаются в гл. 27 (т. 3).
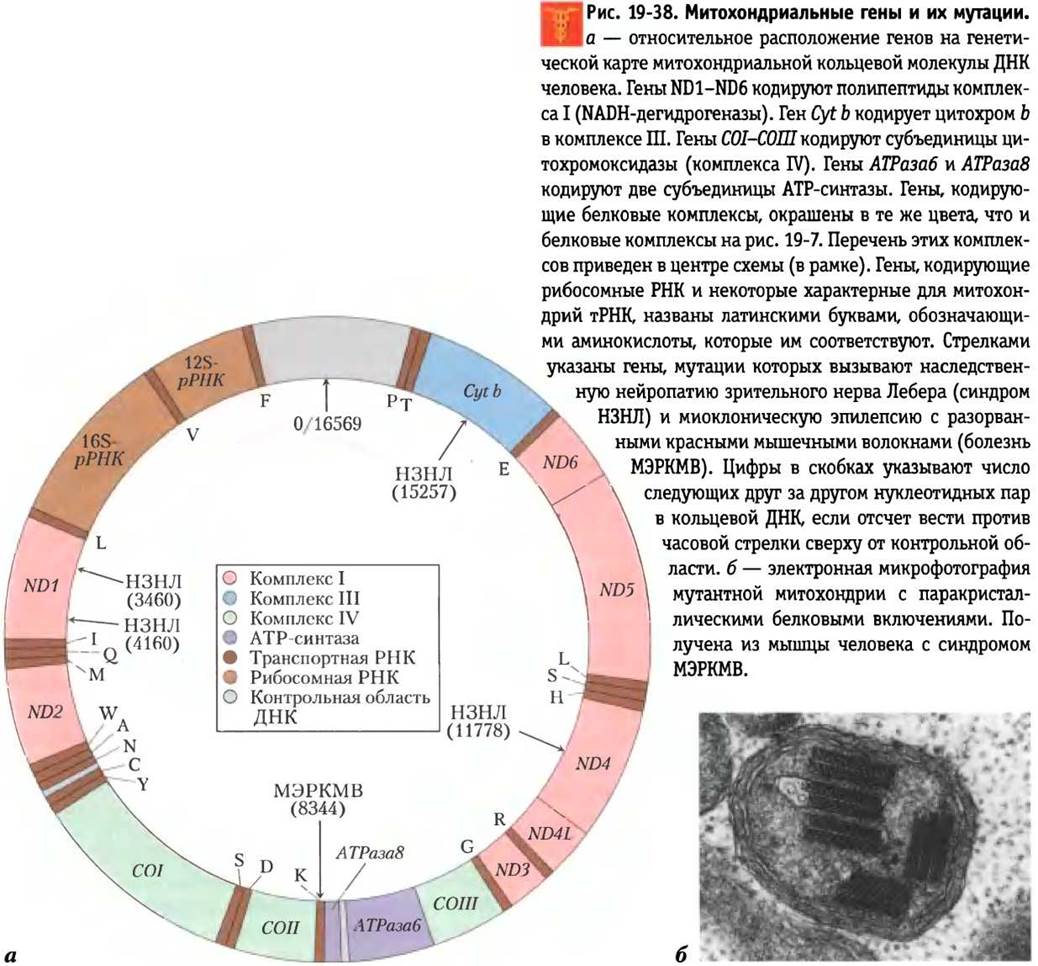
Таблица 19-6. Ферменты дыхательной цепи митохондрий, кодируемые митохондриальными генами человека
Комплекс |
Число субъединиц |
Число субъединиц, кодируемых мтДНК |
Комплекс I (NADH-дегидрогеназа) |
43 |
7 |
Комплекс II (сукцинатдегидрогеназа) |
4 |
0 |
Коплекс III (убихинон-цитохром-с-оксидоредуктаза) |
11 |
1 |
Комплекс IV (цитохромоксидаза) |
13 |
3 |
Комплекс V (АТР-синтаза) |
8 |
2 |
Митохондрии возникли в результате эндосимбиоза
Митохондрии содержат небольшие количества ДНК, а также тРНК и рибосомы (см. рис. 1-36, т. 1). Почему в митохондриях содержится ДНК? Для ответа на этот вопрос была создана гипотеза эндосимбиотического происхождения митохондрий. Согласно этой гипотезе, первыми клетками, способными использовать молекулярный кислород для окисления питательных веществ и синтеза АТР за счет энергии переноса электронов, были прокариотические клетки. В результате вторжения малых аэробных прокариотических клеток (бактерий) в цитоплазму крупных эукариотических анаэробных клеток (живущих за счет брожения) и дальнейшего эволюционного развития этих симбиотических отношений между клетками-хозяевами и клетками-паразитами, примитивные эукариоты приобрели способность к окислительному фосфорилированию, а бактерии, внедренные в цитоплазму эукариотических клеток, превратились в митохондрии.
Эта гипотеза возникновения митохондрий предполагает, что древние свободноживущие прокариотические клетки имели ферментативный аппарат для осуществления процессов окислительного фосфорилирования. Поэтому следует ожидать, что у современных бактерий, которые являются потомками этих аэробных прокариотических клеток, дыхательная цепь по своему строению и свойствам должна быть похожа на дыхательную цепь в современных эукариотических клетках. Действительно, у аэробных бактериях перенос на кислород электронов, отщепленных от субстратов с помощью NAD-зависимых дегидрогеназ, сопряжен с процессом фосфорилирования цитозольного ADP. Дегидрогеназы располагаются в бактериальных клетках в цитозоле, а переносчики электронов дыхательной цепи — в плазматической мембране. В бактериальных клетках при переносе электронов на кислород происходит выкачивание ионов Н+ наружу через плазматическую мембрану. В плазматических мембранах бактерии Escherichia coli имеются ферментные комплексы F0F1, компонент F1 которых погружен в цитозоль и катализирует синтез АТР из ADP и фосфата при возвращении протонов в клетку через протонный канал компонента F0.
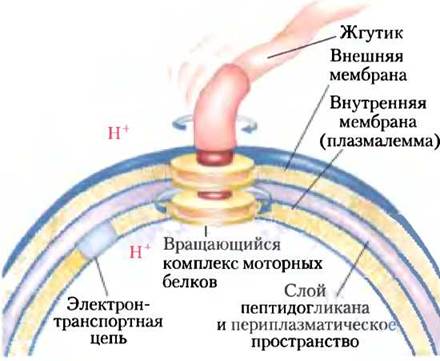
Транспорт протонов через плазматическую мембрану бактериальных клеток за счет энергии, высвобождающейся при переносе электронов по дыхательной цепи, приводит к возникновению движущей силы, используемой не только для синтеза АТР, но и для поддержания других биологических процессов. Транспортные системы некоторых бактерий способны переносить питательные вещества, например, лактозу, внутрь против градиента концентрации в симпорте с протонами (см. рис. 11-42, т. 1). Бактериальным жгутикам сообщают вращательное движение «протонные турбины» — молекулярные моторы, работающие непосредственно за счет энергии трансмембранного электрохимического потенциала, возникшего вследствие выкачивания протонов из матрикса при переносе электронов по дыхательной цепи (рис. 19-39). Можно считать, что хемиосмотический механизм передачи энергии переноса электронов на синтез АТР возник раньше, чем появились эукариотические клетки.
Рис. 19-39. Вращение бактериальных жгутиков под действием протон-движущей силы. Вращательное движение бактериальным жгутикам сообщает расположенная в клеточной мембране и состоящая из стержня и колец особая структура, которую называют «протонной турбиной». Ионы Н+, выведенные наружу в результате переноса электронов, поступают обратно в клетку через эту «турбину», вызывая вращение стержня жгутика. Движение бактериальных жгутиков отличается от движения соответствующих образований в эукариотических клетках, ресничек и мышц, происходящего за счет высвобождающейся при гидролизе АТР энергии.
На протяжении жизни организма в митохондриальной ДНК накапливаются мутации
Дыхательная цепь представляет собой основной источник активных форм кислорода в клетке, поэтому митохондрии, включая митохондриальный геном, в большей степени, чем другие отделы клетки, подвержены негативному воздействию свободных радикалов кислорода. Кроме того, система репликации митохондриальной ДНК не так эффективно исправляет допущенные ошибки, как система репликации ядерной ДНК. В результате со временем в митохондриальной ДНК накапливаются ошибки. По одной из теорий именно, это постепенное накопление ошибок и является основной причиной «симптомов» старения, например таких, как развитие слабости скелетных и сердечной мышц.
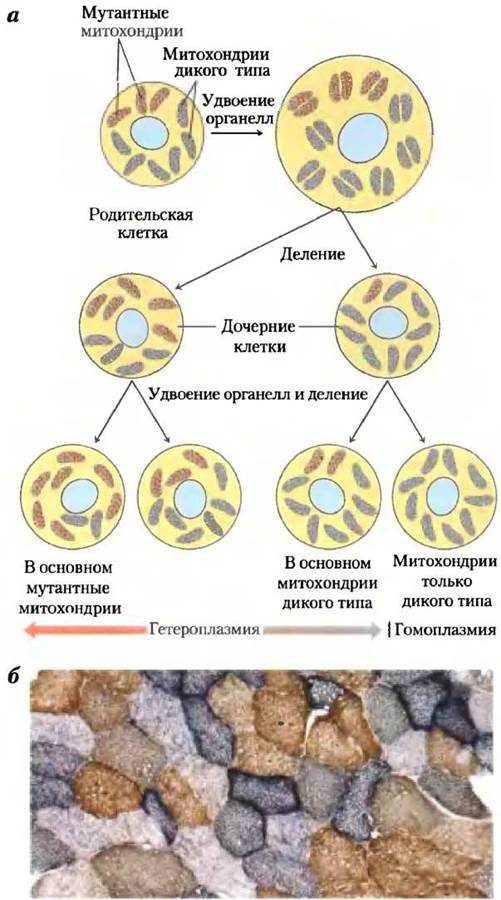
Особенности наследования генетического материала митохондрий приводят к тому, что отдельные клетки, а также разные организмы несут разное количество мутаций. Обычная клетка содержит сотни или тысячи митохондрий, каждая имеет свою собственную копию генома (рис. 19-40). Предположим, что в организме женщины произошло повреждение митохондриального генома зародышевой клетки, из которой образуется яйцеклетка, в результате чего эта зародышевая клетка содержит в основном митохондрии с генами дикого типа и одну митохондрию с дефектным геном. В процессе созревания яйцеклетки при ее многократном делении число митохондрий с дефектом увеличивается и распределяется случайным образом среди дочерних клеток. В итоге зрелые яйцеклетки содержат разное количество дефектных митохондрий. После оплодотворения яйцеклетки и многократного деления клеток в процессе развития зародыша образуются соматические клетки, содержащие разное количество мутировавших митохондрий (рис. 19-41, а). (Вспомните, что все митохондрии в клетках зародыша происходят от яйцеклетки, а не от сперматозоида.) Подобная гетероплазмия митохондриальной ДНК (в отличие от гомоплазмии, при которой геномы всех митохондрий во всех клетках идентичны) приводит к появлению мутантных фенотипов с отклонениями разной степени тяжести. Клетки (и ткани), содержащие в основном митохондрии дикого типа, имеют фенотип дикого типа и являются нормальными. Другие клетки с гетероплазмией митохондриальной ДНК имеют промежуточный фенотип: одни практически нормальные, другие (с более высоким содержанием мутантных митохондрий) — аномальными (рис. 19-41, б). Если такой аномальный фенотип связан с каким-либо заболеванием (см. ниже), то люди с одинаковой мутацией митохондриальной ДНК могут иметь симптомы заболевания разной степени тяжести — в зависимости от количества и распределения поврежденных митохондрий.
Рис. 19-40. В каждой клетке содержится множество митохондрий. Обычная клетка организма животного содержит несколько сотен или тысяч митохондрий, причем геном некоторых из этих митохондрий может содержать мутации, нарушающие функционирование митохондрии. Эта эпителиальная клетка почки овцы была выращена в лабораторных условиях, зафиксирована, а затем окрашена с помощью флуоресцентных маркеров. При визуализации с помощью флуоресцентного микроскопа митохондрии выглядят золотыми, актиновые микрофиламенты — красными, а ядра — зелеными.
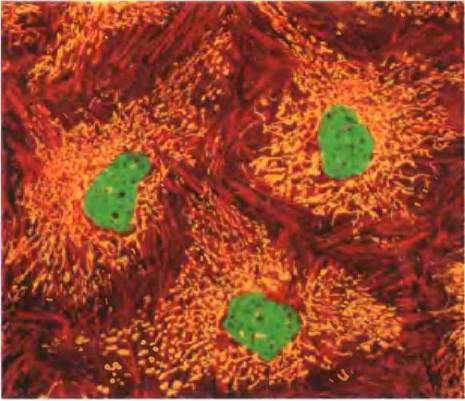
Рис. 19-41. Гетероплазмия митохондриальной ДНК. а — после оплодотворения зрелой яйцеклетки все митохондрии образующейся диплоидной клетки (зиготы) являются материнскими — ни одна не происходит от сперматозоида. Если некоторые митохондрии материнской клетки содержали мутировавший ген, в результате случайного распределения митохондрий в ходе последующих делений клетки появятся дочерние клетки с высоким, промежуточным и низким содержанием дефектных митохондрий. Таким образом, дочерние клетки различаются по степени гетероплазмии. б — различная степень гетероплазмии приводит к образованию разного фенотипа. Здесь представлен срез мышечной ткани человека с дефектом цитохромоксидазы. Образец окрашен таким образом, что клетки дикого типа выглядят синими, а клетки с мутантным ферментом коричневыми. Как видно, мутация митохондриальной ДНК в различной степени влияет на отдельные клетки в одной и той же ткани.
Мутации митохондриальных генов вызывают заболевания человека
Все большее число заболеваний человека связывают с мутациями митохондриальных генов, снижающими способность клеток производить АТР. Некоторые типы клеток и тканей — нейроны, миоциты скелетных и сердечной мышц, а также клетки поджелудочной железы — хуже других клеток переносят уменьшение количества АТР и поэтому сильнее повреждаются при мутациях генов митохондриальных белков. Число выявленных заболеваний человека, вызванных мутациями митохондриальных генов, возрастает по мере развития методов регистрации последствий мутаций.
Многие из этих болезней, известные под названием митохондриальных энцефалопатий, связаны в основном с поражением мозга и скелетных мышц. Это наследственные заболевания; они передаются от матери, поскольку эмбрион получает митохондриальные гены, в том числе мутантные, от материнской яйцеклетки. Редкое заболевание наследственная нейропатия зрительного нерва Лебера (НЗНЛ), связанная с поражением центральной нервной системы, включая зрительные нервы, вызывает двустороннюю потерю зрения уже в раннем возрасте. Замена одного азотистого основания на другое в митохондриальном гене ND4 вызывает в полипептидной цепи комплекса I изменение: вместо остатка аргинина там находится гистидин, в результате чего митохондрии недостаточно эффективно выполняют функции по переносу электронов от NADH на убихинон (рис. 19-38, а). Митохондрии с мутантным геном сохраняют способность синтезировать некоторое количество АТР за счет энергии переноса электронов от сукцината, но этого оказывается недостаточно для поддержания активных процессов метаболизма в нейронах, в результате чего возникает повреждение зрительного нерва, приводящее к слепоте. Замена одного азотистого основания на другое в митохондриальном гене, кодирующем цитохром b в комплексе III, также вызывает появление синдрома НЗНЛ. Эти примеры показывают, что у человека наследственные патологии могут возникать из-за общего снижения способности митохондрий выполнять свои функции, а не из-за нарушений в механизме переноса электронов через комплекс I.
Мутация (в АТР6), поражающая протонный канал АТР-синтазы, приводит к снижению скорости синтеза АТР, не затрагивая последовательности дыхательной цепи. Окислительный стресс, связанный с постоянным поступлением электронов от NADH, сопровождается увеличением продукции активных форм кислорода, а вызываемое ими повреждение митохондрий замыкает порочный круг. Половина новорожденных с мутацией данного гена умирает через несколько дней или месяцев после рождения.
Миоклоническая эпилепсия с разорванными красными мышечными волокнами (синдром МЭРКМВ) возникает в результате мутаций в митохондриальном гене, кодирующем транспортную РНК, связывающую лизин (тРНКLus). Для этого заболевания характерно неконтролируемое подергивание мышц, по-видимому, вследствие нарушения биосинтеза нескольких белков с участием митохондриальных тРНК. Митохондрии из волокон скелетных мышц человека, страдающего синдромом МЭРКМВ, имеют резко очерченный контур и иногда содержат паракристаллические включения (рис. 19-38, б). Другие мутации митохондральных генов, вероятно, вызывают прогрессирующую слабость мышц, характерную для митохондриальной миопатии, а также увеличение и нарушения работы сердечной мышцы, характерное для гипертрофированной кардиомиопатии. Согласно одной из гипотез, прогрессирующие возрастные изменения в организме человека являются результатом накопления в течение жизни мутаций митохондриальных ДНК, возникших под действием таких АФК, как •O2-. Митохондрии с поврежденными ДНК не могут обеспечить клетки организма достаточным количеством АТР. Заболевания, вызванные дефектами митохондрий, могут возникнуть также из-за мутаций любого из 900 генов ядерной ДНК, кодирующих полипептидные цепи митохондрий. ■
Диабет может возникать из-за дефекта митохондрий в β-клетках поджелудочной железы
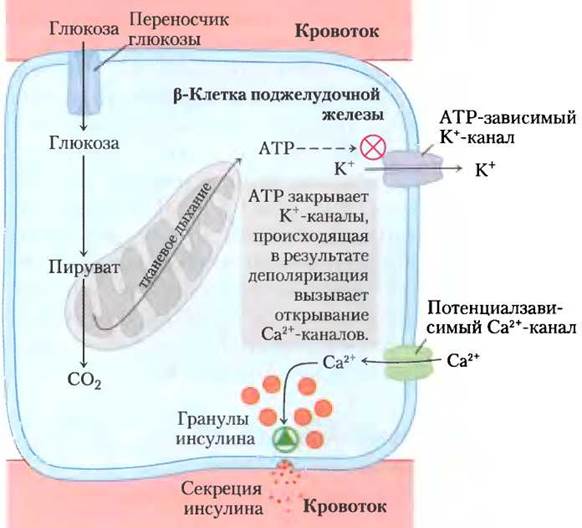
Механизм регуляции высвобождения инсулина (3-клетками поджелудочной железы тесно связан с концентрацией АТР в этих клетках. При высоком уровне глюкозы крови глюкоза, поступая в β-клетки, окисляется там в процессе гликолиза и в цикле лимонной кислоты, в результате чего концентрация АТР увеличивается выше порогового уровня (рис. 19-42). Как только концентрация АТР превышает это значение, закрываются ATP-зависимые калиевые каналы в плазматической мембране, что приводит к деполяризации мембраны и высвобождению инсулина (см. рис. 23-28). Панкреатические β-клетки с нарушением окислительного фосфорилирования не могут создавать концентрацию АТР выше порогового значения, в результате чего нарушается процесс высвобождения инсулина и развивается диабет. Например, дефекты гена глюкокиназы (изофермент гексокиназы IV, присутствующий в р-клетках) приводят к появлению редкой формы диабета с фенотипом MODY2 (см. доп. 15-3). Низкая активность глюкокиназы не позволяет превысить пороговую концентрацию АТР, блокируя секрецию инсулина. Мутации митохондриальных генов тРНКLYS или TPHKLeu также нарушают выработку АТР в митохондриях, поэтому у человека с такой мутацией нередко возникает сахарный диабет II типа (хотя эти случаи составляют лишь малую долю всех случаев заболевания диабетом).
При генетических мутациях NADP-транс- гидрогеназы — важного элемента системы защиты от АФК (рис. 19-18) — накопление свободных радикалов приводит к повреждению митохондрий, уменьшая образование АТР и блокируя высвобождение инсулина β-клетками (рис. 19-42). Вызванные свободными радикалами повреждения, включая повреждения митохондриальной ДНК, могут быть причиной и других заболеваний человека; известны данные, что они способствуют возникновению болезней Альцгеймера, Паркинсона, Хантингтона и заболеваний сердца, а также связаны с процессами старения. ■
Рис. 19-42. Нарушение окислительного фосфорилирования в β-клетках поджелудочной железы блокирует секрецию инсулина. Б норме при повышении концентрации глюкозы усиливается выработка АТР в клетках. АТР блокирует К+-каналы, что приводит к деполяризации мембраны и открыванию потенциалзависимых Са2+-каналов. Происходящий при этом приток Са2+ запускает экзоцитоз содержащих инсулин секреторных гранул и высвобождение инсулина. При нарушении окислительного фосфорилирования в клетках концентрация АТР никогда не достигает необходимого уровня, чтобы запустить этот процесс, поэтому высвобождения инсулина не происходит.
Краткое содержание раздела 19.5 Митохондриальные гены: происхождение и мутации
■ Гены митохондриальной ДНК в клетках человека кодируют лишь некоторые митохондриальные белки (около 13 белков), синтезируемых в митохондриях и участвующих в окислительном фосфорилировании.
■ Митохондрии происходят от аэробных бактерий, когда-то проникших в эукариотические клетки и закрепившихся в них в процессе эволюции.
■ Мутации митохондриального генома накапливаются в течение жизни организма. Мутации в генах, которые кодируют компоненты дыхательной цепи, ATP-синтазу, систему защиты от АФК, а также мутации в генах тРНК вызывают у человека ряд заболеваний, чаще всего поражающих мышечный аппарат, сердце, (3-клетки поджелудочной железы и мозг.
ФОТОСИНТЕЗ: ПОГЛОЩЕНИЕ СОЛНЕЧНОЙ ЭНЕРГИИ
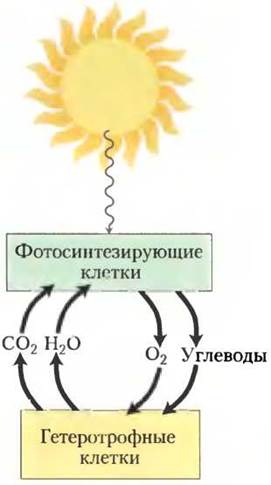
Обратимся к рассмотрению молекулярных процессов, в результате которых под действием энергии света, поглощаемой фотосинтезирующими организмами, происходит движение электронов и сопряженное с ним образование АТР. В итоге солнечная энергия, превращенная в химическую энергию восстановленных органических соединений, служит источником почти всей биологической энергии. Фотосинтезирующие и гетеротрофные организмы сосуществуют в биосфере в сбалансированном стационарном состоянии (рис. 19-43). Фотосинтезирующие организмы поглощают солнечную энергию и запасают ее в форме АТР и NADPH, которые служат им источником энергии для синтеза углеводов и других органических компонентов клетки из углекислого газа и воды; при этом они выделяют в атмосферу кислород. Аэробные гетеротрофы, например человек и растения в темноте, используют этот кислород для расщепления богатых энергией органических продуктов фотосинтеза до СO2 и Н2O и за счет этой энергии синтезируют АТР для своих собственных нужд. Углекислый газ СO2, образующийся при дыхании гетеротрофов, возвращается в атмосферу и вновь используется фотосинтезирующими организмами. Солнечная энергия создает движущую силу для круговорота, в процессе которого углекислый газ и кислород атмосферы непрерывно циркулируют, проходя через биосферу и образуя восстановленные субстраты, например, глюкозу, которая служит источником энергии для нефотосинтезирующих организмов.
Рис. 19-43. Солнечная энергия — первичный источник всей биологической энергии. Фотосинтезирующие клетки используют энергию солнечного света для образования глюкозы и других органических веществ. Эти органические продукты служат гетеротрофным клеткам источником энергии и углерода.
Фотосинтез происходит не только в хорошо знакомых нам сосудистых растениях, но также в одноклеточных эукариотах (водорослях) и разнообразных бактериях. В принципе у различных организмов фотосинтез протекает одинаково, хотя заметны и некоторые особенности в зависимости от вида фотосинтезирующих клеток. Результаты изучения процесса фотосинтеза у простейших организмов можно использовать при установлении механизмов фотосинтеза в высших растениях. Для процесса фотосинтеза у растений, когда для восстановления углекислого газа до углеводов в качестве донора электронов (водорода) используется вода, общее уравнение можно записать следующим образом:
![]()