ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ - 2014
ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
14. ГЛИКОЛИЗ, ГЛЮКОНЕОГЕНЕЗ И ПЕНТОЗОФОСФАТНЫЙ ПУТЬ
14.3. Превращение пирувата в анаэробных условиях: брожение
В аэробных условиях пируват, образующийся на финальной стадии гликолиза, окисляется до ацетата (ацетил-СоА), который поступает в цикл лимонной кислоты и окисляется до СO2 и Н2O, a NADH, образующийся при дегидрировании глицеральдегид-3-фосфата, в итоге вновь окисляется до NAD+ в результате передачи электронов на O2 в митохондриях. Однако при недостатке кислорода (при гипоксии), например, в активно работающих мышцах, в подводных частях растений или у молочнокислых бактерий, образовавшийся в результате гликолиза NADH не может возвращаться в окисленную форму с помощью O2. Невозможность регенерации NAD+ оставляла бы клетки без акцептора электронов, необходимых для окисления глицеральдегид-3-фосфата, что привело бы к остановке энергетически выгодных реакций гликолиза. Следовательно, должен существовать какой-то другой путь регенерации NАD+.
Первые клетки, появившиеся в практически лишенной кислорода атмосфере, умели добывать энергию из топливных молекул в анаэробных условиях. Большинство современных организмов сохранили способность регенерировать NАD+ в анаэробном процессе гликолиза путем переноса электронов от NАDН с образованием таких восстановленных конечных продуктов, как лактат или этанол.
Пируват является последним акцептором электронов при молочнокислом брожении
Если ткани животных не получают достаточного количества кислорода, чтобы поддерживать аэробное окисление пирувата и NАDН, образовавшихся в результате гликолиза, то регенерация NАD+ из NАDН происходит путем восстановления пирувата до лактата. Как уже отмечалось выше, некоторые типы клеток и тканей (например, эритроциты, не имеющие митохондрий и не способные окислять пируват до СO2) образуют лактат из глюкозы даже в аэробных условиях. Восстановление пирувата катализирует фермент лактатдегидрогеназа, под действием которой при pH 7 образуется L-изомер лактата:
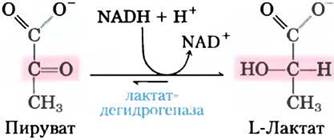
∆G′°= -25,1 кДж/моль
Равновесие этой реакции сильно сдвинуто в сторону образования лактата, на что указывает большое отрицательное изменение стандартной свободной энергии.
При гликолизе дегидрирование двух молекул глицеральдегид-3-фосфата, образующихся из каждой молекулы глюкозы, сопровождается превращением двух молекул NАD+ в две молекулы NАDН. Поскольку восстановление двух молекул пирувата до двух молекул лактата приводит к образованию двух молекул NАD+, то суммарное содержание NАD+ и NАDН не меняется.
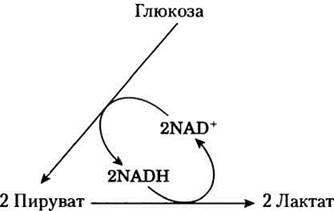
Лактат, образующийся при активной работе мышц (или в эритроцитах), может быть повторно использован. При восстановлении сил после активной мышечной деятельности он переносится кровотоком к печени, где превращается в глюкозу. Во время активной физической нагрузки (например, при спринтерском беге) образуется большое количество лактата; снижение pH в крови и мышцах, связанное с диссоциацией молочной кислоты, ограничивает период наиболее напряженной физической активности. Даже тренированные легкоатлеты в самой лучшей спортивной форме способны бежать с максимальной скоростью не более одной минуты (доп. 14-2).
Хотя превращение глюкозы в лактат протекает через две окислительно-восстановительные стадии, углерод не меняет своей степени окисления: в глюкозе (С6Н12O6) и молочной кислоте (С3Н6O3) соотношение Н:С одно и то же. Тем не менее некоторое количество энергии, заключенной в молекуле глюкозы, при превращении в лактат высвобождается, и этой энергии достаточно для образования двух молекул АТР на одну молекулу расщепленной глюкозы. Подобные процессы, идущие с выделением энергии (в форме АТР), но не сопровождающиеся потреблением кислорода или изменением концентрации NAD+ и NADH, обычно называют брожением. Брожение осуществляют очень многие организмы, часто обитающие в анаэробных условиях; конечные продукты брожения довольно разнообразны и нередко находят практическое применение.
Дополнение 14-2. Спортсмены, аллигаторы и целаканты: гликолиз при пониженном содержании кислорода
Большинство позвоночных являются аэробными организмами; они превращают глюкозу в пируват в процессе гликолиза, а затем с помощью молекулярного кислорода полностью окисляют пируват до СO2 и Н2O. Анаэробный катаболизм глюкозы до лактата происходит в краткие моменты чрезвычайно высокого мышечного напряжения, например, при беге на стометровку, когда кислород не успевает поступать в мышцы с достаточной скоростью, чтобы окислять пируват. В это время мышцы в качестве источника энергии для выработки АТР используют внутренние запасы глюкозы (гликоген), сбраживая ее до лактата. При спринтерском беге концентрация лактата в крови достигает очень высоких значений. В процессе глюконеогенеза в печени лактат медленно превращается обратно в глюкозу (это происходит после снятия нагрузки при восстановлении дыхания, когда интенсивность потребления кислорода снижается), постепенно достигая нормы. Избыток кислорода, потребленного при восстановлении дыхания, покрывает его предыдущие затраты. При восстановлении дыхания кислород необходим для синтеза АТР в процессе глюконеогенеза, цель которого — регенерировать гликоген, «заимствованный» из печени и мышц в период максимальной нагрузки. Цикл реакций, включая превращение глюкозы в лактат в мышцах и превращения лактата в глюкозу в печени, называют циклом Кори в честь Карла и Герти Кори, работы которых (1930-1940 гг.) позволили объяснить суть и роль данного метаболического пути (см. доп. 15-1).
Кровеносная система большинства мелких позвоночных достаточно быстро переносит кислород к мышцам, так что не возникает необходимости использовать анаэробный путь разложения мышечного гликогена. Например, перелетные птицы часто без отдыха покрывают большие расстояния с высокой скоростью, не превышая обычных затрат кислорода. В мышцах многих «бегающих» животных среднего размера также поддерживается почти исключительно аэробный метаболизм. А вот кровеносная система более крупных животных, к которым относится и человек, не может полностью обеспечивать аэробный метаболизм в мышцах в длительные периоды интенсивной мышечной активности. Такие животные в обычных условиях передвигаются довольно медленно, а интенсивная мышечная деятельность развивается лишь в случае крайней необходимости, поскольку подобные вспышки активности требуют периода длительного восстановления для погашения перерасхода кислорода.
Аллигаторы и крокодилы, например, в обычных условиях довольно пассивны. Лишь при возбуждении они способны на молниеносную атаку и стремительные удары своим мощным хвостом. Время такой взрывной активности очень короткое, а после этого наступает длительный период восстановления. Движения, осуществляемые в случае крайней необходимости, сопровождаются сбраживанием молочной кислоты в мышцах с образованием АТР. При этом запасы мышечного гликогена быстро расходуются, а концентрация лактата в мышцах и внеклеточных жидкостях резко возрастает. После бега на стометровку спортсмен восстанавливает дыхание примерно за полчаса или даже быстрее, а вот аллигатору после вспышки активности может потребоваться много часов покоя и повышенного потребления кислорода для удаления избытка лактата из крови и восстановления уровня мышечного гликогена.
Другие крупные животные, например, слоны и носороги, а также ныряющие млекопитающие, такие как киты и тюлени, имеют похожие особенности метаболизма. Возможно, динозавры и другие вымершие крупные животные для своей мышечной активности использовали молочнокислое брожение, требующее длительных периодов восстановления, и в это время они были уязвимы для более мелких хищников, способных лучше использовать кислород и более приспособленных к продолжительной мышечной активности.

Глубоководные исследования позволили обнаружить огромное разнообразие жизни на больших морских глубинах, где концентрация кислорода практически равна нулю. Например, оказалось, что у первобытного целаканта — огромной рыбы, живущей у побережья Южной Африки на глубинах около 4000 м, практически во всех тканях осуществляется анаэробный метаболизм. В организме этого животного углеводы превращаются в лактат и другие продукты, большинство из которых должны удаляться. Некоторые морские позвоночные получают АТР путем сбраживания глюкозы до этанола и СO2.
Этанол — восстановленный продукт спиртового брожения
Дрожжи и другие микроорганизмы сбраживают глюкозу не до лактата, а до СO2 и этилового спирта. Сначала в процессе гликолиза глюкоза превращается в пируват, а затем пируват в двустадийном процессе разлагается на этанол и СO2:
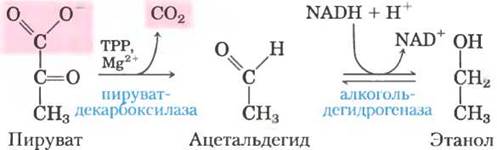
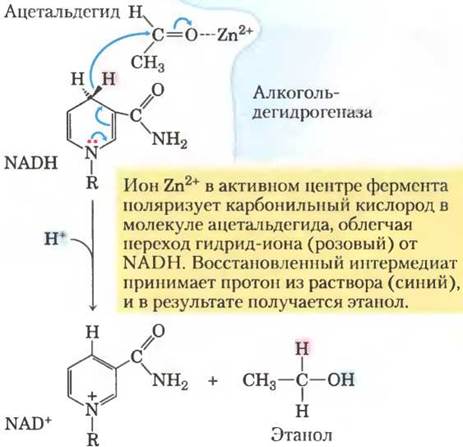
На первой стадии пируват необратимо декарбоксилируется под действием пируватдекарбоксилазы. Эта простая реакция декарбоксилирования не приводит к окислению пирувата. Пируватде- карбоксилаза требует присутствия ионов и кофермента тиаминпирофосфата (ТРР). На второй стадии ацетальдегид восстанавливается до этанола под действием алкогольдегидрогеназы; при этом роль восстановителя играет NАDН, образовавшийся при дегидрировании глицеральдегид-3-фосфата. Данная реакция хорошо изучена и является примером переноса водорода с участием NАDН (рис. 14-13). Таким образом, продукты спиртового брожения — этанол и СO2, что можно записать в виде суммарного уравнения реакции:
Глюкоза + 2 ADP + 2 Pi —> 2 этанол + 2 СO2 + 2 АТР + 2 Н2O
Рис. 14-13. Механизм реакции. Действие алкогольдегидрогеназы. Механизм действия алкогольдегидрогеназы
Как и в случае молочнокислого брожения, при спиртовом брожении не меняется соотношение числа атомов водорода и углерода при превращении глюкозы (Н:С = 12:6 = 2) в две молекулы этанола и две молекулы СO2 (в сумме Н:С = 12:6 = 2). При любом процессе брожения в исходных веществах и продуктах реакции отношение Н: С одинаково.
Пируватдекарбоксилаза обнаружена у пивных и пекарских дрожжей (Saccaromyces cerevisiae), а также у всех других организмов, сбраживающих глюкозу до этилового спирта, в том числе и у некоторых растений. Характерные пузырьки в шампанском связаны с декарбоксилированием пирувата и образованием СO2 под действием пивных дрожжей. Древнее искусство пивоварения кроме реакций спиртового брожения включает в себя целый ряд других ферментативных процессов (доп. 14-3). При изготовлении хлеба именно СO2, выделяющийся при смешивании дрожжей с сахаром, заставляет подниматься тесто. Этот фермент отсутствует в тех тканях позвоночных, а также у тех организмов, которые осуществляют молочнокислое брожение.
Алкогольдегидрогеназа обнаружена у многих организмов, способных метаболизировать этанол, в том числе у человека. В печени этот фермент катализирует окисление этанола как потребленного человеком, так и образованного кишечной микрофлорой; этот процесс сопровождается восстановлением NAD+ до NADH. В данном случае реакция протекает в направлении, обратном образованию этанола при брожении.
Тиаминпирофосфат переносит «активные» ацетальдегидные группы
При рассмотрении реакции, катализируемой пируватдекарбоксилазой, мы впервые сталкиваемся с коферментом тиаминпирофосфатом (ТРР; рис. 14-14) — производным витамина В1. Недостаток витамина В1 в рационе питания человека может привести к развитию болезни бери- бери, характеризующейся накоплением жидкости в организме (отеками), болями, параличом; болезнь может иметь летальный конец. ■
Дополнение 14-3. Спиртовое брожение: пивоварение и производство биотоплива
Пивоварением люди начали заниматься давно, а на определенном этапе перенесли этот процесс в крупномасштабное производство. Пиво является продуктом спиртового брожения углеводов, содержащихся в семенах зерновых культур (например, ячменя), под действием гликолитических ферментов дрожжей. Углеводы, в основном полисахариды, прежде всего должны расщепиться на ди- и моносахариды. Поэтому сначала готовят солод, для чего семена ячменя проращивают до тех пор, пока они не синтезируют необходимые гидролитические ферменты, а затем дальнейшее проращивание прекращают нагреванием. Полученный солод содержит ферменты, катализирующие гидролиз β-связей в целлюлозе и в других полисахаридах из клеточных стенок семенных оболочек ячменя, а также другие ферменты, например, α-амилазу и мальтазу.
Следующий производственный процесс пивоварения — приготовление сусла, т. е. питательной среды для роста клеток дрожжей. Солод смешивают с водой, а затем дробят или растирают. При этом ферменты солода воздействуют на полисахариды и расщепляют их до мальтозы, глюкозы и других простых сахаров, растворимых в водной среде. Затем клеточный остаток отделяют, а жидкое сусло варят, добавляя для ароматизации хмель, охлаждают и аэрируют.
На следующем этапе добавляют клетки дрожжей. В аэробном сусле дрожжи растут и размножаются очень быстро, получая энергию из присутствующих в сусле сахаров, причем этиловый спирт не образуется, поскольку при достаточном содержании кислорода дрожжи окисляют возникающий в результате гликолиза пируват до СO2 и Н2O через цикл лимонной кислоты. После того как весь растворенный в сусле кислород исчерпан, клетки дрожжей переключаются на анаэробный метаболизм и начинают сбраживать сахара до этилового спирта и СO2. Процесс брожения контролируется концентрацией образующегося этанола, значением pH и количеством оставшихся сахаров. После остановки брожения дрожжевые клетки удаляют, а молодое пиво готово для финальной стадии дображивания.
На этой заключительной стадии пивоварения контролируют количество пены, возникающей из-за наличия в пиве растворенных белков. Обычно образование пены регулируется протеолитическими ферментами, выделяющимися в процессе приготовления солода. Если эти ферменты воздействуют на белки слишком долго, то пены и пузырьков возникает мало, а если недостаточно долго, то охлажденное пиво не будет прозрачным. Иногда для пенообразования к пиву добавляют протеолитические ферменты из других источников.
Технология крупномасштабного производства алкогольных напитков в настоящее время используется и для решения совершенно иной задачи — для производства этанола в качестве альтернативного топлива. Из-за понимания того факта, что ископаемые ресурсы могут закончиться, а также из-за роста цен на топливо для двигателей внутреннего сгорания, проявляется интерес к этанолу как альтернативе традиционному топливу или добавки к топливу. Основным преимуществом этилового спирта в качестве топлива является возможность его получения из сравнительно недорогих и возобновляемых источников, богатых сахарозой, крахмалом или целлюлозой (крахмал — из кукурузы или пшеницы, сахароза — из сахарной свеклы или сахарного тростника, а целлюлоза — из соломы, отходов деревообрабатывающей промышленности или твердых городских отходов). Обычно сначала исходный материал химическим путем превращают в моносахариды, а затем эту смесь используют в качестве питательного субстрата для определенных штаммов дрожжей в промышленных ферментерах (рис. 1). В результате ферментации образуется не только этанол, но и побочные продукты, такие как белки, которые можно использовать в качестве кормовых добавок в животноводстве.
Рис. 1. Промышленное брожение для получения биотоплива и других продуктов обычно проводят в ферментерах объемом на тысячи литров среды.

Тиаминпирофосфат (ТРР) играет важную роль при расщеплении связей, прилегающих к карбонильной группе, например, при декарбоксилировании α-кетокислот, а также в тех химических реакциях, при которых происходит перенос активированной ацетальдегидной группы между двумя атомами углерода (табл. 14-1). Функциональная часть молекулы ТРР (тиазольное кольцо) имеет довольно кислый протон при атоме С-2. Диссоциация этого протона приводит к образованию карбаниона, который как раз и является активным началом в ТРР-зависимых реакциях (рис. 14-14). Карбанион легко взаимодействует с карбонильными группами, а тиазольное кольцо выступает в качестве «электронной ловушки», сильно облегчающей такие реакции, как декарбоксилирование под действием пируватдекарбоксилазы.
Таблица 14-1. Некоторые ТРР-зависимые реакции

С помощью брожения получают многие продукты питания и химические реагенты
Уже несколько тысяч лет назад наши предки использовали процесс брожения для получения и переработки продуктов питания. Некоторые микроорганизмы, присутствующие в сырых пищевых продуктах, сбраживают углеводы и превращают их в продукты метаболизма, придающие пище ее характерную форму, текстуру и вкус. Йогурт, известный с библейских времен, образуется в результате жизнедеятельности бактерии Lactobacillus bulgaricus, сбраживающей углеводы молока до молочной кислоты; происходящее при этом уменьшение pH среды приводит к осаждению молочных белков, что и создает густую консистенцию и кисловатый привкус натурального йогурта. Бактерия Propionibacterium freudenreichii сбраживает углеводы молока с образованием пропионовой кислоты и СO2; пропионовая кислота осаждает молочные белки, а пузырьки газа создают сырные дырки, так характерные для сортов швейцарского сыра. Многие другие продукты питания также получают в результате брожения; это пикули, квашеная капуста, сосиски и колбасы, соевый соус, а также множество излюбленных продуктов национальной кухни, таких как кимчи (Корея), темпояк (Индонезия), кефир (Россия), дахи (Индия) и позол (Мексика). Уменьшение pH среды, сопровождающее брожение, позволяет консервировать продукты питания, поскольку большинство микроорганизмов, вызывающих порчу продуктов, не способны расти при низких значениях pH. В сельском хозяйстве отходы растениеводства, такие как стебли кукурузы, используют на корм скоту в виде силоса; для приготовления силосной массы отходы собирают в больших контейнерах (силосных ямах), где при ограниченном доступе воздуха происходит микробное брожение, что снижает pH силосной массы. Силос может храниться долгое время и не портиться.
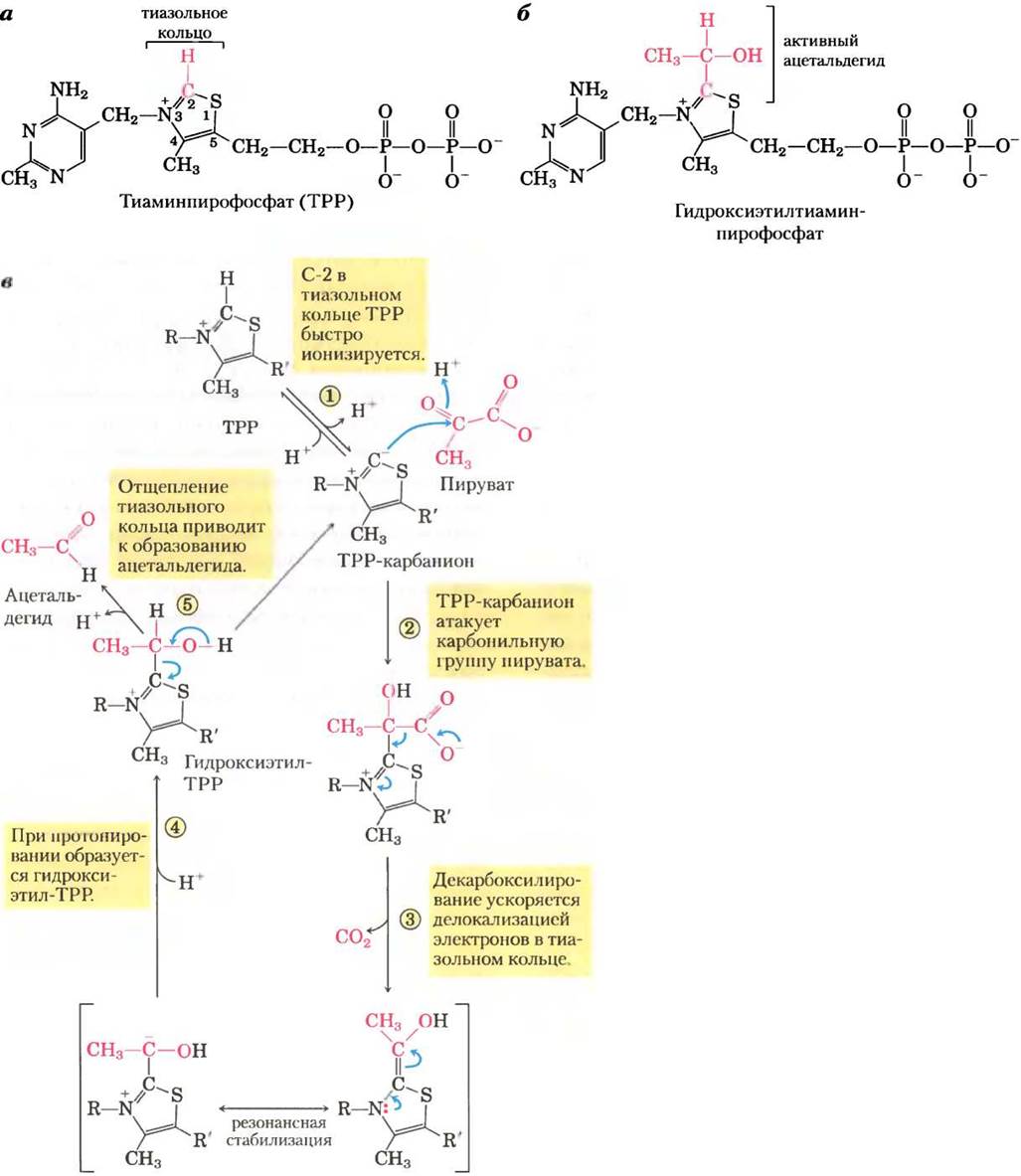
Рис. 14-14. Механизм реакции. Тиаминпирофосфат (ТРР) и его роль при декарбоксилировании пирувата. а — в форме ТРР витамин В1 (тиамин) выступает в роли кофермента. Красным цветом выделен реакционноспособный атом углерода в тиазольном кольце молекулы ТРР. В реакции, катализируемой пируватдекарбоксилазой, два из трех атомов углерода пирувата временно переносятся на ТРР в форме гидрокси- этильной («активной» ацетальдегидной) группы (6), которая впоследствии высвобождается в виде ацетальдегида, в — тиазольное кольцо в ТРР стабилизирует карбанион, поскольку является электронодефицитной структурой, позволяющей делокализовать электроны карбаниона за счет резонансной стабилизации. Обладающие таким свойством структуры иногда называют «электронными ловушками»; они играют важную роль во многих биохимических реакциях (здесь помогают разорвать связь С-С). Механизм действия тиаминпирофосфата
В 1910 г. Хаим Вейцман (позже он стал первым президентом Израиля) обнаружил, что бактерия Clostridium acetobutyricum превращает крахмал в смесь бутилового спирта и ацетона. Это открытие послужило началом развития промышленной ферментации, при которой некоторые доступные богатые сахарами вещества (например, кукурузный крахмал или мелассу), смешивают с чистой культурой специфических микроорганизмов, способных превратить их в более ценные продукты. Так, используемый для получения газохола (смесь спирта с бензином) метанол, а также муравьиная, уксусная, пропионовая, масляная, янтарная кислоты, глицерин, этанол, изопропанол, бутанол и бутандиол получают в промышленности с помощью ферментации. Промышленную ферментацию обычно проводят в больших закрытых цистернах, в которых температура и подача воздуха регулируются таким образом, чтобы создать наиболее благоприятные условия для развития полезных микроорганизмов и неблагоприятные — для нежелательных микроорганизмов. Прелесть промышленной ферментации заключается в том, что сложные, многостадийные химические превращения осуществляются с высоким выходом и небольшим количеством побочных продуктов под действием самовоспроизводящихся живых «химических заводов» — микробных клеток. В некоторых технологиях применяются иммобилизованные на инертном носителе клетки, что позволяет осуществлять непрерывный процесс, пропуская исходный субстрат через слой клеток и собирать на выходе конечный продукт. Это ли не мечта инженеров!
Краткое содержание раздела 14.З Превращение пирувата в анаэробных условиях: брожение
■ Образующийся в процессе гликолиза NADH должен быть вновь переведен в окисленную форму — в NAD+, который необходим в качестве акцептора электронов в начале второй стадии гликолиза. В аэробных условиях это осуществляется в митохондриях путем передачи электронов от NADH на O2.
■ В анаэробных условиях или при пониженном содержании кислорода многие организмы регенерируют NAD+, перенося электроны от NADH на молекулу пирувата, в результате чего образуется лактат. Другие организмы, такие как дрожжи, получают NAD+ при восстановлении пирувата до этилового спирта и СO2. При таком анаэробном процессе (брожении) не происходит окисления или восстановления углерода в молекулах глюкозы.
■ Многие микроорганизмы способны сбраживать сахар, содержащийся в сырой пище, что изменяет кислотность (pH), вкус и текстуру продуктов и, кроме того, защищает их от гниения. Процесс брожения используют в промышленных масштабах для получения различных ценных продуктов из недорогого исходного органического сырья.