Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Фибриллярные белки
Рентгеноструктурные исследования пептидов свидетельствуют о жесткости и плоской конфигурации пептидных групп
Следующий шаг в развитии наших знаний о пространственной структуре белков был сделан в 40-х и начале 50-х годов Лайнусом Полингом и Робертом Кори (США). Они получили дифракционные картины кристаллов аминокислот и простых ди- и трипептидов. На основе этих рентгенограмм им удалось установить точную структуру пептидной группы. Они обнаружили, что С—N-связь, соединяющая два аминокислотных остатка в пептидной цепи (рис. 7-4), короче большинства других С—N-связей, например С—N-связи в простых аминах. Более того, пептидная С—N-связь имеет в какой- то степени характер двойной связи и поэтому вокруг нее не может происходить свободного вращения. Далее эти ученые сделали вывод, что четыре атома пептидной группы лежат в одной плоскости, причем атом кислорода карбонильной группы и атом водорода—NH-группы находятся относительно пептидной связи в транс-положении (рис. 7-4). Исходя из всех этих исследований, они заключили, что С—N-связи, составляющие одну треть всех связей полипептидного остова, не допускают свободного вращения и имеют частично характер двойных связей. Таким образом, остов полипептидной цепи можно представить в виде ряда жестких плоскостей, разделенных замещенными метиленовыми группами (—CHR—), как показано на рис. 7.5. Теперь нам ясно, что жесткие пептидные связи накладывают некоторые ограничения на число возможных пространственных конформаций полипептидной цепи.
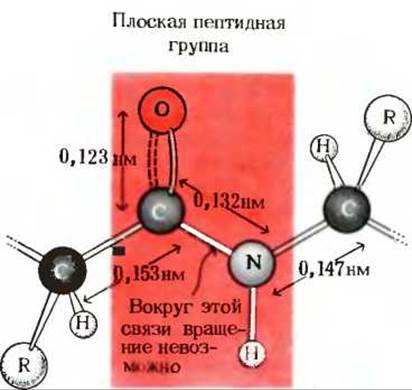
Рис. 7-4. Плоская пептидная группа.
С—N-связь частично имеет характер двойной связи и поэтому вокруг нее свободное вращение невозможно. Обратите внимание, что атомы кислорода и водорода лежат в этой плоскости по разные стороны от С—N-связи. Это соответствует транс-конфигурации пептидной связи.