Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Глобулярные белки: структура и функция гемоглобина
По своей третичной структуре а- и ß-цепи гемоглобина очень сходны с миоглобином
Рентгеноструктурный анализ и химические исследования гемоглобина выявили ряд важных закономерностей. Прежде всего, было обнаружено, что а- и ß-цепи гемоглобина имеют почти одинаковую третичную структуру. Обе они более чем на 70% состоят из а-спиралей, причем все эти а-спиральные участки почти одинаковы по длине и образуют в местах изгибов примерно одни и те же углы.
Вторая закономерность состоит в том, что гемоглобины у разных видов позвоночных характеризуются приблизительно одинаковой третичной структурой их полипептидных цепей. Более того, они очень сходны и по четвертичной структуре.
Третий важный вывод заключается в том, что третичная структура а- и ß-цепей гемоглобина имеет много общего с третичной структурой миоглобина. Сходство третичной структуры этих двух белков можно сопоставить с присущей обоим белкам способностью связывать кислород, лежащей в основе их биологической функции.
О принадлежности миоглобина и цепей гемоглобина к одному семейству белков свидетельствует также сравнение аминокислотных последовательностей миоглобина кашалота и а- и ß-цепей гемоглобина лошади. Как показано на рис. 8-11, во всех трех цепях имеются 27 эквивалентных положений, в которых находятся идентичные аминокислотные остатки; кроме того, в других 40 положениях обнаруживаются близкие по своим свойствам остатки аминокислот, например аспарагиновая и глутаминовая кислоты, или изолейцин и валин. Таким образом, и здесь мы видим, что в аминокислотных последовательностях гомологичных белков имеется ряд инвариантных аминокислотных остатков и что для гомологичных белков характерно сходство их трехмерной структуры.
Из структурных данных по миоглобину и гемоглобину вытекает еще один вывод. Представляется весьма вероятным, что миоглобин и гемоглобин произошли от одного и того же предкового кислород-связывающего гемопротеина (рис. 8-12), который скорее всего состоял из одной полипептидной цепи. В какой-то момент последующей эволюции видов ген, кодировавший предковый кислород-связывающий белок, подвергся дупликации. Образовавшиеся при этом две копии гена далее стали мутировать независимо друг от друга, так что одна из них постепенно превратилась в ген, кодирующий белок миоглобинового типа, приспособленный для запасания кислорода в клетках, а вторая, изменившись в результате другой серии мутаций, стала кодировать а- и ß-цепи гемоглобина, приспособленные для переноса кислорода, осуществляемого эритроцитами. Мы еще встретим немало других примеров функционально и структурно сходных белков, происшедших в процессе эволюции от общих предшественников.
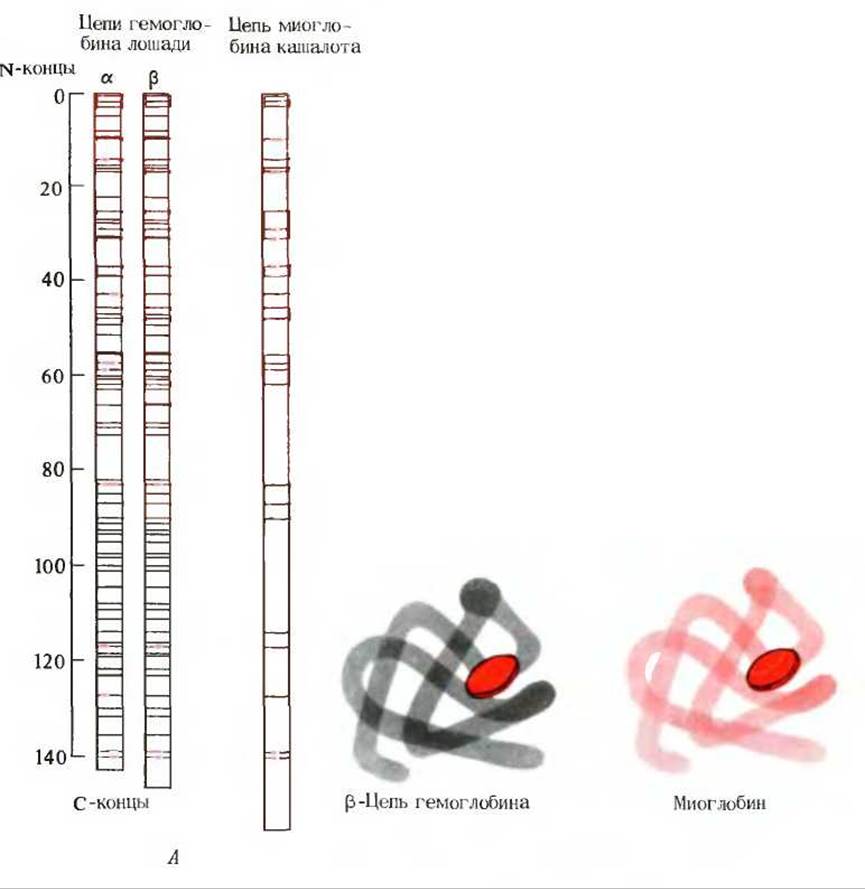
Рис. 8-11. А. Положение инвариантных аминокислотных остатков (красные черточки), общих для а- и ß-цепей гемоглобина лошади и миоглобина кашалота. Черными черточками показаны положения, занятые идентичными аминокислотными остатками в а- и ß-цепях гемоглобина. Б. Сходство третичных структур ß-цепи гемоглобина лошади и миоглобина кашалота. Красный диск гемогруппа.