Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Ферменты
Ферменты ускоряют химические реакции, снижая энергию активации
Ферменты-это истинные катализаторы. Они значительно повышают скорость строго определенных химических реакций, которые в отсутствие фермента протекают очень медленно. Ферменты не могут влиять на положение равновесия ускоряемых ими реакций, при этом в ходе реакций они не расходуются и не претерпевают необратимых изменений.
Каким образом катализаторы, в частности ферменты, повышают скорость химических реакций? Прежде всего мы должны вспомнить о том, что в любой популяции молекул индивидуальные молекулы при постоянной температуре сильно различаются по количеству содержащейся в них энергии и что распределение общей энергии между молекулами описывается колоколообразной кривой. Одни молекулы обладают высокой энергией, а другие более низкой, но в большинстве из них содержится количество энергии, близкое к среднему значению. Химическая реакция типа А→Р протекает потому, что в любой момент времени некоторая доля молекул А обладает большей внутренней энергией по сравнению с другими молекулами данной популяции, и этой энергии оказывается достаточно для достижения ими вершины энергетического барьера (рис. 9-3) и перехода в активную форму, называемую переходным состоянием. Энергией активации называется количество энергии в калориях, необходимое для того, чтобы все молекулы I моля вещества при определенной температуре достигли переходного состояния, соответствующего вершине энергетического (активационного) барьера. В этой точке существует равная вероятность того, что достигшие ее молекулы вступят в реакцию с образованием продукта Р или вернутся обратно на уровень непрореагировавших молекул А (рис. 9-3). Скорость любой химической реакции пропорциональна концентрации молекул, находящихся в переходном состоянии. Следовательно, скорость химической реакции будет очень высокой, если на вершине энергетического барьера находится значительная доля молекул А, и очень низкой, если доля таких молекул невелика.
Существуют два основных пути повышения скорости химической реакции. Первый путь повышение температуры, т.е. ускорение теплового движения молекул, которое приводит к увеличению доли молекул, обладающих достаточной внутренней энергией для достижения переходного состояния. Как правило, повышение температуры на 10 С вызывает ускорение химической реакции приблизительно в два раза.
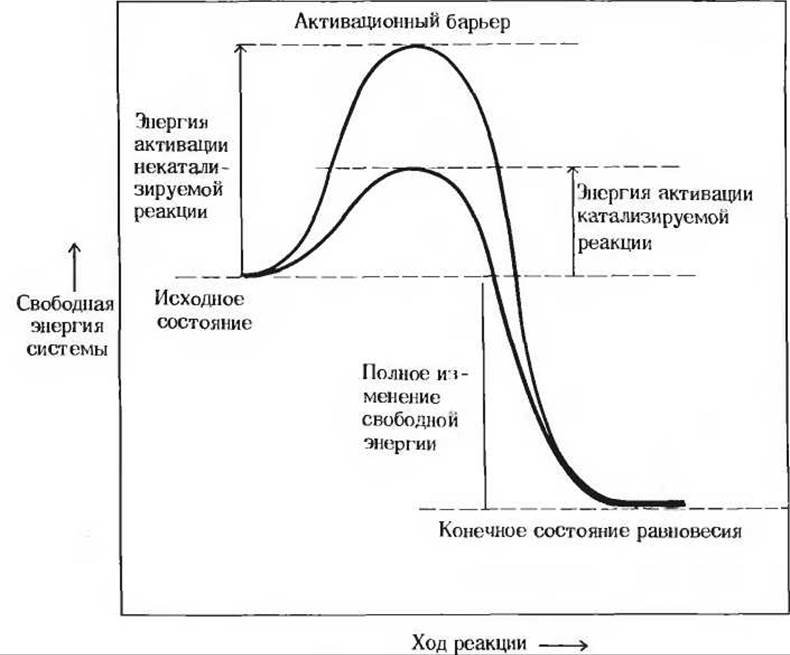
Рис. 9-3. Катализаторы снижают энергию активации (энергетический, или активационный, барьер) химических реакций, не влияя при этом на полное изменение свободной энергии в ходе реакции и на конечное состояние равновесия. Вершина энергетического барьера соответствует переходному состоянию.
Второй путь ускорения химической реакции добавление катализатора. Катализаторы ускоряют химические реакции, находя «обходные пути», позволяющие молекулам преодолевать активационный барьер на более низком энергетическом уровне. Катализатор (обозначим его буквой С) на промежуточной стадии реакции взаимодействует с реагентом А с образованием нового комплекса или соединения СА, переходному состоянию которого соответствует значительно более низкая энергия активации по сравнению с переходным состоянием реагента А в некатализируемой реакции (рис. 9-3). Затем комплекс реагент - катализатор (СА) распадается на продукт Р и свободный катализатор, который может опять соединиться с другой молекулой А и повторить весь цикл. Именно таким образом катализаторы снижают энергию активации химической реакции; в их присутствии гораздо более значительная доля молекул данной популяции вступает в реакцию в единицу времени. Ферменты, так же как и другие катализаторы, соединяются с своими субстратами в ходе каталитического цикла.