Основы биохимии Том 1 - А. Ленинджер 1985
Биомолекулы
Вода
Почти все аминокислоты содержат асимметрический атом углерода
Как следует из рис. 5-2, все стандартные аминокислоты, кроме одной, содержат в a-положении асимметрический атом углерода, с которым связаны четыре разные замещающие группы: карбоксильная группа, аминогруппа, R-группа и атом водорода. Таким образом, асимметрический a-атом углерода является хиральным центром (разд. 3.5). Как мы знаем, соединения с хиральным центром встречаются в двух разных изомерных формах, у которых одинаковы все химические и физические свойства, за исключением одного - направления вращения плоскости поляризации проходящего через них плоскополяризованного света; угол поворота плоскости поляризации измеряют при помощи поляриметра (разд. 3.5). Если не считать глицина, не имеющего асимметрического атома углерода (рис. 5-3), все остальные 19 аминокислот, образующиеся при гидролизе белков в достаточно мягких условиях, обладают оптической активностью, т.е. способны вращать плоскость поляризации света в том или ином направлении. Благодаря тому что в аминокислотах валентные связи вокруг а-атома углерода имеют тетраэдрическое расположение, четыре различные замещающие группы могут располагаться в пространстве двумя разными способами, так что молекула может существовать в двух конфигурациях, представляющих собой несовместимые зеркальные отображения друг друга (рис. 5-4). Эти две формы молекулы называются оптическими изомерами, энантиометрами или стереоизомерами. Раствор одного стереоизомера данной аминокислоты вращает плоскость поляризации света влево (против часовой стрелки); такой стереоизомер называется левовращающим изомером [перед его названием ставят знак (—)]. Другой стереоизомер поворачивает плоскость поляризации света точно на такой же угол, но вправо (по часовой стрелке) и называется правовращающим изомером [в этом случае впереди ставят знак (+)]. Эквимолярная смесь (+)- и (—)-форм не способна вращать плоскость поляризации света. Поскольку все аминокислоты (за исключением глицина), выделенные из белков в мягких условиях, вращают плоскость поляризации света, ясно, что в составе белковых молекул они присутствуют только в какой-либо одной стереоизомерной форме.
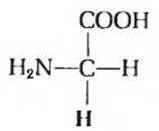
Рис. 5-3. Глицин, единственная аминокислота, у которой нет асимметрического атома углерода. R-группа, представляющая собой атом водорода, выделена красным цветом.
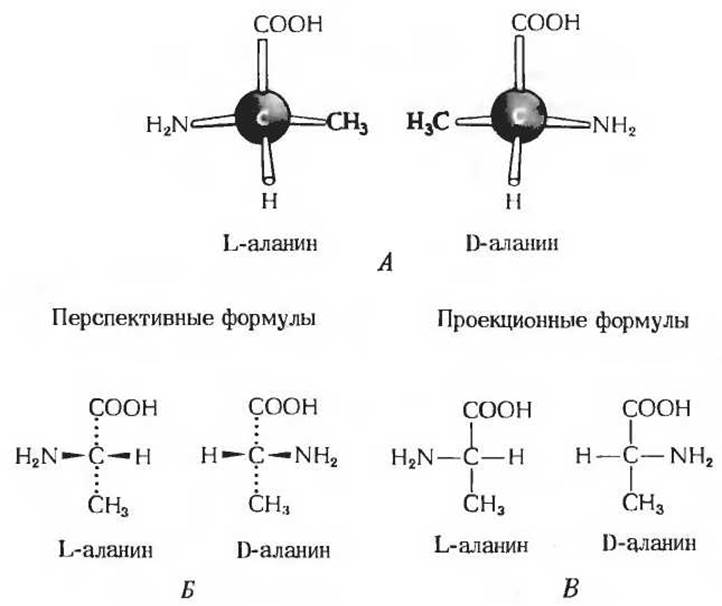
Рис. 5-4. А. Два оптических изомера аланина. Карбоксильные группы, представляющие собой точки отсчета, расположены на конце связи, идущей от хирального центра по вертикали. Структуры L- и D-аланина - это несовмещающиеся зеркальные отражения друг друга. Б и В. Два разных способа изображения пространственной конфигурации оптических изомеров. В перспективных формулах связи, выступающие над плоскостью рисунка, изображаются в виде клиньев, а связи, уходящие за плоскость рисунка, обозначаются пунктиром. В проекционных формулах предполагается, что горизонтальные связи выступают над плоскостью рисунка, а вертикальные - уходят за его плоскость. Правда, проекционным формулам далеко не всегда придают строгий смысл и пользуются ими вне всякой связи со стереохимической конфигурацией молекулы.
Оптическая активность стереоизомера количественно выражается величиной удельного вращения, которую можно определить, измерив угол поворота плоскости поляризации при прохождении света через раствор чистого стереоизомера с известной концентрацией в кювете поляриметра при заданной длине пути света в растворе:

Таблица 5-2. Удельное вращение некоторых аминокислот, выделенных из белков
Все эти аминокислоты имеют L-конфигурацию, но одни из них правовращающие, а другие - левовращающие.
|
Аминокислота |
Удельное вращение, [а]D |
|
L-аланин |
+ 1,8 |
|
L-аргинин |
+ 12,5 |
|
L-гистидин |
- 38,5 |
|
L-глутаминовая кислота |
+ 12,0 |
|
L-изолейцин |
+ 12,4 |
|
L-лизин |
+ 13,5 |
|
L-пролин |
- 86,2 |
|
L-серин |
- 7,5 |
|
L-треонин |
- 28,5 |
|
L-фенилаланин |
- 34,5 |
Длину оптического пути выражают в дециметрах и обязательно указывают температуру и длину волны используемого света (обычно это D-линия в спектре натрия, λ = 589 нм). В табл. 5-2 приведены значения удельного вращения для нескольких аминокислот; обратите внимание, что среди них есть как левовращающие, так и правовращающие.