Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Биосинтез липидов
Малонил-СоА образуется из ацетил-СоА
Непосредственным предшественником большей части двухуглеродных фрагментов в ходе биосинтеза жирных кислот служит малонил-СоА; однако сам он образуется из ацил-СоА в цитозоле. В цитоплазму ацетил-СоА попадает из митохондрий. Давайте последовательно проследим этапы образования малонил-СоА.
Почти весь подвергающийся метаболизму ацетил-СоА образуется в митохондриях в результате окисления пирувата (гл. 16) и жирных кислот (гл. 18), а также при расщеплении углеродных скелетов аминокислот (гл. 19). Однако, как мы уже знаем, (разд. 18.2), митохондриальная мембрана непроницаема для ацетил-СоА. Как же в таком случае митохондриальный ацетил-СоА может служить источником цитоплазматического ацетил-СоА? Эта проблема решается в клетке при помощи челночного механизма переноса ацильных групп через митохондриальную мебрану (рис. 21-3). В этой челночной системе внутримитохондриальный ацетил-СоА сначала реагирует с оксалоацетатом, образуя цитрат, т.е. происходит, по существу, первая реакция цикла лимонной кислоты, катализируемая цитрат-синтазой (разд. 16.5).
Ацетил-СоА + Оксалоацетат +
+ Н2О → Цитрат + СоА + Н+.
Образовавшийся цитрат переносится через внутреннюю мембрану митохондрий из матрикса в цитозоль при помощи специальной трикарбоксилат-транспортирующей системы (разд. 17.19). Далее цитрат реагирует с находящимся в цитозоле СоА и АТР, образуя цитозольный ацетил-СоА. Эта реакция катализируется АТР-цитрат-лиазой (называемой также цитратрасщепляющим ферментом).
Цитрат + АТР + СоА →
→ Ацетил-СоА + ADP + Рi +
+ Оксалоацетат.
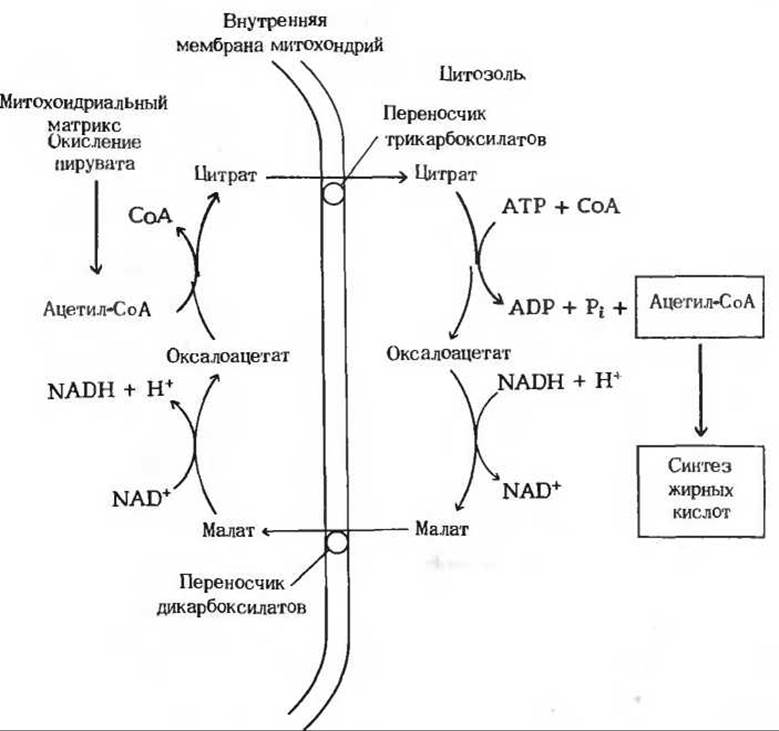
Рис. 21-3. Челночный механизм переноса ацетильных групп из митохондрий в цитозоль, функционирующий в процессе синтеза жирных кислот. Красным цветом выделена последовательность реакций, в ходе которых ацетильные группы в виде цитрата выходят из митохондрий в цитозоль, где используются в форме ацетил-СоА для синтеза жирных кислот. Черные стрелки показывают, каким образом челночный цикл замыкается в результате регенерации митохондриального оксалоацетата.
Возникший в хоре реакции оксалоацетат как таковой не может попасть обратно внутрь митохондрий. Он восстанавливается под действием цитозольной малатдегидрогеназы до малата, который при помощи дикарбоксилат-транспортирующей системы возвращается в митохондриальный матрикс, где вновь окисляется до оксалоацетата, завершая челночный цикл.
Образовавшийся в цитозоле ацетил-СоА подвергается карбоксилированию, в результате чего образуется малонил-СоА - непосредственный предшественник 14 из 16 углеродных атомов в молекуле пальмитиновой кислоты. Эту необратимую реакцию (рис. 21-4) катализирует ацетил-СоА—карбоксилаза:
АТР + Ацетил-СоА + СO2 + Н2O →
→ Малонил-СоА + ADP + Рi + Н +
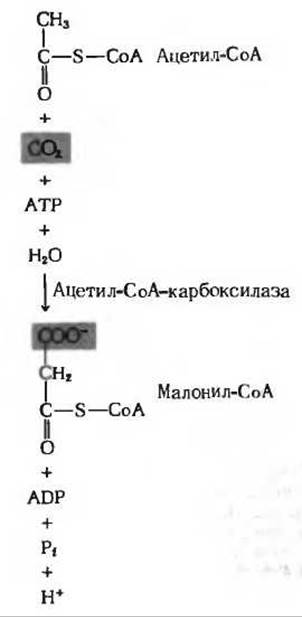
Рис. 21-4. Ацетил-СоА-карбоксилазная реакция. Роль переносчика СО, играет биотин, входящий в состав простетической группы фермента. Строение биотина и биоцитина показано на рис. 10-11.
Участвующий в реакции СO2 образует свободную карбоксильную группу малонил-СоА. Ацетил-СоА-карбоксилаза - очень сложный фермент, который в качестве простетической группы содержит биотин (разд. 10.9), ковалентно связанный амидной связью с ε-аминогруппой лизинового остатка одной из четырех субъединиц молекулы фермента. Биотиновая группа служит как бы «подвижной рукой», осуществляющей перенос СО, на ацетил-СоА:

Присоединение новой карбоксильной группы к ацетил-СоА и необратимость реакции обеспечиваются за счет энергии АТР.
Ацетил-СоА—карбоксилаза - регуляторный фермент; катализируемая этим ферментом реакция является лимитирующим этапом, определяющим скорость всего процесса биосинтеза жирных кислот в животных тканях. Главным положительным модулятором этого фермента служит цитрат, инициирующий переход фермента в высокоактивный нитевидный полимер. Как только содержание цитрата в митохондриях увеличивается, что наблюдается при высокой скорости образования митохондриального ацетил-СоА и АТР, цитрат выходит из митохондрий и выступает одновременно в роли предшественника цитозольного ацетил-СоА и аллостерического активатора ацетил-СоА—карбоксилазы.