Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Биосинтез аминокислот и нуклеотидов
Фиксация азота - сложный ферментативный процесс
В фиксации азота роль катализатора играет ферментный комплекс - нитрогеназная система, действие которой изучено еще не до конца. Нитрогеназная система нестабильна и быстро инактивируется при соприкосновении с атмосферным кислородом; поэтому ее трудно выделить в активной форме и она плохо поддается очистке. Первым стабильным продуктом фиксации азота считается аммиак (NH3). Таким образом, весь процесс в целом сводится, как полагают, к восстановлению молекулярного азота (N2) до двух молекул аммиака
N2 + 3Н2 → 2NH3
∆G0' = -8,0 ккал/моль.
Поскольку изменение стандартной свободной энергии при этой реакции выражается большой отрицательной величиной, реакция при стандартных условиях должна идти слева направо. Однако молекулярный азот - довольно инертный газ, и два его атома соединены очень прочной связью, так что для его восстановления в аммиак требуется очень большая энергия активации. Нитрогеназная система преодолевает этот активационный барьер (разд. 9.4) каким-то нам пока не известным способом.
Донором водорода для нитрогеназного комплекса является в конечном счете NADPH. Сначала восстановительные эквиваленты передаются от NADPH на ферредоксин. Этот белок, содержащий железо и серу, служит непосредственным донором восстановительных эквивалентов при восстановлении азота. В состав его молекулы входят семь атомов железа и такое же число атомов кислотолабильной серы. Молекулярная масса ферредоксина равна 6000. От ферредоксина восстановительные эквиваленты передаются нитрогеназному комплексу, который состоит из двух металлсодержащих ферментов: в состав одного из них входит железо, а в состав другого - железо и молибден (рис. 22-28). Для фиксации азота требуется также АТР, гидролизующийся до ADP и фосфата. Точное назначение этого АТР неизвестно, поскольку никаких фосфорилированных промежуточных продуктов обнаружить не удалось. Предполагается, что свободная энергия гидролиза АТР помогает преодолеть высокий активационный барьер. Вполне вероятно, что на каждую молекулу N2, восстановленную до двух ионов NH+4, гидролизуются 12 молекул АТР до ADP и Pі. Если это так, то суммарное уравнение фиксации азота имеет вид
N2 + 3NADPH + 5Н+ +
+ 12АТР + 12Н2О →
→ 2NH+4 + 3NADP+ + 12ADP + 12Рі.
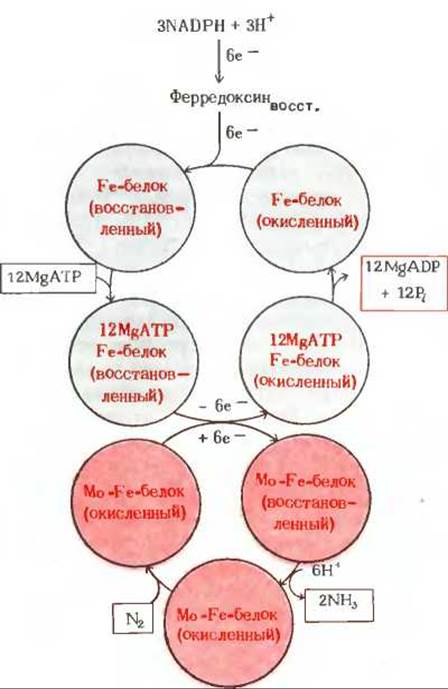
Рис. 22-28. Гипотетический ход нитрогеназной реакции. Предполагается, что в активных центрах этих ферментов протекает ряд промежуточных этапов процесса.
Нитрогеназная система обладает одним интересным свойством, которое делает возможным количественное изучение фиксации азота в интактных растениях. Нитрогеназа катализирует не только восстановление N2, но и восстановление ацетилена (НС=СН) до этилена (Н2С=СН2). Поскольку соотношение этилена и ацетилена в атмосфере можно измерить физическими методами, имеется возможность определять активность нитрогеназы в любых системах растение - почва в экспериментальной теплице, вводя в газовую фазу ацетилен и измеряя скорость образования этилена.
Изучению нитрогеназной системы посвящено очень большое число экспериментальных исследований, что следует объяснить ее огромным практическим значением. В промышленности аммиак для удобрений получают путем каталитического восстановления атмосферного азота по способу, предложенному Габером. Эта реакция
N2 + 3Н2 → 2NH3
требует очень высокой температуры и высокого давления. Если бы удалось воспроизвести нитрогеназную реакцию, используя более простой набор дешевых катализаторов, то это дало бы возможность организовать сравнительно недорогое производство таких удобрений, как растворимые аммониевые соли, что особенно важно для развивающихся стран, которым энергоемкий процесс Габера не по средствам.
Испытываются также и биологические подходы, с помощью которых можно было бы сделать атмосферный азот более доступным. Была, например, предпринята попытка определить, нельзя ли заселить различными видами азотфиксирующих бактерий или какими-нибудь их мутантами обычные небобовые культурные растения, в частности кукурузу, и таким путем создать новые полезные симбиотические ассоциации. Попутно обнаружилось, что в корнях ряда небобовых растений тропических стран тоже обитают азотфиксирующие бактерии. К сожалению, таким растениям для фиксации азота требуется очень теплая почва; если выращивать их в умеренной зоне, то фиксации азота не происходит.
Другой подход заключается в том, чтобы выделить бактериальную ДНК, кодирующую нитрогеназную систему, и ввести ее в геном микроорганизмов, не имеющих нитрогеназы, или в геном растений. Такой перенос генов из азотфиксирующих бактерий в нефиксирующие, в частности в Е. coli, удалось осуществить. Гораздо труднее добиться включения нитрогеназной ДНК в геном высших растений и заставить ее в этом геноме «работать». Однако методы генетической инженерии постепенно совершенствуются, а значит, и эту задачу со временем, быть может, удастся решить.