Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Перенос электронов, окислительное фосфорилирование и регуляция синтеза АТР
Краткое содержание главы
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, способность донора электронов (восстановителя) отдавать электроны характеризуется стандартным восстановительным потенциалом Е'0. Окислительно-восстановительные системы, обладающие более электроотрицательными значениями Е'0, стремятся передать свои электроны системам с более электроположительными значениями E'0. Изменение стандартной свободной энергии в окислительно-восстановительных реакциях определяется из уравнения ∆G0' = -nF∆E'0. В митохондриях атомы водорода, отщепленные от субстратов дегидрогеназами, передают свои электроны в цепь переноса электронов. Переходя по этой цепи от одного переносчика к другому, электроны в конечном итоге достигают молекулярного кислорода и восстанавливают его в Н2O. Энергия, высвобождающаяся в процессе переноса электронов, используется для окислительного фосфорилирования ADP в АТР. Окислительное фосфорилирование протекает во внутренней митохондриальной мембране.
От всех NAD-зависимых реакций дегидрирования восстановительные эквиваленты переходят к митохондриальной NADH-дегидрогеназе, содержащей в качестве простетической группы FMN. Затем через ряд железо-серных центров они передаются на убихинон, который передает электроны цитохрому b. Далее электроны переходят последовательно на цитохромы с1 и с, а затем на цитохром аа3 (цитохромоксидазу), которая содержит медь. Цитохромоксидаза передает электроны на O2. Для того чтобы полностью восстановить O2 с образованием двух молекул Н2O, требуются четыре электрона и четыре иона Н+. Перенос электронов блокируется в определенных точках ротеноном, антимицином А и цианидом. Процесс переноса электронов сопровождается значительным снижением свободной энергии. В трех участках дыхательной цепи происходит запасание энергии в результате синтеза АТР из ADP и Pi. Окислительное фосфорилирование и перенос электронов можно разобщить, воспользовавшись для этого разобщающими агентами или ионофорами, такими, как валиномицин. Для того чтобы могло происходить окислительное фосфорилирование, внутренняя митохондриальная мембрана должна сохранять свою целостность и должна быть непроницаемой для ионов Н+ и некоторых других ионов. Перенос электронов сопровождается «выталкиванием» ионов Н+ из митохондрий. Согласно хемиосмотической гипотезе (одной из трех гипотез, предложенных для объяснения механизма окислительного фосфорилирования), перенос электронов создает между двумя сторонами внутренней митохондриальной мембраны градиент концентрации ионов Н+, при котором их концентрация снаружи выше, чем внутри. Предполагается, что именно этот градиент служит движущей силой синтеза АТР, когда ионы Н+, возвращающиеся из цитозоля в матрикс, проходят через молекулы F0F1-ATPaзы в мембране. Во внутренней митохондриальной мембране имеются транспортные системы для адениновых нуклеотидов, фосфата и ряда метаболитов. Перенос электронов тормозится при понижении концентрации ADP и ускоряется, когда концентрация ADP возрастает благодаря тем или иным клеточным процессам, сопровождающимся утилизацией АТР. Скорости гликолиза, цикла лимонной кислоты и процесса окислительного фосфорилирования согласованы между собой. Эта согласованность обеспечивается взаимосвязанными регуляторными механизмами, которые реагируют на величину отношения [ATP]/[ADP] [Pi] и на содержание некоторых наиболее важных метаболитов, отражающих энергетическое состояние клеток.
В клетках протекают также окислительные реакции, в процессе которых атомы кислорода включатся в органические молекулы, прежде всего в относительно гидрофобные молекулы различных чужеродных веществ и лекарственных препаратов с образованием гидроксилированных и карбоксилированных продуктов.
ЛИТЕРАТУРА
Общие сводки
Dickerson R. Е. Cytochrome с and the Evolution of Energy Metabolism, Sci. Am., 242, 137-153, March (1980).
Hinkle P., McCarty R E. How Cells Make ATP.
Sci. Am., 2.38, 104-123, March (1978). Whittaker D. A., Danks S.M. Mitochondria: Structure, Function and Assembly, Longman, London, 1978. Краткий, написанный на современном уровне обзор. Материал ясно изложен и хорошо иллюстрирован. Прекрасное руководство для общего ознакомления с вопросом.
История вопроса и общие сведения
Keilin D. The History of Cell Respiration and Cytochromes, Cambridge University Press, London, 1966.
Lehninger A.L. The Mitochondrion: Molecular Basis of Structure and Function, Benjamin, New York, 1965. (Имеется перевод: Ленинджер А. Митохондрия. Молекулярные основы структуры и функции.-М.: Мир, 1966.) Митохондрии как силовые станции клетки.
Racker Е. A. New Look at Mechanisms in Bioenergetics, Academic, New York, 1976. (Имеется перевод: Рэкер Э. Биоэнергетические механизмы: новые взгляды,- М.: Мир, 1979.) Отчет о собственных исследованиях с забавными комментариями.
Механизм окислительного фосфорилирования
Boyer P.D., Chance В., Ernster L., Mitchell Р., Racker E., Slater E. C. Oxidative Phosphorylation and Photophosphorylation, Ann. Rev. Biochem., 46, 955-1026 (1977). Различные представления о механизме окислительного фосфорилирования в изложении ведущих исследователей, работающих в этой области.
Mitchell Р. Kellin's Respiratory Chain Concept and Its Chemiosmotic Consequences, Science, 206, 1148-1159 (1979). Речь при вручении Нобелевской премии, в которой вкратце рассказано о том, как создавалась хемиосмотическая гипотеза.
Tedeschi Н. Mitochondria: Structure, Biogenesis, and Transducing Functions, Springer-Verlag, New York, 1976. Более подробная сводка.
Специальные темы
Lehninger A. L. Mitochondria and Biological Mineralization Processes: an Exploration. In: E. Quagliariello, F. Palmieri and T. Singer (eds), Horizons in Biochemistry and Biophysics, vol. 4, pp. 1-30, Addison-Wisley, Reading, Mass., 1977. Поскольку митохондрии наряду с фосфатом накапливают и Са2+, они, возможно, служат тем местом, где протекают первые стадии процесса биологического кальцинирования.
Luft R., lrkos D., Palmieri G., Ernster L., Afzelius B. A Case of Severe Hypermetabolism of Non-Thyroid Origin with a Defect in Mitochondrial Respiratory Control: A Correlated Clinical, Biochemical, and Morphological Study, J. Clin. Invest., 41, 1776-1804 (1962). Первый изученный случай нарушения регуляции переноса электронов у человека.
Вопросы и задачи
1. Окислительно-восстановительные реакции. NADH-дегидрогеназиин комплекс митохондриальной цепи переноса электронов катализирует следующие окислительно- восстановительные реакции (Fe3+ и Fe2+ означают здесь атомы железа железо-серных центров, Q - убихинон, QH2 - убихинол и Е - фермент):
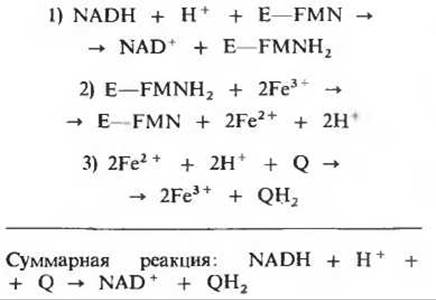
Укажите для каждой из этих трех реакций, катализируемых NADH-дегидрогеназным комплексом: а) донор электронов, б) акцептор электронов, в) сопряженную окислительновосстановительную пару, г) восстановитель и д) окислитель.
2. Стандартные восстановительные потенциалы. Стандартный восстановительный потенциал любой окислительно-восстановительной пары определяется реакцией, протекающей в полуэлементе:
Окислитель + (n)Электроны = Восстановитель.
Стандартные восстановительные потенциалы двух сопряженных пар NAD+/NADH и пируват/лактат равны соответственно -0,32 и -0,19 В.
а) Какая из этих пар обладает большей способностью отдавать электроны? Аргументируйте свой ответ.
б) Какая из них является более сильным окислителем? Почему?
в) В каком направлении пойдет реакция
Пируват + NADH + Н+ = Лактат + NAD+,
если в начальный момент времени концентрации исходных веществ и продуктов равны 1 М при рН7?
г) Чему равно изменение стандартной свободной энергии ∆G0' для этой реакции при 25°С?
д) Чему равна константа равновесия этой реакции при 25°С?
3. Последовательность расположения переносчиков в цепи переноса электронов у одного из растений. Изучение цепи переноса электронов в клетках листьев шпината выявило в этих клетках ряд веществ, способных обратимо присоединять электроны. Ниже приведены стандартные восстановительные потенциалы этих веществ.
|
Восстановленная форма |
Окисленная форма |
Е0', В |
|
Цитохром b6 (Fe2+) |
Цитохром b6 (Fe3+) |
-0,06 |
|
Цитохром f (Fe2+) |
Цитохром f (Fe3+) |
+0,365 |
|
Ферредоксин (восстановленный) |
Ферредоксин (окисленный) |
-0,432 |
|
Ферредоксин-восстанавливающий субстрат (восстановленный) |
Ферредоксин-восстанавливающий субстрат (окисленный) |
-0,60 |
|
Пластоцианин (восстановленный) |
Пластоцианин (окисленный) |
+0,40 |
Укажите вероятную последовательность этих переносчиков электронов в дыхательной цепи, исходя из величин их стандартных восстановительных потенциалов. Составьте энергетическую диаграмму, подобную той, которая изображена на рис. 17-4. На каких этапах переноса выделение свободной энергии (в стандартных условиях) представляется недостаточным для того, чтобы на каждую пару переносимых электронов могла синтезироваться одна молекула АТР?
4. Баланс синтеза АТР, сопряженного с окислением субстрата. Ниже указаны четыре субстрата. Расcчитайтe число молекул АТР, образующихся при полном окислительном расщеплении одной молекулы каждого из этих субстратов до СO2 и Н2O.
а) Фруктозо-6-фосфат
б) Ацетил-СоА
в) Глицеральдегид-3-фосфат
г) Сахароза
5. Энергетический диапазон дыхательной цепи. Перенос электронов в митохондриальной дыхательной цепи описывается следующим суммарным уравнением:
![]()
а) Вычислите величину ∆E0' для этой суммарной реакции митохондриального переноса электронов.
б) Вычислите изменение стандартной свободной энергии ∆G0' для этой реакции.
в) Сколько молекул АТР теоретически может быть синтезировано за счет этой реакции, если изменение стандартной свободной энергии образования АТР равно +7,3 ккал/моль?
6. При окислении сукцината акцептором электронов служит не NAD+, a FAD. На всех этапах, связанных с дегидрированием, в процессе гликолиза и в цикле лимонной кислоты акцептором электронов служит NAD + (E0’ = -0,32 В). Единственным исключением является реакция, катализируемая сукцинатдегидрогеназой, использующей в качестве акцептора электронов ковалентно связанный с ней FAD (E0' = +0,05 В). Почему FAD является более подходящим акцептором электронов, чем NAD+, при дегидрировании сукцината? Предложите возможное объяснение этого факта, исходя из сравнения величин E'0 сукцинат-фумаратной системы, сопряженной пары NAD+ /NADH и пары FAD/FADH2.
7. Степень восстановления переносчиков электронов в дыхательной цепи. Степень восстановления каждого из переносчиков электронов в дыхательной цепи определяется условиями, существующими в митохондриях. Когда NADH и молекулярного кислорода достаточно, соответствующая стационарному состоянию степень восстановления переносчиков снижается при переходе электронов от субстрата на кислород. Если перенос электронов блокирован, то переносчики, занимающие в дыхательной цепи место перед блокированным этапом, становятся более восстановленными, а те, которые располагаются после блока, - более окисленными, как это поясняет гидравлическая модель дыхательной цепи, изображенная на рис. 17-14. Как будут выглядеть такие модели для следующих четырех случаев:
а) Достаточно NADH и O2, но добавлен цианид.
б) Достаточно NADH, но исчерпан запас O2.
в) Достаточно O2, но исчерпан запас NADH.
г) Достаточно и NADH, и O2.
8. Влияние ротенона и антимицина А на перенос электронов. Ротенон (токсичное вещество, вырабатываемое одним из видов растений) резко подавляет активность митохондриальной NADH-дегидрогеназы. Токсичный антибиотик антимицин А сильно ингибирует окисление убихинола.
а) Почему ротенон оказывается смертельным ядом для некоторых насекомых и рыб?
б) Почему антимицин А действует как яд в животных тканях?
в) Допустим, что оба эти вещества блокируют соответствующие участки дыхательной цепи с равной эффективностью. Какое из них будет при этом более мощным ядом? Дайте аргументированный ответ.
9. Разобщающие агенты при окислительном фосфорилировании. В нормальных митохондриях скорость переноса электронов строго согласована с потребностью в АТР. Поэтому если скорость использования АТР сравнительно невелика, то соответственно небольшой оказывается и скорость переноса электронов. Если же АТР расходуется с большой скоростью, то скорость переноса электронов тоже бывает высокой. В подобных условиях (при тесном сопряжении этих двух процессов) отношение P/О, т. е. число образовавшихся молекул АТР, в расчете на один атом потребленного кислорода, когда донором электронов служит NADH, равно приблизительно 3.
а) Как должна влиять относительно низкая и относительно высокая концентрация разобщающего агента на скорость переноса электронов и на величину Р/О?
б) Прием внутрь разобщающих агентов вызывает обильное потоотделение и повышение температуры тела. Дайте этому феномену объяснение на молекулярном уровне. Как изменяется отношение P/О в присутствии разобщающих агентов?
в) 2,4-динитрофенол, который является разобщающим агентом, пытались одно время использовать для борьбы с ожирением. На чем в принципе может быть основано подобное его действие? Теперь такого рода разобщающие агенты уже не применяются в качестве лекарственных препаратов, поскольку известны случаи, когда их применение приводило к летальному исходу. Почему прием разобщающих агентов может вызвать смерть?
10. Механизм действия дициклогексилкарбодиимида (ДЦКД, или DCCD). Если к суспензии активно дышащих митохондрий, в которых дыхание тесно сопряжено с фосфорилированием, добавить DCCD, то наблюдается резкое уменьшение скорости переноса электронов (оцениваемой по количеству поглощенного кислорода) и скорости фосфорилирования (оцениваемой по образованию АТР). Добавив затем к таким ингибированным митохондриальным препаратам 2,4-динитрофенол, мы обнаружим, что потребление кислорода возвращается к нормальному уровню, однако синтез АТР так и остается подавленным.
а) На какой этап процесса переноса электронов или окислительного фосфорилирования влияет DCCD?
б) Почему DCCD нарушает потребление О2 в митохондриях? Каков механизм действия 2,4-динитрофенола на препарат ингибированных митохондрий?
в) С каким из перечисленных ниже ингибиторов более всего сходен по своему действию DCCD: с аитимицином А, ротеноном, олигомицином или арсенатом?
11. Окислительное фосфорилирование в инвертированных субмитохондриальных пузырьках. Согласно хемиосмотической гипотезе, во время переноса электронов из интактных митохондрий «откачиваются» наружу ионы Н+, что приводит к возникновению градиента pH между двумя сторонами митохондриальной мембраны. Этот градиент pH заключает в себе энергию, благодаря которой ионы Н+ перемещаются в обратном направлении - из окружающей среды в митохондриальный матрикс. При этом ионы Н+ проходят через молекулы F0F1-АТРазы, чем обеспечивается синтез АТР из ADP и Рі. Удалось показать, что полученные из внутренней митохондриальной мембраны инвертированные пузырьки, у которых F0F1-АТРазные головки обращены наружу (рис. 17-15), тоже способны к окислительному фосфорилированию.
а) Нарисуйте схему, которая показывала бы направление откачивания ионов Н+ во время переноса электронов в субмитохондриальных пузырьках.
б) Укажите на этой схеме направление потока ионов Н+ через молекулы F0F1-АТРазы во время синтеза АТР.
в) Как будут влиять на перенос электронов и на синтез АТР в таких субмитохондриальных пузырьках олигомицин и атрактилозид?
12. Митохондрии бурого жира. У новорожденных детей в области шеи и в верхней части спины имеется особая жировая ткань, которая у взрослых практически отсутствует, - так называемый бурый жир. Бурую окраску придают этой ткани митохондрии, которых в ней чрезвычайно много. У некоторых животных, впадающих в зимнюю спячку или приспособленных к обитанию в холодных местностях, тоже имеется бурый жир. В то время как в митохондриях печени при окислении NADH на каждый атом поглощенного кислорода образуются обычно три молекулы АТР, в митохондриях бурого жира выход АТР на один атом поглощенного кислорода составляет менее одной молекулы.
а) Какая физиологическая функция может определяться этим низким отношением P/О в буром жире новорожденных?
б) Укажите возможные механизмы, которые могли бы определять столь низкое отношение P/О, характерное для митохондрий бурого жира.
13. Дикарбоксилатная транспортная система митохондрий. Во внутренней митохондриальной мембране имеется дикарбоксилатная транспортная система, которая обеспечивает перенос через мембрану маната и а-кетоглутарата. Эта транспортная система ингибируется н-бутилмалонатом. Предположим, что н-бутилмалонат добавлен к суспензии аэробных почечных клеток, использующих в качестве топлива одну только глюкозу. Как должен подействовать н-бутилмалонат на а) гликолиз, б) потребление кислорода, в) образование лактата и г) синтез АТР?
14. Эффект Пастера. Если в суспензию анаэробных клеток, потребляющих глюкозу с большой скоростью, ввести кислород, то клетки начнут его поглощать и уровень потребления глюкозы резко понизится. Одновременно с этим прекратится накопление лактата. Этот эффект, характерный для клеток, способных и к аэробному, и к анаэробному потреблению глюкозы, впервые наблюдал Луи Пастер в 60-х годах прошлого века, и потому он был назван эффектом Пастера.
а) Почему при введении в клеточную суспензию кислорода прекращается накопление лактата?
б) Почему в присутствии кислорода снижается скорость потребления глюкозы?
в) Каким образом после начавшегося потребления кислорода понижается скорость потребления глюкозы? Объясните это, исходя из специфичного действия ферментов.
15. Изменение энергетического заряда клеток. При изменении физиологической активности клеток скелетных мышц энергетический заряд этих клеток, равный в норме 0,89, сначала резко снижается приблизительно до 0,70, а потом постепенно возвращается к своему обычному уровню.
а) Какое именно изменение активности обусловливает это внезапное уменьшение энергетического заряда? Поясните свой ответ.
б) Как должно повлиять это внезапное изменение на скорость гликолиза и дыхания?
в) Каким образом энергетический заряд способен влиять на гликолиз и дыхание?
16. Сколько ионов Н+ содержится в одной митохондрии? Хемиосмотическая гипотеза предполагает, что в результате переноса электронов ионы Н+ «выталкиваются» из матрикса митохондрий наружу, вследствие чего между двумя сторонами митохондриальной мембраны возникает градиент pH, при котором наружная фаза оказывается более кислой, чем внутренняя. Способность ионов Н+ диффундировать в обратном направлении, из окружающей среды в митохондриальный матрикс (где их концентрация ниже), служит, согласно этой гипотезе, движущей силой для синтеза АТР, катализируемого F0F1-АТРазой. В митохондриях, суспендированных в среде с pH 7,4, происходит окислительное фосфорилирование. Найдено, что pH митохондриального матрикса равен при этом 7,7.
а) Вычислите, чему равны молярные концентрации ионов Н+ в окружающей среде и в матриксе митохондрий для этих условий.
б) Определите отношение концентраций Н+ снаружи и внутри, дающее представление об энергии, которую эта разность концентраций в себе заключает (см. гл. 14).
в) Определите число ионов Н+, приходящееся на одну дышащую митохондрию печени. При этом расчете исходите из предположения, что внутреннее пространство митохондрии представляет собой сферу диаметром 1,5 мкм.
г) Учитывая полученные вами данные, можно ли считать один только этот градиент pH достаточным источником энергии для синтеза АТР?
д) Если, по вашему мнению, одного этого градиента pH недостаточно, то какой другой источник энергии, необходимой для синтеза АТР, могли бы вы указать?