Биохимия человека Том 2 - Марри Р. 1993
Структура, функция и репликация информационных макромолекул
Технология рекомбинантных ДНК
ДНК
В 1944 г. в экспериментах, проведенных Эвери, Маклеодом и Маккарти, было продемонстрировано, что способность к образованию капсулы у мутантного бескапсульного штамма пневмококков может быть восстановлена посредством введения в его клетки очищенной ДНК пневмококков, способных к синтезу капсулы. Авторы назвали агент (ДНК), ответственный за это изменение, — «трансформирующим фактором». Очень скоро метод трансформации стал широко использоваться в генетических исследованиях. Относительно недавно были проведены эксперименты, в которых реципиентами служили клетки дрожжей, млекопитающих, эмбрионы грызунов и насекомых, а донором генетической информации — клонированная ДНК.
Химические свойства ДНК
Химическая природа мономерных единиц, образующих ДНК (дезоксиаденилат, дезоксицитидилат, дезоксигуанилат и тимидилат), описана в гл. 34. Мономеры полимеризуются с образованием 3', 5'-фосфодиэфирных связей, формируя одиночную цепь ДНК (рис. 37. 1). Информация в ДНК записана в виде определенной последовательности пуриновых и пиримидиновых дезоксирибонуклеотидов.
Полимерная молекула ДНК, как видно из рисунка, полярна. На одном конце расположена 5'-гидроксил-(либо фосфатная группа), на другом 3'-фосфат-(либо гидроксильная группа). Основываясь на данных рентгеноструктурного анализа ДНК и правиле Чаргаффа, согласно которому в молекуле ДНК содержание остатков дезоксиаденозина (А) равно содержанию тимидина (Т), а содержание дезоксигуанозина (G) равно содержанию дезоксицитозина (С), Уотсон, Крик и Уилкинс предложили в начале 50-х годов модель двухспиральной структуры ДНК. Модель В-формы ДНК изображена на рис. 37.2. Две цепи этой правозакрученной, двухспиральной молекулы удерживаются друг возле друга за счет водородных связей, образующихся между пуриновыми и пиримидиновыми основаниями. Образование комплементарных пар строго специфично. А всегда спаривается с Т, a G—с С (рис. 37. 3).
В двухцепочечной молекуле ограничения, обусловленные заторможенностью вращения вокруг фосфодиэфирной связи, преимущественная «автоконфигурация гликозидных связей (рис. 34.9) и превалирующие таутомерные формы четырех оснований (A, G, Т и С, рис. 34.3) создают условия, в которых А может образовать прочную пару только с Т, a G только с С (рис. 37.3). Именно этим и объясняются правила Чаргаффа (А = Т; G = С). Две цепи двойной спирали, будучи полярными, являются и антипаралельными, т. е. направление одной цепи 5'→3', а другой 3'→5'. Такая картина напоминает две параллельные улицы с односторонним движением, направленным в противоположные стороны. Одну из двух комплементарных цепей ДНК, содержащую информацию о структуре определенного гена в виде специфической последовательности нуклеотидов, обычно называют кодирующей (или матричной); другая, комплементарная ей цепь носит название некодирующей.
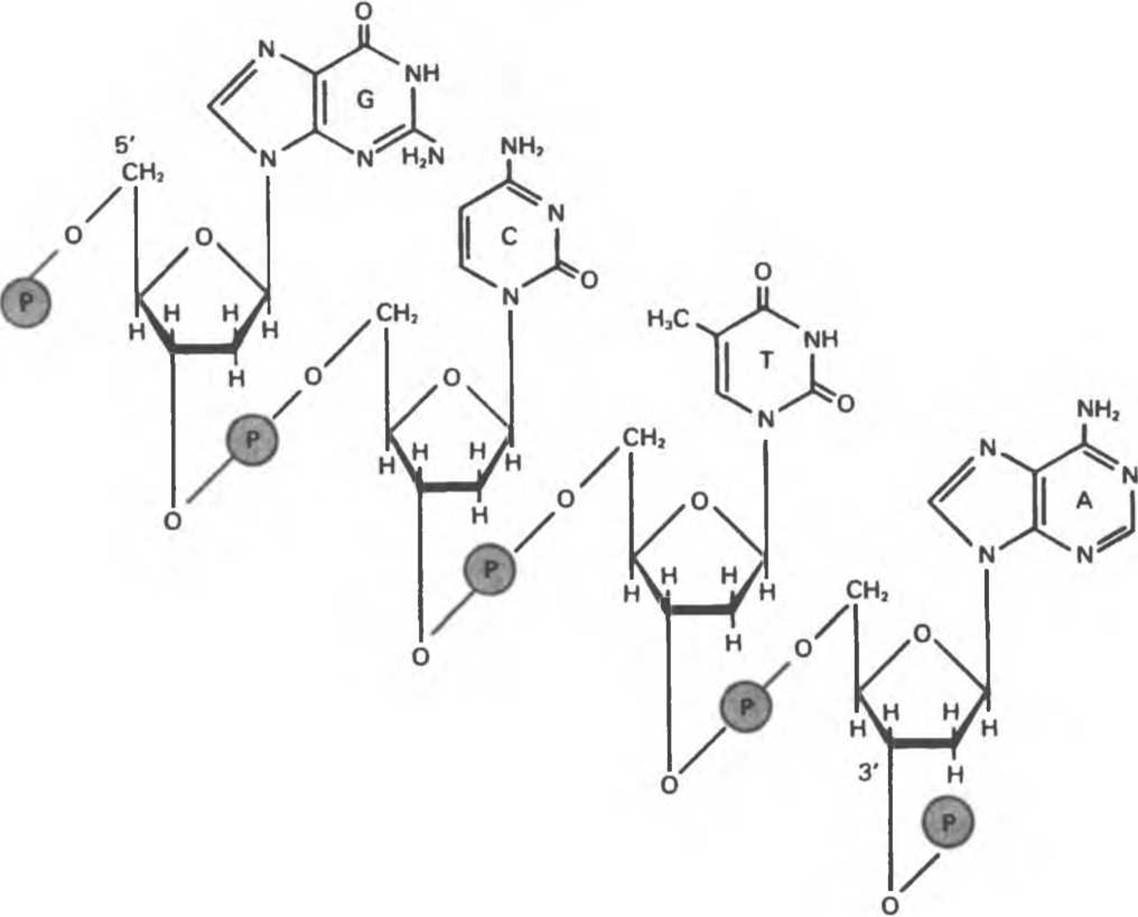
Рис. 37.1. Фрагмент структуры молекулы ДНК, в которой пуриновые и пиримидиновые основания аденин (А), тимин (Т), цитозин (С) и гуанин (G) удерживаются вместе фосфодиэфирным остовом, соединяющим 2'-дезоксирибозильные остатки, связанные N-гликозидной связью с соответствующими нуклеиновыми основаниями. Обратите внимание: фосфодиэфирный остов единичной цепи ДНК обладает «полярностью» (т. е. в нем можно выделить определенное направление, например 5'→3').
Как показано на рис. 37.3, между остатками дезоксигуанозина и дезоксицитидина образуются три водородные связи, а между тимидином и дезоксиаденозином — только две. Поэтому связь G—С прочнее примерно на 50%. Этим обстоятельством, а также стэкинг-взаимодействиями и можно объяснить более высокую температуру денатурации (плавления) G—С-богатых областей ДНК.
Структура ДНК
ДНК может формировать несколько типов двойных спиралей. В настоящее время уже известно шесть форм (от А до Е и Z-форма). Большая часть структурных вариантов ДНК может существовать только в строго контролируемых условиях эксперимента. Эти варианты различаются 1) числом пар оснований, приходящихся на один виток двойной спирали; 2) расстоянием между плоскостями пар оснований и углом, который они образуют с осью спирали; 3) диаметром спирали; 4) направленностью (правая, левая) двойной спирали (табл. 37. 1).
Некоторые из этих форм переходят друг в друга при изменении концентрации соли и степени гидратации. Не исключено, что переходы между различными структурными формами ДНК происходят и in vivo.
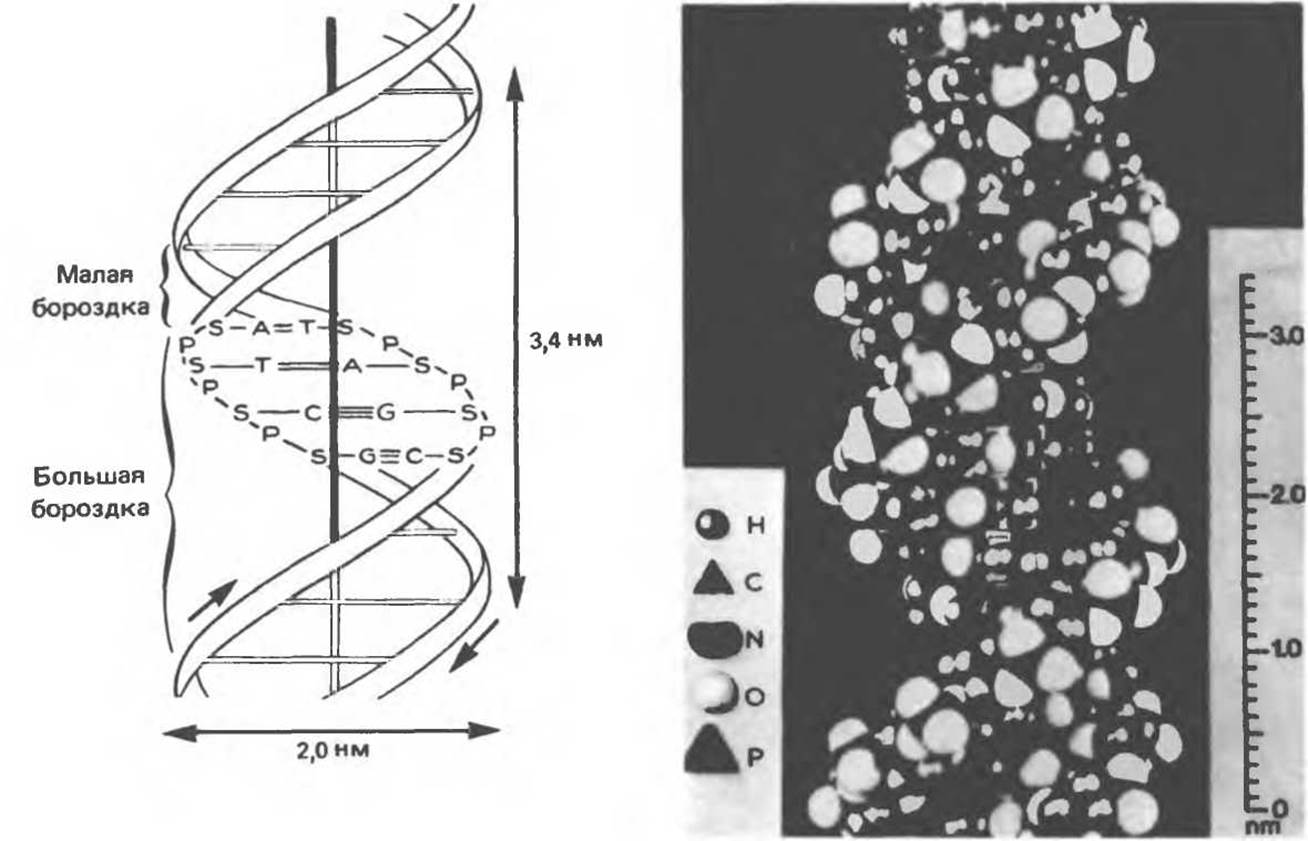
Рис. 37.2. Модель двухспиральной структуры В-формы по Уотсону и Крику. Слева: Схематическое изображение молекулы (А — аденин, С — цитозин, G — гуанин, Т — тимин, Р — фосфат, S — сахар [дезоксирибоза]). Справа: модель структуры ДНК. (Photograph from J. D. Watson, Molecular biology of the Gene 3rd ed. Copyright 1976, 1970, 1965 by W. A. Benjamin, Inc., Menlo Park, Calif.)
При физиологических условиях (низкая концентрация соли, высокая степерь гидратации) доминирующим структурным типом ДНК является В- форма. Шаг спирали такой молекулы равен 3,4 нм. Виток ДНК можно представить в виде двух скрученных стопок «монет», по 10 в каждой. Стопки удерживаются водородными связями между двумя противолежащими «монетами» стопок, и «обмотаны» двумя лентами фосфодиэфирного остова, закрученными в правую спираль. В условиях менее высокой гидратации и при более высоком содержании ионов Na+ или К+ возникает несколько иная структура — так называемая A-форма. Эта правоспиральная конформация имеет больший диаметр спирали, чем В-форма, и большее число пар оснований на виток. Она сходна со структурой, характерной для двухцепочечной РНК или для РНК—ДНК-дуплексов. Формы С—Е также правоспиральные, их образование можно наблюдать только в специальных экспериментах, и, по-видимому, они не существуют in vivo.
Z-форма ДНК представляет собой левозакрученную двойную спираль, в которой фосфодиэфирный остов расположен зигзагообразно вдоль оси молекулы. Отсюда и название молекулы Z (zigzag)-ДHK.
Z-ДНК — наименее скрученная (12 пар оснований на виток) и наиболее тонкая из известных в природе, она обладает только одним желобком (см. ниже). Z-ДНК выявляют в повторяющихся последовательностях чередующихся пуриновых и пиримидиновых дезоксинуклеотидов (GC или АС) при наличии ряда других стабилизирующих факторов. К ним относятся: 1) высокая концентрация соли или наличие специфических катионов, таких, как спермин и спермидин; 2) высокое содержание отрицательных супервитков в молекуле ДНК (см. гл. 38); 3) связывание Z-ДНК-специфичных белков; 4) метилирование атома углерода-5 некоторых остатков дезоксицитидина.
ДНК в Z-форме может участвовать в регуляции экспрессии генов как близко расположенных, так и существенно удаленных от Z-участка. Некоторые белки, связывающиеся в большой или малой бороздках В-формы ДНК, вероятно, не способны связываться с Z-формой ДНК. Кроме того, реверсия участка ДНК из Z-формы в В-форму ДНК, которая происходит, например, в результате потери метильных групп 5-метилдезоксицитидином может влиять на торсионный статус участков ДНК, расположенных на значительном расстоянии от области реверсии.
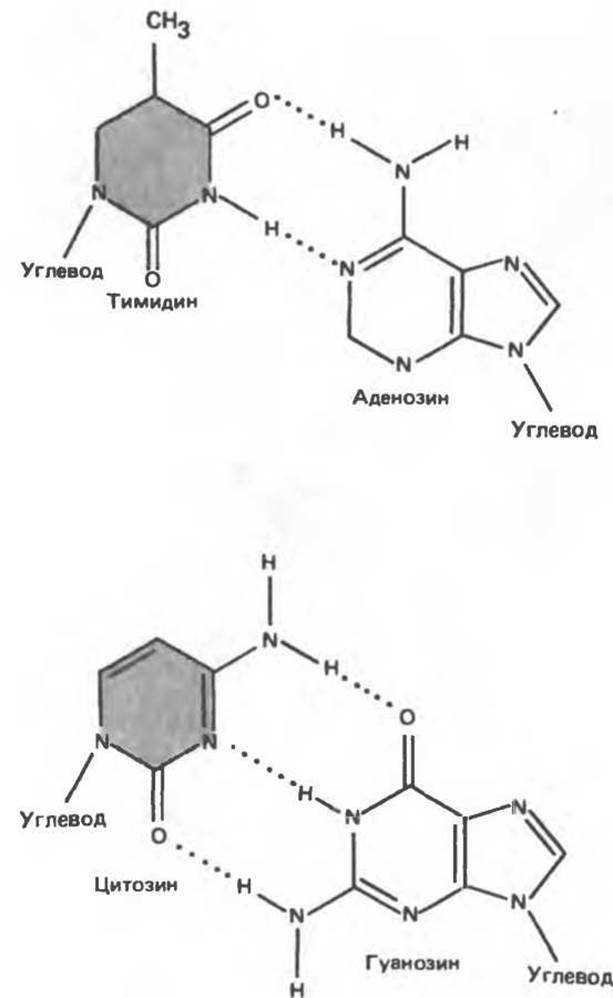
Рис. 37.3. Образование двух водородных связей (пунктирная линия) между основаниями дезоксиаденозина и тимидина (вверху) и трех водородных связей между основаниями дезоксигуанозина и дезоксицитидина (внизу). В ДНК углеводным остатком является 2-дезоксирибоза, в РНК
D-рибоза.
Торсионное скручивание — раскручивание ДНК так же, как и метилирование дезоксицитидина, вероятно, влияет на активность генов (см. ниже).
Наличие Z-ДНК в хромосомах Drosophila (плодовая мушка) было показано с применением антител специфичных к Z-форме ДНК. В ДНК человека имеются участки, потенциально способные переходить в Z-форму; они диспергированы в геноме. Есть основания предполагать, что и в клетках человека могут реализоваться условия, необходимые для стабилизации Z-формы.
Таблица 37.1. Характеристика некоторых типов структур ДНК
|
Тип |
Закрученность спирали |
Число пар оснований на виток |
Расстояние между плоскостями оснований |
Диаметр спирали |
|
А |
Правая |
11 |
0,256 нм |
2,3 нм |
|
В |
Правая |
10 |
0,338 нм |
1,9 нм |
|
Z |
Левая |
12 |
0,371 нм |
1,8 нм |
Денатурация (плавление) ДНК
Двухспиральную структуру ДНК можно «расплавить» в растворе, повышая температуру или понижая концентрацию соли. При плавлении происходит не только расхождение цепей ДНК, но и нарушается система стэкинг-взаимодействий нуклеиновых оснований внутри данной цепи. Фосфодиэфирные связи при этом не разрываются. Денатурация ДНК сопровождается усилением оптического поглощения пуриновых и пиримидиновых оснований. Это явление называют гиперхромным эффектом денатурации ДНК. При денатурации исчезает также высокая вязкость, присущая растворам нативной ДНК, волоконноподобная структура которой обусловлена как стэкинг-взаимодействиями нуклеиновых оснований в каждой цепи, так и комплементарными взаимодействиями между двумя цепями.
Разделение цепей данной молекулы ДНК происходит в пределах определенного интервала температур. Средняя точка этого интервала называется температурой плавления ДНК или Тm. Значение Тm зависит от нуклеотидного состава ДНК и концентрации соли в растворе. Молекулы ДНК, обогащенные G—С-парами (они связаны тремя водородными мостиками), «плавятся» при более высокой температуре, чем А—Т-богатые молекулы (пары А—Т связаны двумя водородными мостиками). Десятикратное увеличение концентрации моновалентных катионов увеличивает Тm на 16,6° С. Формамид, обычно используемый в экспериментах с рекомбинантной ДНК, дестабилизирует водородные связи между основаниями, тем самым снижая Тm. Это позволяет цепям ДНК или ДНК—РНК-гибрида расходиться при более низкой Тm, что уменьшает вероятность разрыва индивидуальных цепей, происходящего при высокой температуре.
Бороздки в структуре ДНК
При изучении модели, изображенной на рис. 37.2, можно обратить внимание на наличие в структуре ДНК большой и малой бороздок, закрученных вокруг оси молекулы параллельно фосфодиэфирному остову. В этих бороздках белки могут специфически взаимодействовать с определенными атомами нуклеиновых оснований, а значит, и «узнавать» конкретные нуклеотидные последовательности, не нарушая комплементарных взаимодействий в структуре двойной спирали. Как будет показано в гл. 39 и 41, именно за счет таких взаимодействий регуляторные белки могут осуществлять контроль экспрессии генов.
Релаксированная и суперспиральная ДНК
ДНК некоторых организмов, таких, как бактерии, бактериофаги и многие ДНК-содержащие вирусы животных, представляет собой замкнутую кольцевую структуру. Конечно, такая структура не нарушает полярность молекул, но в ней исчезают свободные 3'- и 5'-гидроксильные и фосфорильные группы. Замкнутые кольца могут существовать в релаксированной или суперспиральной формах. Суперспиральность проявляется тогда, когда замкнутое кольцо сворачивается вокруг собственной оси или когда скручивается участок линейной ДНК, концы которой зафиксированы. Этот требующий энергии процесс приводит к появлению внутримолекулярного напряжения структуры. При увеличении числа супервитков внутреннее (торсионное) напряжение возрастает (проверьте это на обычной резиновой ленте). Супервитки в ДНК, образованные за счет скручивания против часовой стрелки (в направлении, обратном закручиванию правосторонней двойной спирали В-формы ДНК), называются отрицательными. В некотором смысле можно считать, что энергия, необходимая для достижения такого структурного состояния, запасается в обычных (неотрицательных) супервитках. Энергия перехода молекулы ДНК к другому типу надмолекулярной структуры может понижаться за счет образования участков отрицательного скручивания. Один из таких переходов — разделение цепей при подготовке к репликации и транскрипции. Вот почему суперспирализация ДНК весьма выгодна в биологических системах. Ферменты, катализирующие топологические изменения молекулы ДНК, получили название топоизомераз. Наиболее изучена из них — бактериальная гираза, инициирующая образование отрицательных супервитков.
Функция ДНК
Генетическая информация, закодированная в последовательности нуклеотидов, служит двум целям. Во-первых, она необходима для синтеза белковых молекул, во-вторых, обеспечивает передачу самой себя в ряду клеточных поколений и поколений организмов. Обе функции основаны на том, что молекула ДНК служит матрицей; в первом случае для транскрипции — перекодирования информации в структуру молекул РНК и во втором для репликации — копирования информации в дочерних молекулах ДНК.
Комплементарность цепей двойной спирали Уотсона и Крика предполагает полуконсервативный способ репликации ДНК. Это означает, что цепи расходятся и каждая служит матрицей для синтеза новой комплементарной последовательности (рис. 37.4). Две образовавшиеся двухспиральные молекулы ДНК, каждая из которых состоит из одной родительской и одной вновь синтезированной комплементарной цепи, распределяются между двумя дочерними клетками (рис. 37.5). Таким образом, каждая из дочерних клеток получает информацию, идентичную той, которой обладала родительская клетка. В каждой из двух дочерних клеток сохраняется одна цепь от исходной родительской ДНК.
Полуконсервативный механизм репликации у бактерии Escherichia coli был однозначно продемонстрирован в классическом эксперименте Мезелсона и Сталя с применением тяжелого изотопа азота в сочетании с равновесным центрифугированием.
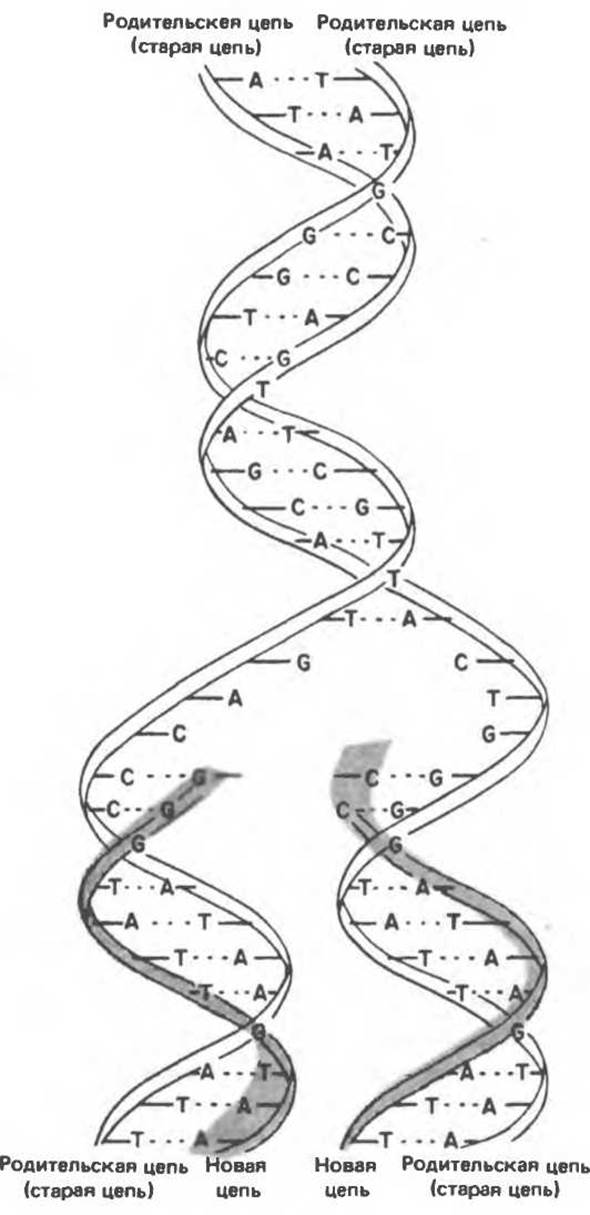
Рис. 37.4. Двухцепочечная структура ДНК. Каждая из двух цепей родительской молекулы ДНК используется в качестве матрицы для синтеза новых комплементарных цепей. (From J. D. Watson. Molecular biology of the Gene 3rd ed. Copyright 1976, 1970, 1965 by W. A. Benjamin, Inc., Menlo Park, Calif.)
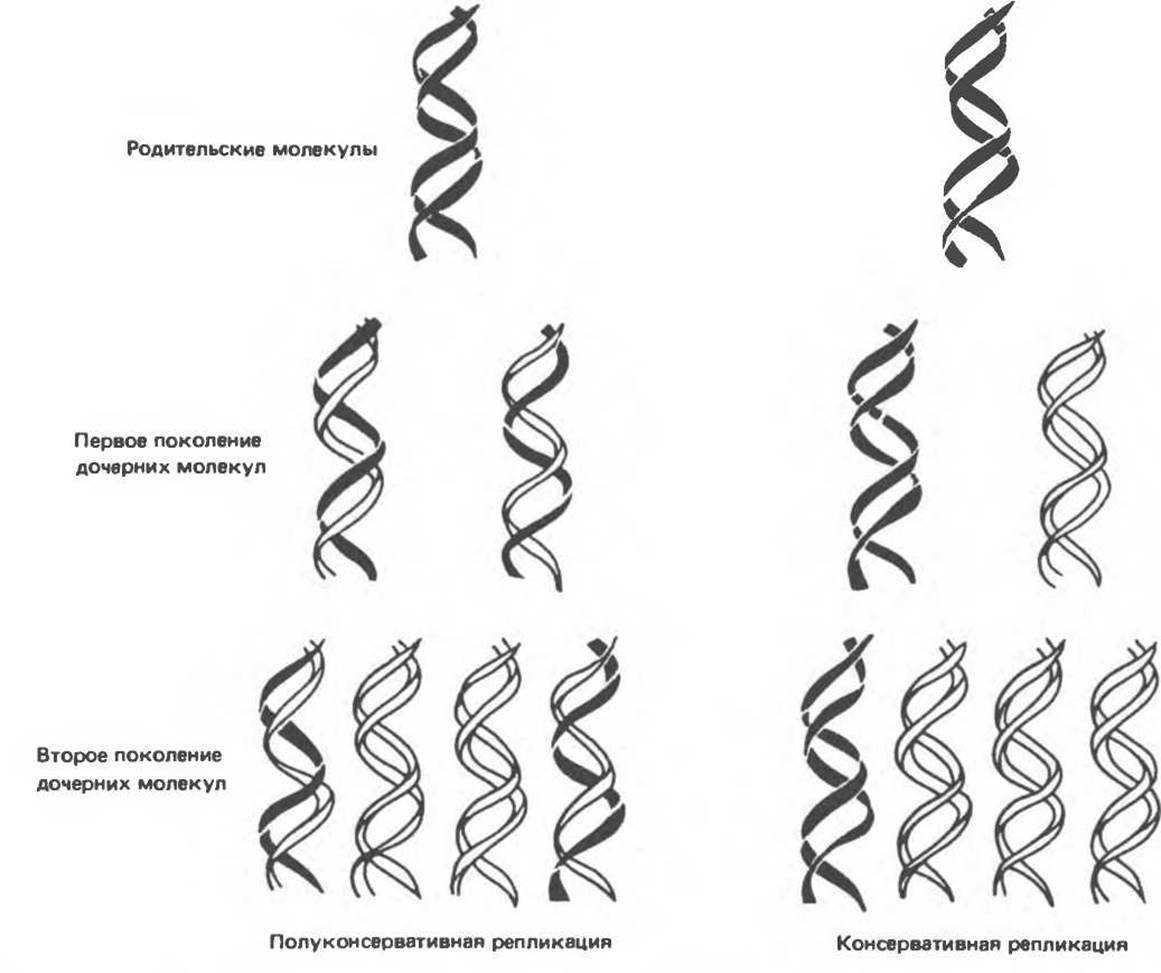
Рис. 37.5. Ожидаемое распределение цепей ДНК при полуконсервативной и консервативной репликациях. На рисунке родительские цепи — черные, а новые цепи — светлые. (Redrawn and reproduced, with permission from Lehninger A. L. Biochemistry 2nd. ed., Worth, 1975.)
ДНК E. coli и ДНК человека химически идентичны, хотя, конечно, последовательности нуклеотидов в них отличаются и, кроме того, клетка человека содержит примерно в 1000 раз больше ДНК, чем бактериальная. Оказалось, что химический механизм репликации ДНК — один и тот же у прокариот, таких, как Е. coli, и эукариот, включая человека, несмотря на то что ферменты, вовлеченные в эти процессы, в клетках прокариот и эукариот различаются. Есть все основания считать, что данные, полученные при изучении химии нуклеиновых кислот прокариотических организмов, приложимы и к эукариотическим системам. Действительно, результаты экспериментов с клетками млекопитающих, аналогичных опытам Мезелсона и Сталя, оказались сопоставимыми с данными, полученными ранее на Е. coli.