Биохимия человека Том 2 - Марри Р. 1993
Биохимия внутри- и межклеточных коммуникаций
Гормоны щитовидной железы
Биосинтез тиреоидных гормонов - Метаболизм иодида
Метаболизм иодида включает ряд отдельных этапов, представленных на рис. 46.2.
Концентрирование иодида (I-)
Щитовидная железа наряду с некоторыми другими эпителиальными тканями, такими, как молочная железа, плацента, слюнные железы и желудок, обладает способностью концентрировать І- против высокого электрохимического градиента. Это требующий энергии процесс, связанный с зависимым от АТРазы Na+/K+-нacocoм. Активность I--насоса щитовидной железы можно оценить отдельно путем ингибирования органификации I- соединениями класса тиомочевины (рис. 46.3). Отношение количества иодида в щитовидной железе к иодиду сыворотки (отношение ЩЖ/С) отражает активность этого насоса (или концентрирующего механизма). Она регулируется в первую очередь тиреотропином (ТТГ), и отношение ЩЖ/С колеблется от 500 у животных, длительно получавших тиреотропин, до 5 и меньше у гипофизэктомированных животных. У людей, потребляющих с пищей нормальные количества иода, эта величина составляет примерно 25.
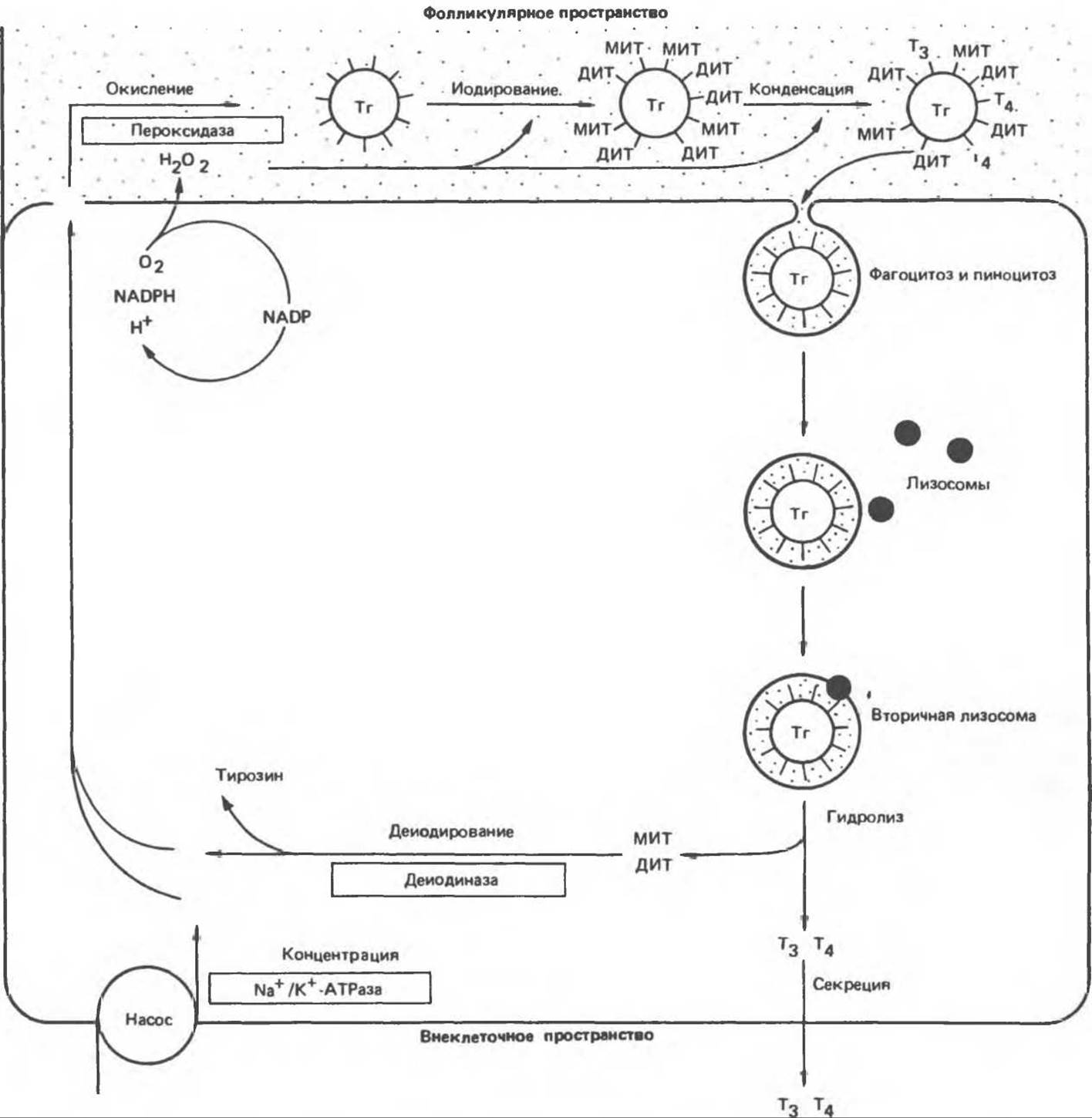
Рис. 46.2. Схема метаболизма иодида в тиреоидном фолликуле. Показана фолликулярная клетка, контактирующая с просветом фолликула (верхняя часть рисунка, выделенная точками) и с внеклеточным пространством (нижняя часть рисунка). Иодид поступает в щитовидную железу благодаря действию насоса и путем пассивной диффузии. Синтез тиреоидных гормонов протекает в фолликулярном пространстве через ряд реакций, многие из которых опосредуются пероксидазой. Гормоны высвобождаются из тиреоглобулина путем гидролиза. ТГ — тиреоглобулин; МИТ — моноиодтирозин; ДИТ — дииодтирозин; Т3 — трииодтиронин; Т4 — тетраиодтиронин. Звездочки обозначают стадии или процессы, катализируемые ферментами, врожденная недостаточность которых вызывает зоб и часто приводит к гипотиреозу.
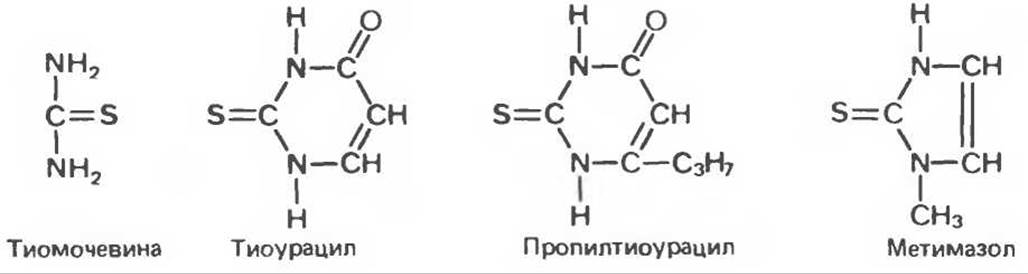
Рис. 46.3. Антитиреоидные препараты группы тиомочевины.
Очень малые количества иодида поступают в щитовидную железу также путем диффузии. Внутриклеточный I-, не включившийся в МИТ или ДИТ (обычно менее 10%), с помощью этого механизма может и покидать железу.
Транспортный механизм ингибируется двумя классами молекул. Первая группа состоит из анионов с таким же специфическим парциальным объемом, как у I-, и включает перхлорат (СlO-4), перренат (ReO-4) и пертехнетат (ТсО-4). Эти анионы конкурируют с иодидом за переносчик концентрируются щитовидной железой. Радиоизотоп ТсО-4 часто применяют для изучения транспорта иодида у человека. В качестве примера молекул второй группы можно привести линейный анион тиоцианата (SC- N-), который конкурентно тормозит транспорт I-, но не концентрируется железой. Ингибиторы транспорта I- позволяют оценить быструю диффузию обменивающегося I- из щитовидной железы и применяются для диагностики нарушений его органификации. После разового введения блокирующей дозы ингибитора транспорта количество аккумулированного I (обычно измеряемого с использованием 131I), покидающего железу, обнаруживает прямую зависимость от величины несвязанной или неорганифицированной (неорганической) фракции. У лиц с неполной органификацией в ответ на введение СlO-4 «высвобождается» больше 131I, чем у здоровых людей.
Окисление I-
Щитовидная железа — единственная ткань, способная окислять I до состояния с более высокой валентностью, что необходимо для органификации I- и биосинтеза тиреоидных гормонов. В этом процессе, протекающем на люминальной поверхности фолликулярной клетки, участвует содержащая гем пероксидаза.
Тиреопероксидаза представляет собой тетрамерный белок с мол. массой 60 000, требующий перекись водорода в качестве окисляющего агента. Н2O2 образуется NADPH-зависимым ферментом, сходным с цитохром-с-редуктазой. Ряд соединений тормозит окисление I- и, следовательно, его дальнейшее включение в МИТ и ДИТ. Среди них наибольшее значение для клиники имеют соединения группы тиомочевины; некоторые из них представлены на рис. 46.3. Эти соединения применяют в качестве антитиреоидных препаратов в силу их способности подавлять на данном этапе биосинтез гормонов щитовидной железы.
Иодирование тирозина
Окисленный иодид реагирует с тирозильными остатками тиреоглобулина. причем и в этой реакции, вероятно, принимает участие тиреопероксидаза. В первую очередь иодированию подвергается третье положение ароматического кольца, а затем — пятое с образованием соответственно МИТ и ДИТ. Указанная реакция, иногда называемая органификацией, протекает в люминальном тиреоглобулине в течение секунд. После иодирования иод уже не может быстро покинуть железу. Иодированию может подвергаться свободный тирозин, но он не включается в белки из-за отсутствия тРНК, распознающей иодированный тирозин.
Конденсация иодтирозинов
Конденсация двух молекул ДИТ с образованием Т4 или МИТ и ДИТ с образованием Т3 происходит в составе молекулы тиреоглобулина, хотя нельзя полностью исключить и возможность конденсации свободных МИТ и ДИТ со связанным ДИТ. Специальный конденсирующий фермент, осуществляющий это взаимодействие, не найден, и, поскольку процесс имеет окислительный характер, считают, что и он катализируется тиреопероксидазой которая стимулирует образование свободных радикалов иодтирозина. Эту гипотезу подтверждает тот факт, что реакция конденсации подавляется теми же агентами, которые ингибируют окисление I-. Образовавшиеся гормоны остаются в составе тиреоглобулина до начала его деградации, о которой говорилось выше. Гидролиз тиреоглобулина стимулируется тиреотропином, но тормозится I-; последний эффект иногда используют, применяя KI для лечения гипертиреоза.