Биохимия - Химические реакции в живой клетке Том 1 - Д. Мецлер 1980
Как молекулы соединяются друг с другом
Кооперативные изменения конформации
Неравноценное связывание субстрата и индуцированное соответствие
Допустим, что конформер В связывается с X прочнее, чем конформер А (это отражено на приведенной выше схеме, где форма центров связывания конформеров различается). Истинные константы связывания конформеров А и В с молекулой X — KAX и KBX (или Kт и KR) — соответственно равны
![]()
Ниже представлены все равновесные процессы, протекающие в этой системе.
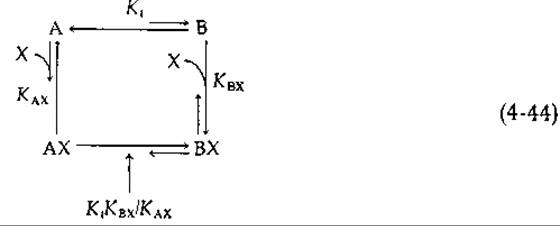
Обратите внимание, что константа, характеризующая равновесие между АХ и ВХ, является функцией трех других констант, а именно КtКBX/КAX. Теперь рассмотрим следующую ситуацию. Предположим, что в отсутствие X преобладает А, однако X более прочно связывается с В, чем с А. Тогда в равновесной смеси будут преимущественно присутствовать или свободный А, или ВХ (в меньших количествах будут находиться также АХ и В). Возникает интересный с точки зрения кинетики вопрос: по какому из двух возможных путей будет протекать реакция перехода от А к ВХ [уравнение (44)]? Первый вариант, рассматриваемый в модели Моно—Уаймена—Шанжё, предполагает, что X связывается только с В, небольшое количество которого присутствует в смеси в равновесии с А. Согласно второму варианту, X связывается с А, но АХ затем быстро переходит в ВХ. Можно сказать, что X вызывает (индуцирует) конформационное изменение в белке А, облегчающее «состыковку». Именно на этом основана концепция Кошланда, известная под названием концепции индуцированного соответствия. Следует иметь в виду, что, зная константы равновесия, можно определить только равновесные концентрации всех четырех форм, присутствующих в уравнении (4-44). Однако при изучении метаболизма нас чаще интересуют скорости тех или иных реакций, а не равновесное состояние, а исходя только из данных для равновесной системы, а priori нельзя сказать, по какому из двух возможных путей будет реально протекать данная реакция.
Заметим, что, если отношение Квх/Ках очень велико, то в равновесной смеси будет присутствовать лишь незначительное количество АХ. В этом случае определить экспериментально величину Ках не удается, но для описания состояния равновесия достаточно знать две константы — Кт и КBX.