Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Пиридиннуклеотидные коферменты и дегидрогеназы
В 1904 г. Гарден и Ионг показали, что бесклеточный «сок»1) дрожжей теряет после диализа способность сбраживать глюкозу в спирт и двуокись углерода. По-видимому, процесс сбраживания зависел от наличия какого-то низкомолекулярного вещества, способного проходить через поры мембраны для диализа. Брожение могло быть востановлено добавлением концентрированного диализата дрожжевого сока или прокипяченного сока дрожжей (в котором ферментные белки были разрушены). В конце концов было установлено, что термостабильный материал, который Гарден и Янг назвали козимазой, является смесью неорганического фосфата, тиаминдифосфата и NAD. Однако NAD не был охарактеризован вплоть до 1935 г.
Чистый NAD выделили в 1934 г. из эритроцитов Варбург и Кристиан, которые изучали окисление в этих клетках глюкозо-6-фосфата [67]. Эти исследователи показали, что для брожения требуется какой-то диализуемый кофактор, который был ими охарактеризован и назван трифосфопиридиниуклеотидом (TPN), ныне официально именуемом NADP+ (рис. 8-10). Интересно, что никотинамид еще до признания за ним роли витамина, необходимого в питании человека, был идентифицирован в качестве составной части NAD.
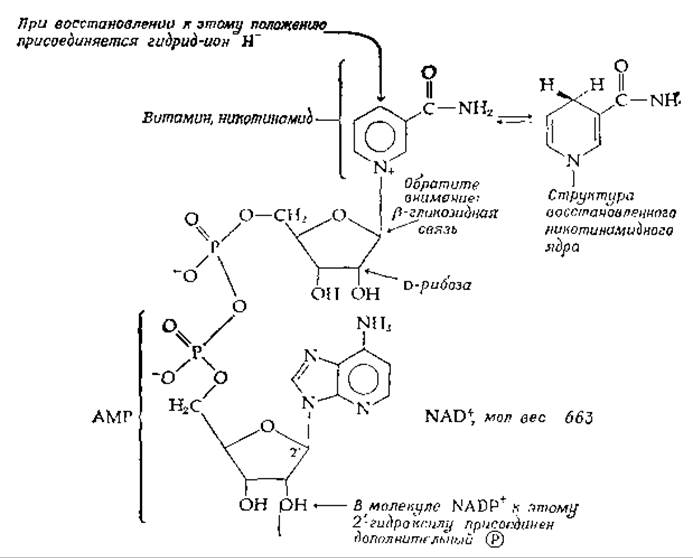
РИС. 8-10. Коферменты переноса водорода NAD+ (DPN+) и NADP+ (TPN+). Обратите внимание на то, что используются сокращения NAD+ и NADP+, несмотря на то, что суммарный заряд всей молекулы при pH 7 является отрицательным.
1) Сок получали растиранием дрожжей с песком и фильтрованием. Установление Бухнером (1899 г.) факта, что такой сок дрожжей сбраживает сахар, явилось одной из отправных точек в развитии современной биохимии.
Варбург и Кристиан пришли к заключению о близости NADP к NAD и предположили, что оба эти соединения функционируют в качестве переносчиков водорода путем чередующихся актов восстановления и окисления пиридинового кольца. Они показали, что эти коферменты могут быть восстановлены как ферментативным, так и неферментативным путем при помощи дитионита натрия Na2S2О4:
S2О2-4- + NAD+ + Н+→ NADH + 2SО2.----------------------------------- (8-39)
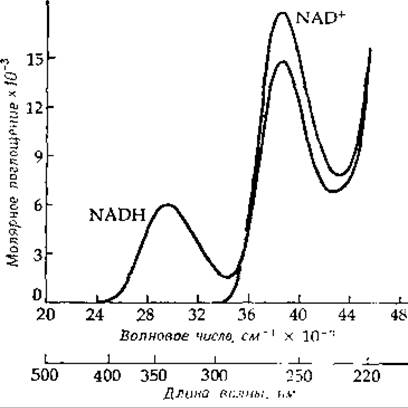
РИС. 8-11. Спектры поглощения NAD+ и NADH. Спектры NADP+ и NADPH выглядят примерно также. Различие в поглощении окисленной и восстановленной форм при 340 нм является основой, по-видимому, наиболее часто используемого в биохимии спектрального метода. Множество методов определения активности ферментов основано на измерении восстановления NAD+ или NADP+ или окисления NADH или NADPH. Если пиридиннуклеотид не является субстратом изучаемого фермента, то часто можно использовать «методы сопряжения». Например, скорость ферментативного синтеза АТР можно определить, добавляя к реакционной смеси глюкозу+гексокиназу+глюкозо-6-фосфатдегидрогеназу+НАDР+. По мере синтеза АТР фосфорилирует глюкозу (при участии гексокиназы). Затем NADP+ окисляет образующийся глюкозо-6-фосфат с образованием NADPH, скорость синтеза которого регистрируется при 340 им.
Для восстановленных коферментов NADH и NADPH характерна новая спектральная полоса поглощения при 340 нм, отсутствующая у окисленных форм; у последних максимум поглощения лежит при 260 нм (рис. 8-11). Восстановленные формы устойчивы на воздухе, однако установлено, что они могут вновь окисляться под действием определенных «желтых ферментов».
Дополнение 8-3
Никотиновая кислота и никотинамид
Никотиновая кислота была получена в 1867 г. окислением никотина. Она была выделена Функом и независимо от него Судзуки (1911—1912 гг.) из дрожжей и рисовых отрубей, однако тогда не подозревали, что она является витамином. Биологическое значение никотиновой кислоты установлено впервые в 1935 г., когда было обнаружено, что в соcтав NAD+ (Эйлер и сотрудники) и NADP+ (Варбург и Кристиан) входит никотинамид.
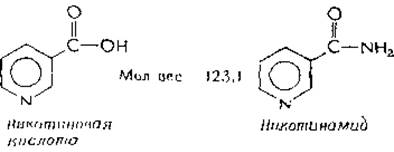
В 1937 г. Эльвигьем и сотрудники описали лечение болезни «черного языка» у собак с помощью никотиновой кислоты, а затем в том же году несколько групп исследователей сообщили о возможности лечения его пеллагры у человека. В то время пеллагра была очень распространенным заболеванием в США, особенно на Юге. По оценке Национальной службы здоровья США в 1912—1916 гг. насчитывалось ежегодно 100 000 жертв этой болезни, причем 10 000 человек из них погибалиа,б. (Для пеллагры характерны слабость, расстройство пищеварения и потеря аппетита, далее следуют дерматит, диарея, психические расстройства и в конце концов смерть).
Физические свойства. Обе формы витамина устойчивы, бесцветны, хорошо растворимы в воде.
Суточная потребность: около 7,5 мг для взрослых. Это количество снижается при наличии в пище триптофана, который может частично превращаться в никотиновую кислоту (гл. 14, разд. И). Активность триптофана составляет примерно 1/60 активности самой никотиновой кислоты. Былое распространение пеллагры на юге США было прямым следствием преимущественного питания кукурузой, белки которой содержат мало триптофана.
а Wagner A. F., Folkers К. (1964). Vitamins and Coenzymes, р. 73, Wiley (Interscience), New York.
б Обзоры двух интересных книг, касающихся истории пеллагры см. в работе Rosenkranlz В. G. (1974). Science, 183, 949—950.