Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Пиридиннуклеотидные коферменты и дегидрогеназы
Глицеральдегид-3-фосфат - дегидрогеназа и образование АТР в реакциях брожения
Восстановление карбоксильных групп в альдегидные в биохимических процессах обычно протекает путем их превращения в тиоэфир в реакциях, протекающих с участием АТР, с последующим восстановлением тиоэфира (реакция типа 9, В в табл. 8-3). И наоборот, окисление альдегида в карбоновую кислоту — сильно экзергоничный процесс; он обычно протекает через тиоэфирное промежуточное соединение, последующее расщепление которого может быть сопряжено с синтезом АТР. Эта реакция (S9C), которая чрезвычайно важна для энергетического метаболизма клетки, приведена на рис. 8-13 для последующего ее обсуждения.
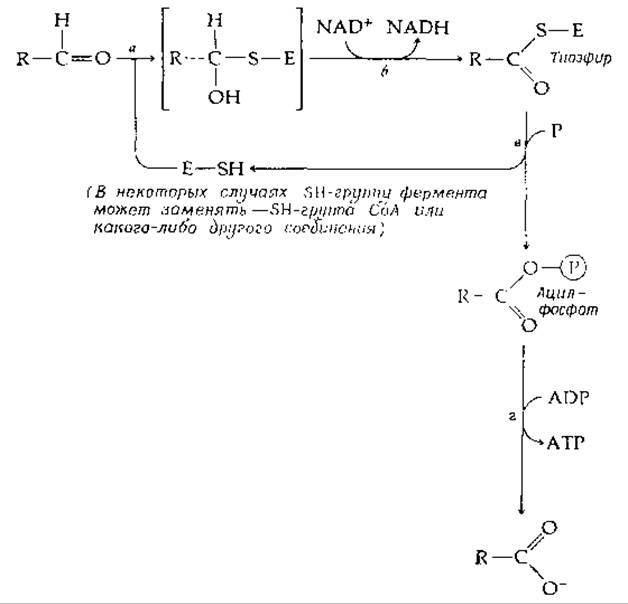
РИС. 8-13. Синтез АТР, сопряженный с окислением альдегида в карбоновую кислоту (реакция типа S9B). Наиболее важной из известных реакций этого типа является окисление глицеральдегид-3-фосфата до 3-фосфоглицерата (рис. 9-7). Другие важные реакции фосфорилирования на «субстратном уровне» приведены на рис. 8-4, 8-19 и 8-21.
Наиболее примечательным примером, заслуживающим упоминания, служит глицеральдегид-3-фосфат—дегидрогеназа—тетрамер, построенный из идентичных субъединиц с мол. весом 45 000. Трехмерная структура этого фермента установлена (рис. 2-10) [78]. Напомним, что альдегиды находятся в равновесии со своим ковалентным гидратом:
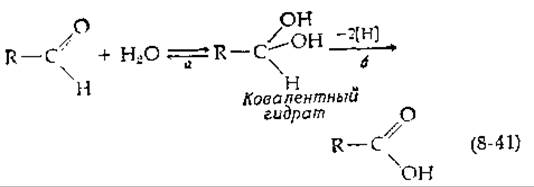
Дегидрирование последнего приводит к образованию кислоты (стадия б). Однако такой механизм не оставлял бы никакой возможности для консервирования энергии, освобождающейся в результате реакции. В случае глицеральдегидфосфатдегидрогеназы фермент обладает специальной сульфгидрильной группой, которая на первой стадии (стадия а, рис. 8-13) присоединяется к карбонильной группе с образованием аддукта (тиополуацеталя). Затем аддукт окисляется NAD+ до тиоэфира S-ацилфермента (стадия б). Последний расщепляется тем же ферментом путем замещения у атома углерода атомов кислорода неорганического фосфата (фосфоролиз, стадия в). Одновременно освобождается сульфгидрильная группа фермента и образуется продукт ацил-фосфат (1,3-дифосфоглицерат). Затем другой фермент переносит фосфатную группу из С-1 1,3-дифосфоглицерата на ADP с образованием АТР и 3-фосфоглицерата. Суммарная реакция, приведенная на рис. 8-13, заключается в синтезе 1 моль АТР, сопряженном с окислением альдегида в карбоновую кислоту.
Заметим, что две последние стадии реакции рис. 8-13 (стадии в и г) представляют собой обращение последовательности S1A (а), приведенной в табл. 7-2. Таким образом, химизм процесса синтеза АТР в ходе гликолиза подобен таковому использования АТР в процессах биосинтеза. Однако в первом случае «высокоэнергетический» тиоэфир образуется в результате реакции окисления (стадии а и б на рис. 8-13). Арсенат разобщает синтез АТР и окисление в этой последовательности (дополнение 7-А).
Реакция, сходная с той, которую катализирует глицеральдегид-3-фосфат—дегидрогеназа, катализируется глюкозо-6-фосфат—дегидрогеназой. Именно этот фермент первоначально привлек к себе внимание Варбурга и привел к открытию NADP+. Субстратом этого фермента служит не свободный альдегид, а циклическая форма полуацеталя, которая окисляется в лактон. Затем лактон гидролизуется до 6-фосфоглюконата.
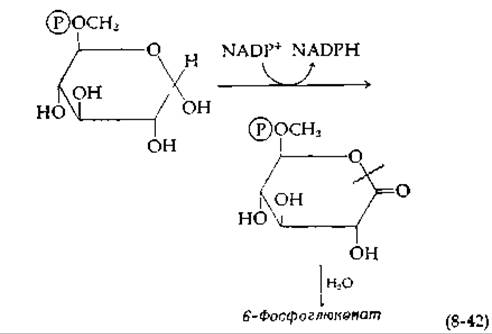
По-видимому, клетки не способны запасать энергию, освобождающуюся при окислении этого альдегида в карбоновую кислоту. Однако стадия раскрытия кольца обеспечивает полноту протекания этой реакции. Следует отметить, что эта реакция служит одним из главных поставщиков восстановленного NADP (NADPH) для восстановительного биосинтеза и что сильное снижение свободной энергии в суммарной реакции обеспечивает поддержание в клетке отношения [NADPH]/[NADP+].