Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Флавиновые коферменты
Реакции восстановленных флавинов с кислородом
В отсутствие фермента свободный дигидрорибофлавин реагирует с молекулярным кислородом (с образованием перекиси водорода) за считанные секунды, а в случае восстановленных флавиновых дегидрогеназ реакция протекает даже быстрее. Промежуточное соединение, по-видимому аддукт в положении 4а [уравнение (8-59)]:
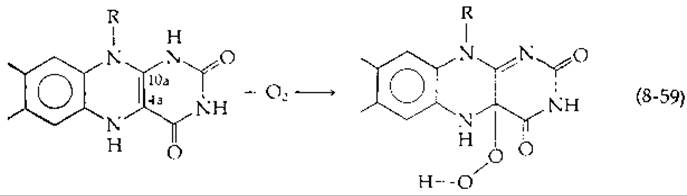
в случае неферментативного процесса можно обнаружить спектрофотометрическим методом [132, 133]. (Возможно также присоединение к другим положениям.) В работе [134] предполагается образование циклической перекиси в результате присоединения O2 к атомам углерода в положениях 4а и 10а:
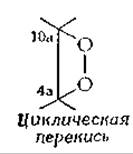
Образование тех или иных продуктов при многих реакциях, катализируемых различными флавопротеидами, можно было бы объяснить, исходя из наличия перекисных промежуточных соединений. Так, например, распад аддукта в реакции (8-59) в результате протонирования внутреннего атома кислорода мог бы привести к образованию Н2О2 и окисленного флавина. В то же время связь С—О могла бы расщепляться гомолитически с образованием двух радикалов: флавинового радикала и пероксирадикала ∙ O2Н. Последний может в свою очередь диссоциировать с образованием супероксидного анион-радикала:
![]()
Различные металлсодержащие супероксиддисмутазы катализируют следующую реакцию:
![]()
При спонтанном реокислении восстановленного флавина в присутствии супероксиддисмутазы скорость процесса будет значительно ниже, чем в отсутствие данного фермента. Это наблюдение указывает на то, что неферментативиое реокисление восстановленных флавинов протекает по механизму с образованием радикалов, включающему образование супероксид-аниона. Для дальнейшего превращения флавинового радикала в полностью окисленную форму нужна вторая стадия:
![]()
Однако супероксиддисмутазы обычно оказывают слабое влияние на реокисление флавина в дегидрогеназах. Исключение составляет ксантиноксидаза, которая является очень мощным продуцентом супероксид-анионов. Фрид и сотр. [134а] предположили, что важной функцией ксантиноксидазы является синтез перекиси водорода и супероксид-радикалов, используемых в сопряженных процессах биологического окисления.
Другой класс флавопротеидов, обсуждаемых в гл. 10 (разд. Ж, 2), составляют монооксигеназы или гидроксилазы. В этих ферментах восстановленный флавин способствует включению одного атома кислорода из молекулы O2 в субстрат с одновременным превращением другого атома кислорода в Н2O. Формально реакцию можно представить как расщепление связи между двумя кислородами аддукта в схеме (8-59) с образованием ОН+ из концевой ОН-группы.