Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Коферменты - особые природные специализированные реагенты
Липоевая кислота и окислительное декарбоксилирование а-кетокислот
Окислительное декарбоксилирование перекисью водорода
Неферментативное окислительное декарбоксилирование а-кетокислот перекисью водорода является хорошо изученной реакцией. Первая стадия состоит, видимо, в образовании аддукта — органической перекиси, которая распадается согласно уравнению (8-67):
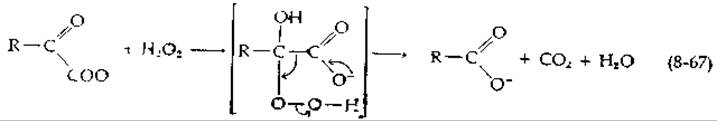
Превращение, которое можно рассматривать как ферментативный вариант этой реакции, ускоряется лактатоксигеназой — гексамерным флавопротеидом с мол. весом ~ 350 000, полученным из Mycobacterium. В анаэробных условиях фермент продуцирует пируват путем простого дегидрирования [142]. Однако в присутствии кислорода образуется уксусная кислота, причем один из атомов кислорода карбоксильной группы происходит из O2. Поскольку перекись водорода — обычный продукт, образующийся из кислорода под действием флавопротеидов, возможно, что в случае лактатоксигеназы образующаяся перекись водорода непосредственно окисляет пируват1) в соответствии с уравнением (8-67).
Тем не менее механизм действия этого фермента точно не установлен. Действительно, фермент вырабатывает пируват в отсутствие O2, однако никакие реагенты, улавливающие пируват или Н2O2, не ингибируют реакции [143]. Возможно, Н2O2 и пируват возникают в непосредственном соседстве и реагируют так быстро, что ни один из этих продуктов нельзя «перехватить». В то же время не исключено образование супероксидного анион-радикала вместо Н2O2 [уравнение (8-60)]. Предложены и другие механизмы [144, 145]. Некоторые другие флавопротеидные гидроксилазы могут действовать аналогичным образом (гл. 10, разд. Ж,2).
1) а-Кетокислоты, полученные под действием оксидаз аминокислот, также окисляются накапливающейся перекисью водорода. Добавление каталазы (гл. 10, разд. Б,6) приводит к разрешению Н2O2 и накоплению кетокислот.