Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
О том, как электроны встречаются с кислородом, как при этом образуется ATR и о некоторых родственных явлениях
Гемопротеиды
Некоторые названия, которые следует запомнить
В 1879 г. немецкий ученый Хоппе-Зейлер, занимавшийся исследованиями в области физиологической химии, установил, что два самых ярких и впечатляющих цвета природы имеют родственное происхождение. Оказалось, что красный железосодержащий гем в крови и зеленый магниевый комплекс хлорофилла а в листьях имеют сходную кольцевую структуру. Однако получить строгие доказательства на этот счет выпало на долю Фишера, работавшего в Чюнхене, который в период с 1910 по 1940 г. установил строение этих соединений, а также ввел систему наименований и нумерацию, которые мы используем в настоящее время.
Порфины представляют coбой большие кольца, образованные из четырех меньших по размеру пиррольных колец, соединенных между собой четырьмя метеновыми мостиками. У хлоринов, обнаруженных в хлорофиллах, одно из колец (D) находится в восстановленной форме. У особого класса порфинов, порфиринов, по периферии большого кольца имеется восемь замещающих групп. Порфирины так же, как хлорины и Корины витамина B12(дополнение 8-Л), образуются путем биосинтеза из порфобилиногена. Это соединение полимеризуется двумя путями (рис. 14-13), образуя порфирины типа I и III (рис. 10-1). При образовании порфиринов типа I полимеризация порфобилиногена идет регулярным образом, так что вокруг кольца наблюдается правильное чередование карбоксиметильных и карбоксиэтильных боковых цепей (которые часто называют боковыми цепями уксусной и пропионовой кислот). Однако наиболее важные в биологическом отношении порфирины принадлежат к типу III, в котором первые три кольца А, В, С имеют такую же последовательность карбоксиметильных и карбоксиэтильных боковых цепей, как и порфирины типа I, а кольцо D — «обратную». В результате карбоксиэтильные боковые цепи колец С и D оказываются расположенными по соседству (см. рис. 10-1). Порфирины, у которых имеются четыре карбоксиметильные и четыре карбоксиэтильные боковые группы, называются уропорфиринами. Уропорфирины типа I и III в небольших количествах выделяются с мочой. Другим продуктом экскреции является копропорфирин III, у которого все карбоксиметильные боковые цепи декарбоксилированы до метальных групп. Окраска перьев тропической птицы турако обусловлена медь(II)- содержащим комплексом копропорфирнна III; этот порфирин наряду с другими имеется в яйцах птиц.
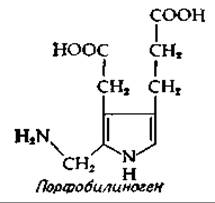
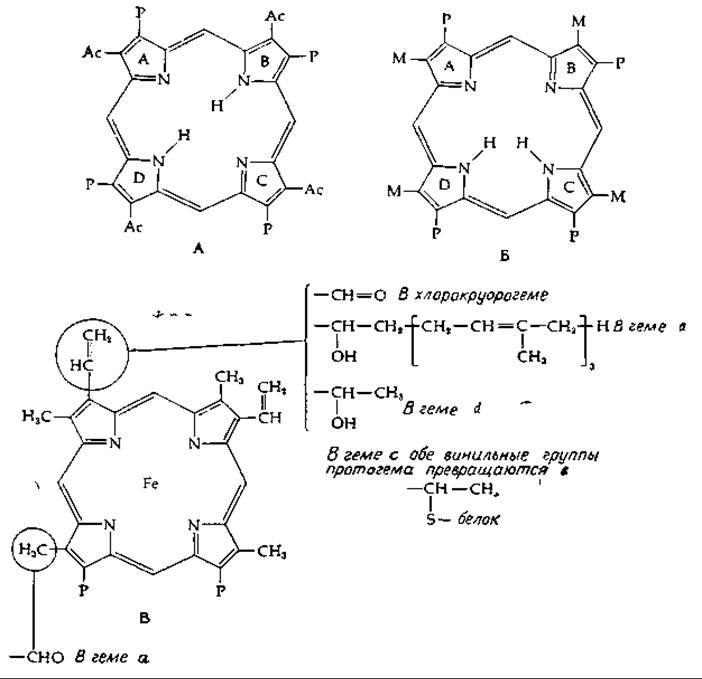
РИС. 10-1. Структура некоторых биологически важных порфиринов А. Уропорфирии I; Ас =—СН2СООН и Р =—СН2СН2СООН. Б. Копропорфирин III (Заметьте, что по сравнению с А здесь изображена другая таутомерная модификация кольца. Такая таутомерия характерна для всех порфиринов) В. Протогем — Ре2+-комплекс протопорфирина IX, присутствующий в гемоглобине, цитохромах b и различных других белках.
Все гемопротеиды образуются из протопорфирина IX, который является продуктом декарбоксилирования копропорфирнна III; вместо двух карбоксиэтильных боковых цепей, у него имеются две винильные группы (рис. 10-1).