Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Биосинтез; как образуются новые молекулы
Биосинтез мономеров
Начиная с СО2
Клетки, в которых имеются необходимые ферменты и требуемое соотношение между восстановленной и окисленной формами ферредоксина, могут использовать реакцию (11-14) для включения СО2 в пируват. Сукцинил-СоА может аналогичным образом взаимодействовать с СО2, давая а-кетоглутарат (гл. 8, разд. К, 3). Это обусловливает обратимость единственной необратимой стадии в цикле трикарбоновых кислот. Используя эти реакции, фотосинтетнческие бактерии и некоторые анаэробные организмы осуществляют восстановительный цикл трикарбоновых кислот. Вместе с реакцией (11-14) этот цикл обеспечивает полное превращение С02 в пируват.
С количественной точки зрения значительно более важным путем, обеспечивающим фиксацию СО2, является восстановительный пентозофосфатный путь, известный под названием цикла Кальвина (дополнение 11-А). Эта последовательность реакций имеет место в хлоропластах зеленых растений, а также в хемоавтотрофных бактериях. Цикл Кальвина представляет собой по существу путь обращения окислительного пентозофосфатного цикла (рис. 9-8), в процессе которого происходит полное окисление глюкозы при помощи NADP+ (с использованием одной молекулы АТР, необходимой для превращения исходной молекулы глюкозы в глюкозо-6-фосфат):
![]()
В связи с большой положительной величиной изменения свободной энергии для зеленых растений представляется почти невозможной фиксация СО2 путем взаимодействия с фотохимически образуемым NADPH точно по пути, обратному последовательности (11-15). Чтобы обойти это термодинамическое по своей природе затруднение, восстановительный пентозофосфатный путь был несколько изменен, в результате чего синтез стал сопряжен с расщеплением дополнительного количества АТР.
На рис. 11-4 система восстановительного карбоксилирования обведена пунктирной линией. Исходным соединением в этой системе является рибозо-5-фосфат, который на первой стадии фосфорилируется до рибулозо-1,5-дифосфата, расходуя при этом одну молекулу АТР. Образующийся рибулозо-1,5-дифосфат далее карбоксилируется и расщепляется на две молекулы 3-фосфоглицерата (эта реакция была рассмотрена в гл. 7, разд. К, 3, Ж). Восстановительная стадия (стадия в) системы реализуется за счет совместного использования NADPH и АTP. Если не считать того, что вместо системы NAD здесь используется система NADP, эта стадия представляет собой точное обращение одной из стадий гликолиза, катализируемой фосфоглицеральдегиддегидрогеназой (гл. 8, разд. 3,5). Если внимательно посмотреть на первые три стадии процесса, приведенного на рис. 11-4, то можно видеть, что в процессе восстановительного пентозофосфатного пути на каждую включенную молекулу СО2 расходуется три молекулы АТР. В то же время окислительное направление этого процесса не сопровождается образованием АТР. Таким образом, различие между катаболическим и биосинтетическим путями опять создает необходимость в сопряжении процесса с гидролизом АТР с тем, чтобы необратимую последовательность реакций сделать обратимой.
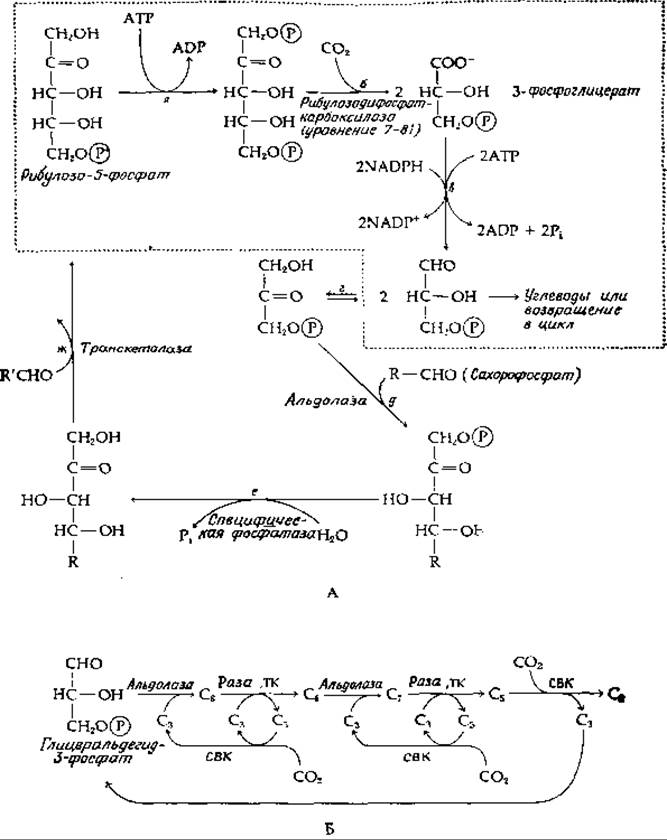
РИС. 11-4. А. Восстановительная карбоксилирующая система, используемая в восстановительном пентозофосфатном метаболическом пути. Сначала показаны реакции, существенные для этой системы (обведены пунктирной линией), после чего идут типичные последующие реакции. Цикл «фосфорилирование — дефосфорилирование» завершается действием фосфатазы. Б. Восстановительный пентозофосфатный цикл изображен таким образом, чтобы было наглядно видно, как связываются три молекулы СО2, давая одну молекулу триозофосфата. RCS — система восстановительного карбоксилирования.
Реакции, обведенные пунктирной линией на рис. 11-4, не дают полного представления о механизме сопряжения. На стадии а фосфатная группа переносится от АТР, и для завершения гидролиза она должна быть удалена на какой-нибудь из последующих стадий. Это показано в общем виде на рис. 11-4 (на стадиях г, д и е). На стадии е происходит действие специфических фосфатаз, которые отцепляют фосфатные группы от содержащего семь углеродных атомов седогептулозодифосфата и от фруктозодифосфата. В обоих случаях образующийся кетозомонофосфат реагирует с альдозой (через транскетолазу, стадия ж), регенерируя рибулозо-5-фосфат, акцептор СО2. Суммарный восстановительный пентозофосфатный цикл (рис. 11,4, Б) легко можно представить себе как процесс, протекающий в направлении, обратном окислительному пентозофосфатному пути, в котором система окислительного декарбоксилирования [уравнение (9-15)] заменена на систему восстановительного карбоксилирования, показанную на рис. 11-4,А. Схема, приведенная на рис. 11-4, Б, показывает включение трех молекул СО2. Система восстановительного карбоксилирования (на рисунке она обозначена «СВК») функционирует соответственно три раза, давая в итоге одну молекулу триозофосфата. В этом цикле, также как и в других биосинтетических циклах (стр. 323), любое количество любого из промежуточных метаболитов может извлекаться и включаться в различные другие метаболические пути так, чтобы поток веществ через цикл не прекращался.
Суммарная реакция восстановления СО2 в цикле Кальвина может быть описана уравнением
![]()
Измерение свободной энергии ∆G' (pH 7) составляет —378 кДж∙моль 1 вместо +278 кДж∙моль-1, требуемых для обращения реакции (11-16).
Дополнение 11-А
14С и цикл Кальвина
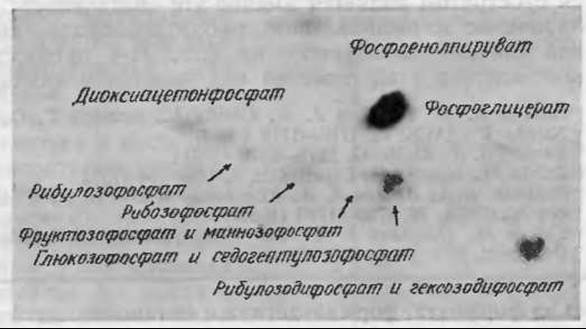
Хроматограмма экстракта водоросли Scenedesmus, полученная после фотосинтеза в присутствии 14СО2 в течение 10 с.
Химическая природа фотосинтеза интересовала химиков в течение столетий, однако мало что было известно относительно деталей этого процесса до тех пор, пока не стал доступен радиоактивный изотоп 14С. Этот изотоп был открыт в 1940 г. С. Рубиным и М. Каменом, однако в достаточных количествах его стали получать только в 1945 г. в качестве продукта ядерного реактора. В этом же году М. Кальвин и его сотрудники начали свои исследования, которые привели к выяснению механизма включения СО2 в органические соединения; за эти исследования Кальвин в 1961 г. был удостоен Нобелевской премии.
Ключевую роль в этом исследовании сыграло сочетание методов двухмерной хроматографии на бумаге и радиоавтографии (дополнение 2-В). Суспензия водоросли Chlorella (рис. 1-9) осуществляла фотосинтез в струе обычной СО2 на свету. Спустя определенное время в систему вводили некоторое количество Н214СО3 и через несколько секунд, в течение которых фотосинтез происходил с 14С, суспензию водоросли переносили в метанол, в котором белки подвергались денатурации и реакция останавливалась. Растворимые вещества, экстрагированные из клеток водоросли, концентрировали и подвергали хроматографическому разделению, после чего с хроматограмм снимали радиоавтографы. Было обнаружено, что в тех случаях, когда фотосинтез в присутствии 14СО2 продолжался более 10 с, водоросли содержали десяток или даже большее число соединений, меченных изотопом 14С, и в частности малоновую кислоту, аспарагиновую кислоту, РЕР, аланин, триозофосфат и другие сахаромонофосфаты и дифосфаты. Однако если фотосинтез продолжался менее пяти секунд, то. большая часть радиоактивности обнаруживалась только в одном соединении — в 3-фосфоглицератеа. Это открытие позволило предположить, что фосфоглицерат представляет собой продукт карбоксилирования при помощи 14СО2 какого-то регенерирующегося двухуглеродного субстрата, протекающего на ранней стадии фотосинтеза. Поиск этого двух углеродного соединения в течение долгого времени не приводил к успеху, однако сотруднику лаборатории Кальвина А Бенсону удалось идентифицировать рибулозодифосфатб и кинетическими исследованиями доказать, что регенерирующимся субстратом является именно это соединениев-г. Карбоксилирование и расщеплениед рибозодифосфата явилось первой стадией показанного на фиг. 11-4 процесса, который впоследствии стал известен под названием цикла Кальвина.
а Benson A. A., Bassham J.. A., Calvin М., Goodale Т. С., Haas V. А., Stepka W., JACS, 72, 1710—1718 (1950).
б Benson A. A., JACS, 73, 2971—2972 (1951)
в Calvin М., Massini Р., Experientia, 8, 445—484 (1952)
г Bassham J. A., Benson А. А, Kay L. D., Harris A. Z., Wilson A. T., Calvin M., JACS, 76, 1760—1770 (1954).
д Calvin M., Bassham J. A., The Photosynthesis of Carbon Compounds, Benjamin, New York, 1962.