Биохимия - Химические реакции в живой клетке Том 2 - Д. Мецлер 1980
Типы реакций, катализируемых ферментами
Реакции множественного замещения и сопряжение реакций расщепления АТР с эндергоническими процессами
СоА-трансферазы
Часто возникает следующая проблема переноса энергии: в распоряжении клетки всегда имеется тиоэфир, например сукцинил-СоА, в нестабильной связи которого запасена энергия, необходимая для синтеза различных тиоэфиров. Клетка могла бы сначала синтезировать АТР или GTP в обратной тиокиназной реакции, а затем использовать образовавшиеся АТР и GTP для синтеза новой связи при участии опять-таки тиокиназы. Однако имеются специальные ферменты, СоА-трансферазы, действие которых осуществляется более прямым путем:
![]()
Механизм действия этих ферментов точно не установлен. Каким образом СоА может переноситься от одной ацильной группы к другой, сохраняя при этом высокий потенциал переноса ацильной группы?
Следующие эксперименты проливают свет на этот вопрос. На основании изучения кинетики реакции, катализируемой сукцинил-СоА: ацетоацетат — СоА-трансферазой, был сделан вывод о наличии пинг-понг механизма (гл. 6). Таким образом, фермент представлен двумя различными формами, одна из которых, как было показано, содержит связанный СоА [92]. Промежуточное соединение фермент—СоА, образующееся при взаимодействии фермента и ацетоацетил-СоА, восстанавливали меченным 3Н боргидридом натрия, а затем при помощи НСl осуществляли полный гидролиз ферментного белка. В результате была выделена тритированная а-амино-δ-оксивалериановая кислота.
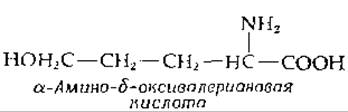
Поскольку тиоэфиры, так же как и сложные эфиры, при действии бор- гидрида натрия расщепляются до спиртов (в результате двухстадийной реакции), было сделано заключение, что промежуточный продукт фермент—СоА представляет собой тиоэфир, образованный с участием карбоксильной группы боковой цепи глутаминовой кислоты [93]. Изучение реакций обмена, протекающих с меченным 18O сукцинатом, показывает, что 18O из сукцината переходит как в промежуточное соединение фермент—СоА, так и в карбоксильную группу ацетоацетата [94].
Можно представить по крайней мере два механизма, лежащих в основе этого процесса. Первый включает образование промежуточного ангидрида и по своей механике подобен реакциям, которые обсуждались в предыдущих разделах [94а]. Студентам следует записать последовательно все стадии этого механизма. Можно ли, исходя из этого механизма, объяснить данные, полученные при изучении 18O-обмена? Второй возможный механизм — реакция с участием четырех центров:
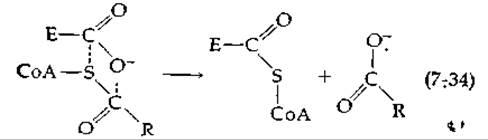
Хотя наличие механизмов этого типа в случае ферментативных реакций не доказано, они в принципе возможны.