Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Метаболизм азотсодержащих соединений
Соединения, образующиеся из аспартата
Лизин, диаминопимелат, дипиколиновая кислота и карнитин
Хотя животные вообще неспособны синтезировать лизин и он для них является одной из незаменимых аминокислот, которые должны обязательно поступать с пищей, известно два различных пути его образования у других организмов. а-Аминоадипинатный путь (рис. 14-2) наблюдается лишь у некоторых представителей низших грибов, у высших грибов и у эвгленид. Исходным соединением служит 5-углеродный а-кетоглутарат. Бактерии, другие виды низших грибов и зеленые растения используют диаминопимелинатный путь (рис. 14-7), начинающийся с четырехуглеродного аспартата.
а-Аминоадипинатный путь (рис. 14-2) идет параллельно пути биосинтеза орнитина. Происходит элонгация цепи а-кетоглутарата (рис. 11-7) с превращением его в а-кетоадипинат, который путем переаминирования преобразуется в а-аминоадипинат. Затем следует ATP-зависимое восстановление в альдегид. Заключительная стадия переаминирования идет необычным образом, без участия PLP-зависимого фермента: альдегид образует шиффово основание с глутаматом с последующим восстановлением в сахаропин. Далее следует стадия окисления, в результате которой образуется шиффово основание между лизином и кетоглутаратом.
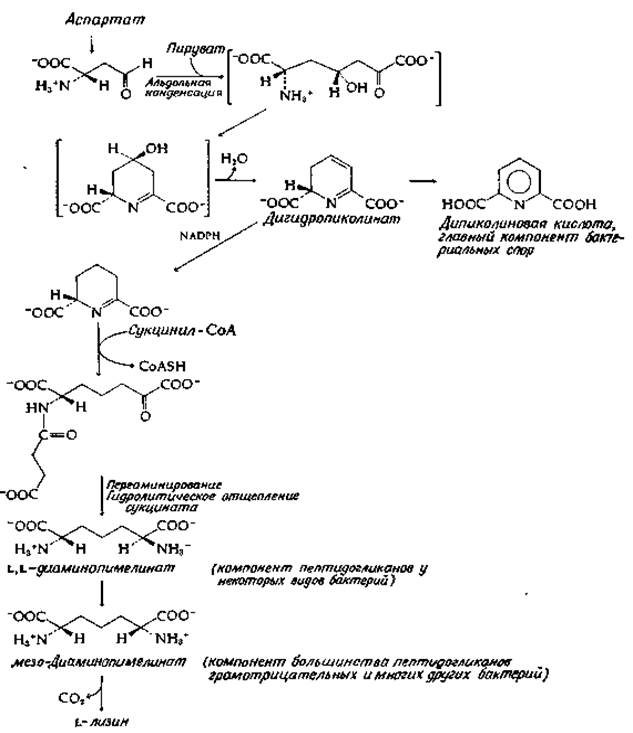
РИС. 14-7. Биосинтез лизина с использованием реакций диаминопимелинатного пути.
В ходе диаминопимелинатного пути синтеза лизина (рис. 14-7) аспартат превращается в полуальдегид аспарагиновой кислоты, к которому в результате альдольной конденсации с пируватом добавляется дополнительное двухуглеродное звено. Декарбоксилирование на конечной стадии приводит к образованию лизина. На этом пути возникает ряд циклических промежуточных соединений, однако стоит отметить, что начальный продукт альдольной конденсации (на рис. 14-7 заключен в скобки) превращается в диаминопимелиновую кислоту через простую последовательность реакций, включающую а,β-элиминирование гидроксильной группы, восстановление за счет NADPH и переаминирование. Процесс осложняется естественной склонностью к замыканию кольца. Стадия сукцинилирования (рис. 14-7) требуется как раз для того, чтобы сместить равновесие обратно — в сторону соединений с разомкнутой цепью. Этот путь имеет особое значение для прокариотических организмов по той причине, что при этом как побочный продукт образуется важная для них дипиколиновая кислота, а на промежуточных стадиях образуются диаминопимелиновые кислоты. Циклическая дипиколиновая кислота — это важный компонент бактериальных спор и более в природе почти нигде не встречается. L,L- и мезо-диаминопимелиновые кислоты являются компонентами пептидогликанов клеточных стенок бактерий (гл. 5, разд. Г).
Лизин не только входит в состав белков, но еще может подвергаться метилированию и последующему расщеплению до у-бутиробетаина [49, 50].
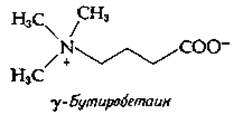
Это соединение образуется как промежуточный продукт при биосинтезе карнитина [50а]:
![]()