Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Метаболизм азотсодержащих соединений
Метаболизм ароматических соединений
Хоризмовая кислота
Хоризмовая кислота обладает такими химическими свойствами, которые и подобает иметь соединению, находящемуся в узловой точке метаболизма. При нагревании она дает смесь префеновой кислоты (реакция и рис. 14-17) и 4-оксибензойной кислоты (реакция м). Обратите внимание, что последняя реакция представляет собой простое элиминирование енолят-аниона из пирувата. Как показано на рис. 14-17, это только лишь две из нескольких возможных метаболических реакций, идущих с участием хоризматиона. Образование фенилпирувата (стадии и я к, рис. 14-17) катализируется одним белком, обладающим двумя четко различающимися видами ферментативной активности [105, 106]. На каждой из этих двух стадий фермент хоризматмутаза-префенатдегидратаза ускоряет ход реакций, идущих спонтанно при нагревании в кислом растворе. Фенилпируват путем переаминирования легко превращается в фенилаланин, чем и завершается биосинтез этой аминокислоты.
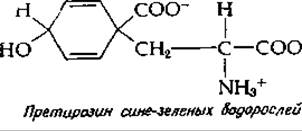
Второй фермент — хоризматмутаза-префенатдегидрогеназа — вызывает окислительное декарбоксилирование префената в n-оксифенилпируват, который может путем переаминирования превращаться в тирозин [105]. И в этом случае один фермент катализирует две стадии и и л; по одной из своих активностей этот белок является изоферментом предыдущего белка, катализирующего стадии и и к. Несколько иной путь образования тирозина был обнаружен у сине-зеленых бактерий. У них префенат подвергается переаминированию с образованием претирозина, а последний путем окислительного декарбоксилирования превращается в тирозин [107].
Хоризмат может также подвергаться изомеризации, гидролизу и дегидрированию с образованием 2,3-дезоксибензоата, предшественника энтеробактина (рис. 2-44) [107а]. Гены (ent), кодирующие эти ферменты, сгруппированы на хромосомной карте Е. coli на расстоянии 14 мин (рис. 15-1).