Фармакогнозія з основами біохімії рослин - Ковальов В. М. 2004
Спеціальна частина
Пептиди та білки
Ферменти
Ферменти, або ензими,— біологічні каталізатори білкової природи, які присутні в усіх живих клітинах і беруть участь у біохімічних перетвореннях, направляють і регулюють тим самим обмін речовин в організмі.
Назва «фермент» походить від латин. fermentum — закваска, що асоціюється з природою процесів зброджування. Спочатку термін «фермент» вживався для визначення живих мікроорганізмів, що брали участь у зброджуванні, а для «ферментів-речовин», таких як пепсин, емульсин тощо, існувало поняття «ензим» (від грецьк. enzym — у заквасці). Однак пізніше з дріжджових клітин був виділений препарат ферменту і доведено, що ферментний каталіз може відбуватися поза живим організмом. Таким чином, відпала необхідність використання двох термінів «ензим» та «фермент» для визначення одного й того ж самого поняття, але обидві назви поширені і тепер вважаються синонімами.
Ферменти використовуються у різних галузях народного господарства, але доля тих, що застосовуються в медицині, невелика. Вони відрізняються високим ступенем очищення, складною і дорогою технологією одержання. Із відомих на теперішній час 3000 ферментів у медичній та мікробіологічній промисловості країн СНД для виготовлення ліків використовується близько 40. З них препаратів тваринного походження — 62 %, засобів з культур мікроорганізмів — 33 % і лише 5 % припадає на долю ензимів з рослинної сировини. Слід відзначити, що досягнутий у країнах СНД рівень розвитку і впровадження лікарських ферментних препаратів не може задовольнити існуючий на них попит. Взагалі арсенал ензимів, які використовуються в клінічній практиці, складає лише 10 % від відомих науці ферментів з встановленим терапевтичним ефектом.
Будова і класифікація
Особливості будови. Білкова природа ферментів підтверджена рентгеноструктурним аналізом. За складом амінокислот ферменти не відрізняються від білків: для них також характерні чотири рівні структурної організації молекули. Частіш за все ферменти побудовані з двох або більше пептидів, зв’язаних між собою нековалентно. Та наявність усіх чотирьох порядків структури макромолекули не завжди обов’язкова. Простіші ферменти, такі як лізоцим, трипсин, рибонуклеаза, не мають четвертинної структури.
У природі існують прості й складні ферменти. Перші цілком складаються з поліпептидів і під час гідролізу розпадаються виключно на амінокислоти (це, зокрема, пепсин, трипсин, папаїн, уреаза, лізоцим та ін.). Більшість ензимів відноситься до класу складних білків, які містять і небілковий компонент — кофактор, присутність якого є істотною для ферментної активності. Поліпептидну частину складного ензиму прийнято називати апоферментом. Складні ферменти з малою константою дисоціації, які під час очищення та виділення не розщеплюються на апофермент і кофактор, називаються холоферментами (холоензимами), а кофактор — простетичною групою. Під коферментом частіше розуміють кофактор, який при дисоціації легко відокремлюється від апоферменту. Один і той самий кофактор може виступати в ролі і простетичної групи, і коферменту. Типовими представниками коферментів є вітаміни. Деякі двовалентні метали (Са2+, Mg2+, Мn2+) виконують роль кофакторів. Доведена кофакторна функція таких біологічно активних речовин як HS-глутатіон. АТФ, ліноєва кислота, похідні нуклеозидів, порфіринвмісні речовини та ін.
При вивченні механізму ферментних реакцій було помічено, що молекули субстратів частіше мають невеликі у порівнянні з молекулами ферментів розміри. Звідси виникло припущення, що при утворенні ферментсубстратних комплексів в контакт з молекулою субстрату вступає обмежена кількість амінокислот поліпептиду, так званий активний центр. Під активним центром розуміють унікальну комбінацію амінокислотних залишків, яка забезпечує безпосередню взаємодію з субстратом і бере участь у реакції каталізу. Встановлено, що до активного центру входять простетичні групи. В активному центрі умовно розрізняють каталітичний центр, який вступає в хімічну взаємодію з субстратом, і зв'язуючий центр, або контактну («якірну») площадку, яка забезпечує специфічну спорідненість до субстрату і формування його комплексу з ферментом. Активний центр визначає каталітичну активність і специфічність ферменту, а для виявлення його дії має значення конфігурація всієї молекули. Порушення структури (це може бути денатурація) спричиняє часткове або повне руйнування активного центру і, як наслідок, втрату ферментом каталітичних властивостей.
Класифікацій. Всі ферменти згідно з класифікацією, прийнятою Комісією ферментів Міжнародної біохімічної спілки, поділяються на шість класів за типом реакції, які вони каталізують.
Оксидоредуктази — ферменти, які каталізують окислювально- відновні реакції і переносять електрони.
Трансферази — ферменти, які каталізують реакції перенесення різних функціональних груп від одного субстрату (донора) до іншого (акцептора).
Гідролази — ферменти, які каталізують розщеплення внутрішньомолекулярних зв’язків у субстратах з приєднанням води за схемою:
R—R'+ НОН → RH + R'OH
Ліази — ферменти, які каталізують розщеплення зв’язків, у тому числі й подвійних, без приєднання води.
Ізомерази — ферменти, які каталізують реакції ізомеризації.
Лігази (синтетази) — ферменти, які каталізують біосинтетичні процеси з’єднання молекул з використанням енергії АТФ.
Кожний з шести класів ферментів поділяється на підкласи, а підкласи, в свою чергу,— на підпідкласи. Окремий фермент, згідно з сучасною класифікацією, має назву і шифр. У шифрі перша цифра означає клас, друга — підклас, третя — підпідклас, четверта — даний конкретний фермент.
Поширення та локалізація найважливіших типів
Клас гідролаз (гідролітичних ферментів) включає більшість ферментів, які мають велике промислове або медичне застосування.
Підклас естерази (шифр 3.1.) — ферменти, які каталізують розщеплення і синтез складних ефірів відповідно до рівняння:
R—СОО—R1 + Н2O ⇆ R—СООН + R1—ОН
Серед естераз слід відмітити ліпази, які каталізують розщеплення і синтез жирів. В організмі людини і тварин найбільш активна ліпаза міститься в соку підшлункової залози. Здатність розщеплювати жири відмічається у багатьох рослин. Ліпаза міститься в насінні злаків, олійних культур, таких як соя, соняшник, бавовник, льон. У той же час насіння кропиви дводомної бідне на ліпазу, вона знаходиться переважно у вегетативних органах рослини. Можливість впливу ліпази повинна враховуватися при зберіганні рослинної сировини, що містить значну кількість олії. Підвищена вологість і температура активізує ліпазу, що веде до розщеплення жирів з утворенням гліцерину й вільних жирних кислот.
До групи естераз належить таназа, фермент, який каталізує гідроліз таніну. Вона має виключну специфічність дії — розщеплює тільки ті складні ефіри, в кислотному компоненті яких є не менш як два фенольних гідроксили.
Карбогідрази (шифр 3.2) є ферментами, які каталізують гідроліз і синтез гомо- та гетероглікозидів.
До карбогідраз належать а- і ß-амілази. Амілази розщеплюють крохмаль до декстранів і мальтози, яка є кінцевим продуктом при повному гідролізі крохмалю цими ферментами. Найбільш активні амілази містяться в слині і соку підшлункової залози людини і тварин. Цікаво, що насіння рослин розрізняється за вмістом у них а- і ß-амілази. Так, у непророслому зерні пшениці, жита і ячменю міститься лише ß-амілаза; а-амілаза утворюється в них тільки після проростання. В соєвих бобах як у пророслих, так і у непророслих міститься ß-амілаза.
ß-Фруктофуранозидаза (інвертаза, або сахароза) каталізує розщеплення сахарози на глюкозу і фруктозу. Цей фермент гідролізує зв’язок, який знаходиться при ß-глюкозидному атомі вуглецю залишку фруктози, в той час як а-глюкозидаза гідролізує зв’язок у сахарозі при а-глюкозидному атомі вуглецю залишку глюкози:
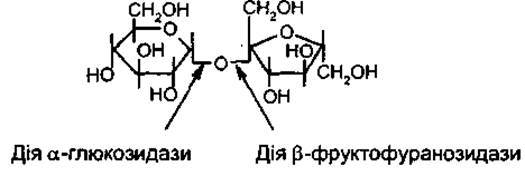
ß-Фруктофуранозидаза міститься в вищих рослинах, дріжджах, мікроорганізмах, травних соках тварин і людини, квітковому пилку.
Протеази (шифр 3.4), пептидгідролази — ферменти, які каталізують гідроліз пептидного зв’язку білків і поліпептидів згідно з рівнянням:
![]()
Протеази поділяють на дві групи: протеїнази (ендопептидази) і пептидази (екзопептидази). Протеїнази гідролізують білки до поліпептидів, а поліпептиди розщеплюються пептидазами до амінокислот.
Серед протеїназ необхідно відзначити травні ферменти — пепсин, трипсин, хімотрипсин.
Пепсин виділяється слизовою оболонкою шлунка. Він може бути отриманий у вигляді білкових кристалів з молекулярною масою 34 644. Молекула пепсину є одним поліпептидним ланцюгом, що складається з 327 амінокислотних залишків. Оптимум дії знаходиться в межах pH 1,2-1,5. Пепсин, окрім білка, здатний гідролізувати поліпептиди і дипептиди. Встановлено, що він переважно розщеплює лише ті пептидні зв’язки, в утворенні яких беруть участь аміногрупи тирозину і фенілаланіну. У клітинах слизової оболонки шлунка пепсин міститься у вигляді неактивного попередника — пепсиногену. Внаслідок дії на пепсиноген вільного пепсину і соляної кислоти він перетворюється на активний пепсин.
Трипсин міститься в соку підшлункової залози. Його молекулярна маса дорівнює 24 000. Молекула трипсину складається з 229 амінокислотних залишків. Оптимальна зона дії відповідає pH 8-9. Ступінь гідролізу білків під дією кристалічного трипсину приблизно відповідає дії кристалічного пепсину, однак неочищений трипсин має значно більшу каталітичну активність. Кристалічний трипсин каталізує гідроліз лише тих пептидних зв’язків, в яких бере участь карбоксильна група лізину або аргініну. Трипсин утворюється з неактивного трипсиногену під дією ентерокінази. А далі сам трипсин впливає на перетворення трипсиногену в трипсин.
У соку підшлункової залози міститься також неактивний фермент хімотрипсиноген. Під дією слідів трипсину він перетворюється на активну протеїназу —хімотрипсин, побудований з 242 амінокислот. Оптимум дії спостерігається при pH 7,5-8,5.
Протеїнази містяться також у деяких рослинах, типовим представником є папаїн. Його отримують з молочного соку динного дерева. Оптимальна зона дії ферменту знаходиться в слабкокислій, нейтральній й слабколужній реакціях середовища (залежно від природи білка-субстрату). Дія папаїну та інших протеолітичних ферментів рослинного походження активізується синильною кислотою і сульфгідрильними сполуками, які містять SH-групу, перш за все цистеїн та відновлений глутатіон.
Протеїнази типу папаїну знайдені в плодах і стеблах ананаса (Ananas comosus) — бромелаїн, а також у молочному соку рослин роду Ficus — фермент фіцин.
Амідази (шифр 3.5). До цієї групи гідролітичних ферментів належить уреаза, яка розщеплює сечовину до аміаку і вуглекислого газу:
CO(NH2)2+ Н2О = СО2 + 2NH3
Уреаза міститься в рослинах, пліснявих грибах і деяких бактеріях. Велика кількість уреази знайдена в насінні сої і конвалії мечовидної. Перспективним джерелом отримання цього ферменту є насіння кавуна.
Фізичні і специфічні властивості
Більшість ферментів — це глобулярні білки і лише деякі з них фібрилярні (наприклад, міозин). За формою глобулярні ферменти є «еліпсоїдами обертання». Молекулярна маса ферментів звичайно знаходиться в межах від 104 до 106. Найчастіше зустрічаються ферменти з молекулярною масою 20 000-60 000. Розмір молекул становить декілька десятків ангстрем.
Як і всі білки, ферменти мають амфотерність, електрофоретичну рухомість, не здатні до діалізу крізь напівпроникні мембрани, можуть зв’язувати значну кількість води (гідратуватися), легко висаджуються з водних розчинів солями або органічними розчинниками (ацетоном, етанолом), зберігаючи при цьому свої каталітичні властивості.
Ферменти відрізняються від хімічних каталізаторів виключно високою ефективністю дії (підвищують швидкість реакції у 1010 - 1013 разів) і специфічністю. Прийнято розрізняти абсолютну, абсолютну групову, відносну групову й оптичну специфічність. Абсолютна специфічність передбачає спорідненість тільки до одного субстрату. Абсолютна групова специфічність виявляється у дії на речовини, які схожі за типом будови і мають певний зв’язок. Відносна групова специфічність можлива у випадках, коли фермент виявляє специфічність до зв’язку між певними частинами молекули і абсолютно інертний до хімічної структури самої молекули. Оптична специфічність передбачає спорідненість ферменту до однієї стереоізомерної форми субстрату.
Методи виділення і визначення активності
Виділення. Ферментні препарати за джерелами їх одержання поділяють на ферменти, які отримують з тканин тварин або плазми крові людини; ферменти — продукти життєдіяльності мікроорганізмів; рослинні ферменти.
Сировиною тваринного походження можуть бути: підшлункова залоза забійної худоби (препарати трипсин, хімотрипсин, рибонуклеаза, пантрипін, панкреатин та ін.), слизова оболонка шлунка (пепсин, ацидинпепсин, абомін, пепсиділ), легені великої рогатої худоби (інгитрил), тканини серця великої рогатої худоби (цитохром С), сім’яники великої рогатої худоби (лідаза, ронідаза), природний шлунковий сік собак і коней (шлунковий сік), плазма крові людини (фібринолізин), білок курячих яєць (лізоцим). Відомо, що бджолиний мед має амілазну активність.
Використання тваринної сировини пов’язане з необхідністю переробки великої кількості тканин забійної худоби для отримання необхідної кількості ферментів, а також створення спеціальних умов зберігання сировини. Перспективним є отримання ферментних препаратів з культур мікроорганізмів, зокрема з пліснявих грибів, бактерій, дріжджів, актиноміцетів. Продуктами життєдіяльності мікроорганізмів є такі препарати як а-амілаза, L-аспарагіназа, ораза, солізим, стрептокіназа та ін. Мікробна сировина доступніша, а мікроорганізми здатні виробляти значну кількість різноманітних за дією ферментів. До недоліків мікробної сировини слід віднести великий обсяг підготовчих робіт: вибір поживного середовища вирощування штамів-продуцентів’ додержання оптимального режиму стерилізації, культивування, контроль за процесом.
Для одержання ферментів використовують також рослинну сировину: латекс динного дерева, насіння чорнушки, насіння кавуна, квітковий пилок тощо. У ряді випадків перевага цього виду сировини істотна: заготівля її технологічно простіша, матеріал можна висушити, подрібнити, компактно упакувати і зберігати тривалий час без створення спеціальних умов.
Виділення і очищення ферментних препаратів залежить від індивідуальних особливостей сировинного матеріалу, тому не є уніфікованими.
Перша стадія виділення внутрішньоклітинних ферментів тваринного і рослинного походження полягає в механічному руйнуванні клітин. Виділення ферментів з мікроорганізмів і субклітинних органел є проблемою. Це зумовлено високою міцністю клітинної оболонки мікроорганізмів і міцним зв’язком ферментів з органелами. У таких випадках використовують спеціальні методи гомогенізації: фізичні (високий тиск, ультразвук, іонізуюча радіація, заморожування-відтаювання), хімічні (дія кислот, лугів, солей, органічних розчинників), ензиматичні (дія літичних ферментів), біологічні (інгібування біосинтезу клітинної оболонки, дія фагів, антибіотиків).
Екстракцію ферментів проводять водою, розведеними розчинами кислот або лугів, буферними розчинами, органічними розчинниками (етанол, ацетон, діоксан тощо). Екстрагент підбирають індивідуально. Використовують також постадійну екстракцію різними екстрагентами.
Отримані екстракти забруднені баластними речовинами з різною молекулярною масою. Низькомолекулярні сполуки видаляють діалізом. Ліпіди екстрагують органічними розчинниками. Використовують кислотну, лужну або термічну денатурацію для переведення в нерозчинний стан баластних білків. Застосовують також осадження неактивних домішок солями важких металів.
Після попереднього очищення, а іноді й без нього, екстракт фракціонують. Для висадження ферментів використовують органічні розчинники (метанол, етанол, ізопропанол, ацетон, діоксан тощо), розчини солей, наприклад амонію сульфату. Для розділення і концентрування ферментних білків використовують різні методи хроматографії (адсорбційну, іонообмінну, афінну), гель-фільтрацію на сефадексах. Концентрують ферменти також ультрацентрифугуванням.
Спосіб і техніку кристалізації підбирають індивідуально для кожного' ферменту. Але кристалічний стан не є критерієм його гомогенності: кристали ферменту іноді можуть містити домішки інших речовин.
Структуру ферментів визначають методами хімічної модифікації, рентгенівського структурного аналізу, спектроскопії. Існує метод сайтспецифічного мутагенезу, який базується на заміні амінокислот у білковій частині молекули методами генної інженерії.
Визначення активності. Ферменти стандартизують за їх активністю. Визначення активності ферментів у біологічних об’єктах викликає деякі труднощі. Частіш за все це пов’язане з тим, що ферменти в тканинах присутні в дуже малих концентраціях. Про активність ферментів свідчить швидкість реакції, яку вони каталізують за певних умов вимірювання. При оптимальній температурі, pH середовища і повному насиченні субстратом швидкість реакції пропорційна концентрації ферменту, яку визначають за швидкістю зменшення субстрату або за швидкістю утворення продукту реакції.
Для вираження концентрації ферменту і кількісної оцінки його активності Комісія з ферментів Міжнародної біохімічної спілки рекомендувала міжнародну стандартну одиницю Е (або U). За одиницю активності будь-якого ферменту береться його кількість, яка в оптимальних умовах каталізує перетворення 1 мікромоля субстрату за хвилину (мкмоль/хв). У зв’язку з введенням Міжнародної системи одиниць (СІ) запропоновано нове визначення ферментної одиниці — катал (кат, kat). Катал — це активність ферменту, при якій реакція перебігає з швидкістю 1 моль за 1 секунду (1 моль/сек). 1 Е відповідає 16,67 нанокаталам (нкат). Обидві одиниці вимірювання застосовуються нарівні. Вимірювання одиниць активності проводять при температурі 25 °С, оптимумі pH і концентрації субстрату, що перевищує концентрацію насичення. За цих умов швидкість залежить тільки від концентрації ферменту.
У практичній роботі з ферментами часто використовують щільну і молярну активності. Щільна активність ферменту — це число одиниць ферментної активності на 1 мг білка (або число каталів на 1 мг активного білка). Число молекул субстрату, яке підлягає перетворенню однією молекулою ферменту за хвилину, прийнято називати числом обертів, або молярною активністю. Кожному ферменту властива своя молярна активність. Карбоангідраза є найактивнішим з усіх відомих ферментів. Її молекулярна активність дорівнює 36 млн.
Біологічна дія та застосування
Порушення метаболічних процесів в організмі людини, які викликані відсутністю або зміненням активності будь-якого ферменту, можуть бути зумовлені генетично (ензимопатії) або виникають внаслідок запальних процесів, травм, пухлин, оперативного втручання та ін. Лікування ферментами захворювань різної етіології здійснюється шляхом замісної терапії і використання ферментів у патологічному процесі.
З досвіду вітчизняної та закордонної ензимотерапії умовно визначають шість основних напрямків використання лікарських ферментних препаратів.
Замісна терапія захворювань шлунково-кишкового тракту. Використання ферментів при їх дефіциті у ШКТ сприяє засвоєнню поживних речовин, нормалізує секреторну діяльність. Наприклад, тритіказа — препарат, створений на основі розробленої в ДНЦЛЗ нової оригінальної рослинної субстанції з пророслого насіння пшениці (Triticum vulgare, род. Роасеае), містить амілолітичні ферменти (ß- і а-амілаза), а також β-галактозидазу, інвертазу, амінокислоти та мікроелементи. Гранули застосовують як засіб замісної терапії з амілолітичною і протизапальною дією для лікування розладів травлення, які виникли внаслідок недостатності функції ферментів, зокрема при хронічному панкреатиті різного походження.
Лікування гострих і хронічних запальних процесів і ран. Протеолітичні ферменти гідролізують залишки ушкоджених запаленням тканин, гнійні ексудати, виявляють протизапальну, фібринолітичну і ранозагоювальну дії. Крім того, ферменти здатні потенціювати дію антибіотиків та підвищувати їх концентрацію в крові й ушкоджених тканинах. Ферментний препарат лізоцим безпосередньо виявляє бактеріологічну дію, руйнуючи оболонки клітин мікроорганізмів. Препарати гіалуронідази (лідаза і ронідаза) сприяють розсмоктуванню рубців і спайок різного походження.
Ензимотерапія хвороб серцево-судинної системи. Лікарські засоби на основі протеолітичних ферментів поліпшують капілярну проникність кровоносних судин, забезпечують гіпотензивний і тромболітичний ефекти. У терапії тромбозів застосовують трипсин, хімотрипсин, террилітин, фібринолізин, стрептокіназу, стрептодеказу, целіазу. При порушеннях процесів тканинного дихання використовують препарат цитохром С.
Комплексна терапія онкологічних захворювань. Протеолітичні ферменти використовуються з кінця XIX ст. для лікування злоякісних пухлин. Під дією ензимів відбувається руйнування сітки, яка з’єднує пухлинні клітини між собою і з ендотелієм, протеоліз мембран ракових клітин, що призводить до зменшення і некрозу пухлини. У ферментотерапії злоякісних пухлин, крім протеаз і нуклеаз, використовують фермент L-аспарагіназу, який каталізує гідроліз незамінної для росту ракових клітин амінокислоти аспарагіну до аспарагової кислоти і аміаку. З дефіцитом аспарагіну гальмується ріст пухлинних клітин і утворення метастазів. L-Аспарагіназа використовується для лікування гострого лімфобластного лейкозу.
Лікування алергічних станів. Застосування антибіотиків пеніцилінового ряду супроводжується ризиком виникнення алергічних реакцій, а іноді й шокових станів. У цих випадках показано використання ферменту пеніцилінази. Цей інактиватор пеніцилінових антибіотиків гідролізує їх ß-лактамне кільце.
Використання ферментів як біохімічних реагентів. Іммобілізований фермент уреаза використовується в системі регенерації діалізу в апараті «штучна нирка». Каталізуючи гідроліз сечовини, уреаза активно сприяє очищенню крові від токсичних речовин.
Дані щодо активності деяких ферментів наведені в табл. 2 Додатків.
Активатори та інгібітори ферментів
При вивченні ферментних реакцій, які відбуваються в живих організмах, було виявлено, що активність ферментів визначається присутністю в середовищі активаторів та інгібіторів. Перші прискорюють реакцію, другі гальмують її. Активаторами ферментів можуть бути різноманітні хімічні речовини. Так, хлороводнева кислота активізує дію пепсину, жовчні кислоти — панкреатичної ліпази, папаїн активується сполуками, які містять вільні SH-групи (глутатіон, цистеїн). Особливо часто як активатори виступають іони дво- або одновалентних металів. Майже чверть усіх відомих ферментів мають потребу в металах для виявлення повної каталітичної активності.
Інгібіторами ферментів називають речовини, які викликають часткове або повне гальмування активності ферментів. Будь-які агенти, що викликають денатурацію білків, також спричиняють інактивацію ферменту, але подібне інактивування неспецифічне.
Практичне значення мають специфічні інгібітори. Вони застосовуються в ензимології для встановлення природи активного центру ферменту та його функціональних груп, для дослідження механізму каталітичних реакцій і взагалі для вивчення метаболічних процесів в організмі. З інгібуванням ферментів пов’язана дія багатьох токсинів. Так, відомо, що отруєння синильною кислотою відбувається внаслідок гальмування дихального ферменту цитохромоксидази. Останніми роками інгібітори ферментів знаходять використання при патологічних процесах з надмірною активністю ферментів в організмі.
Практично всі відомі інгібітори впливають на гідролітичні ферменти. Поки що в медицині використовуються інгібітори протеаз лише тваринного доходження, які мають поліпептидну природу (пантрипін, трієлін, трасилол, контрикал, гордокс та ін.) або синтетичні. У рослинах різних родин знайдений ряд інгібіторів гідролітичних ферментів, таких як протеази, амілази, ліпази. Біологічна роль цих інгібіторів до кінця не з’ясована.
Багаті на інгібітори трипсину і хімотрипсину рослини родин бобових, м’ятликових і пасльонових., Найчастіше білки-інгібітори містяться в насінні і локалізуються в алейронових зернах, ядрах, хлоропластах та мітохондріях клітин. У деяких рослинах вони знайдені в листках, стеблах, квітках, бульбах та ін. Вчені ДНЦЛЗ виділили з насіння сої (Glycine max, Fabaceae) інгібітор протеаз. Вивчається можливість застосування його як лікарського засобу. У результаті проведених досліджень у ДНЦЛЗ також розроблена технологія одержання з насіння пшениці інгібітору протеаз — інамілу. Препарат може бути використаний для клінічної діагностики захворювань ШКТ і як гіпоглікемічний засіб для лікування порушень вуглеводного обміну.
Інгібітори амілаз знайдені в запасаючих органах рослин, а також листках, плодах та проростках. Вони представлені білками або фенольними сполуками, зокрема танідами. Багаті на інгібітори амілаз види родин бобових, м’ятликових та чайних.
Природні інгібітори ліпаз, які були виділені з рослин, належать до класу білків або ліпідів і мають високу активність по відношенню до панкреатичних ліпаз. Інгібітори ліполітичних ферментів знайдені лише в насінні. Проходить клінічне випробування препарат брагузоль, одним з діючих речовин якого с інгібітор ліпаз з насіння рапсу ярового (Bral ssica пат pus var. oleifera). Препарат призначений для лікування інфекційних захворювань верхніх дихальних шляхів. Протизапальна властивість брагузоля забезпечується інгібітором ліпази, здатним пригнічувати активність ліполітичних ферментів у зоні формування запального процесу.