Фармакогнозія з основами біохімії рослин - Ковальов В. М. 2004
Спеціальна частина
Ефірні олії
Стероїди
Стероїди — органічні речовини рослинного і тваринного походження, в основі яких лежить тетрациклічне угрупування стеран, або циклопентанпергідрофенантрен. Фізіологічна дія різних стероїдів залежить від їхньої будови і просторового розміщення функціональних груп, які надають сполукам характерних хімічних властивостей.
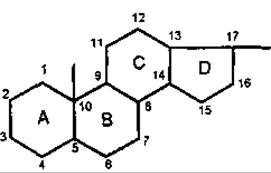
Стеран
Будова і класифікація
З точки зору стереохімії стеран може існувати у трьох просторових конфігураціях кілець А, В, С і D:
група 5 а-стероїдів має орієнтацію транс-транс-транс;
група 5 ß-стероїдів з конфігурацією цис-транс-транс;
група кардіостероїдів з цис-транс-цис розташуванням кілець, що відрізняє серцеві глікозиди від вказаних вище природних стероїдів, у яких кільця С/D займають транс-положення.
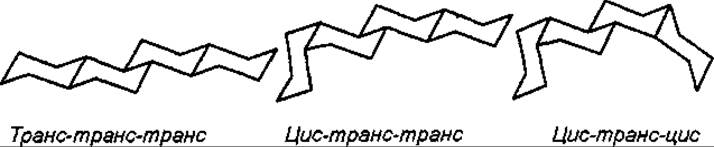
У залежності від характеру замісників у С-17 стероїди поділяють на стероли (холестерол, ерго- та фітостероли), жовчні кислоти, стероїдні гормони, стероїдні сапогеніни, кардіостероїди (геніни серцевих глікозидів), стероїдні алкалоїди (глікоалкалоїди), екдистероїди, вітаноліди та деякі інші сполуки рослинного походження.
Стероли
Формально стероли є похідними тетрациклічних тритерпенів. Стероли ссавців і грибів утворюються з ланостану. Всі вони мають аліфатичний ланцюг у позиції С-17, подвійний зв’язок і гідроксильну групу у С-3.
Стероли вищих рослин і водоростей також походять від ланостану, але їхнім біосинтетичним попередником є похідне циклоартану — циклоартанол. Для рослинних стеролів характерна присутність замісників у С-24 бічному ланцюзі, які вбудовуються у молекулу внаслідок реакцій трансметилювання.
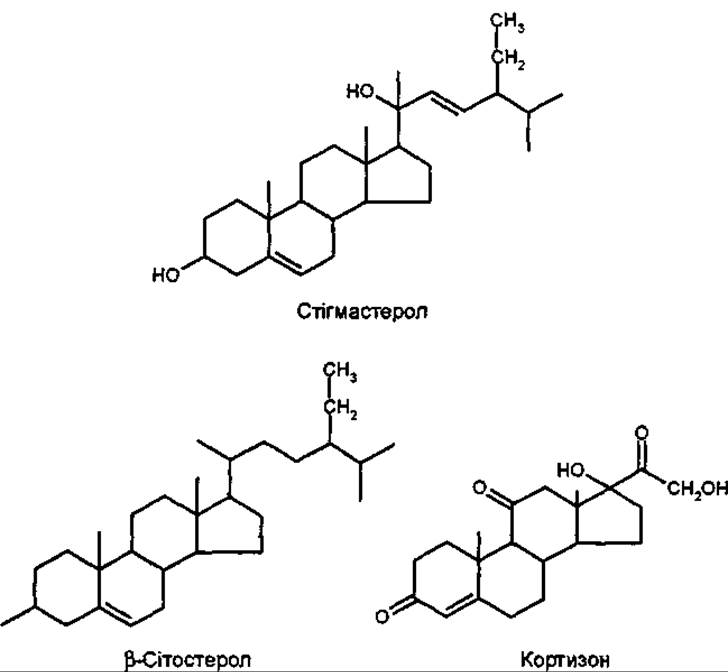
У рослинах знайдені стероли, які не мають додаткових алкільних груп у С-24. Наприклад, холестерол, головний стерол тварин, міститься у незначних кількостях у вищих рослинах і є переважаючим стеролом деяких червоних водоростей.
Особливістю рослинних стеролів є подвійний зв'язок, який часто міститься у бічному ланцюзі і має транс-конфігурацію. Стероли тваринного походження такого зв’язку не мають.
Стігмастерол вперше виділено з бобів фізостігми Physostigma venenosum Fabaceae (1906). У значній кількості він міститься в олії сої разом із сітостеролом. У залишку, що не вмилюється, їх сукупний вміст становить 15-20 %. Їх можна одержати як бічні продукти переробки цієї культури. Джерелами ß-сітостеролу і його глікозидів є корені кропиви, гарбузове насіння тощо. Головний стерол споринні — ергостерол, який міститься й в інших грибах, наприклад дріжджах (Saccharomyces cerevisiae), в кількості 0,1-0,7 %.
Стероли надходять до організму людини з їжею (жирні олії, буряк, селера тощо). Вони беруть участь у метаболізмі фосфатидів, мають певне фізіологічне значення як носії стероїдного угрупування подібного стероїдним гормонам, наприклад кортизону.
Стероїдні сапоніни
Сапогеніни стероїдних сапонінів—це похідні стерану з бічним пентациклічним кільцем у позиції С-17, що мають 27 атомів вуглецю (С-стероїди). Більшість сапогенінів пождать із стеролів, у яких бічний ланцюг зазнав метаболічних перетворень, внаслідок яких з’явилося спірокетальне у групування.
Стероїдні сапоніни відносять до двох типів: спіростану (монодесмозиди) та фуростану (бідесмозиди).
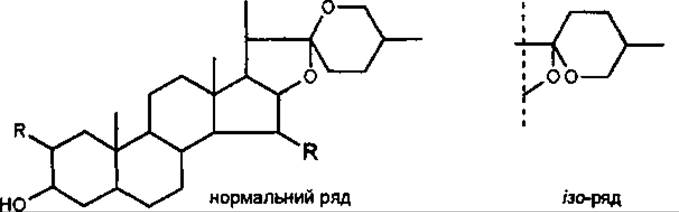
Спіростаноловий тип сапогеніну
Монодесмозиди мають шість циклів у стероїдній частині молекули: А, В, С, D, Е і F. Спіростанолові сапоніни можуть мати різну просторову орієнтацію спірокетального угрупування, внаслідок чого утворюється сапогенін нормального або ізоряду.
Бідесмозиди мають п’ять циклів: А, В, С, D і Е. Кільце F у них розімкнене, а спиртова група у С-27 етерифікована глюкозою. У процесі гідролізу бідесмозидів глюкоза відщеплюється. Вільна гідроксильна група сприяє замиканню бічного ланцюга у спірокеталь, тобто фуростанолові сапоніни можуть легко перетворюватися на спіростанолові.
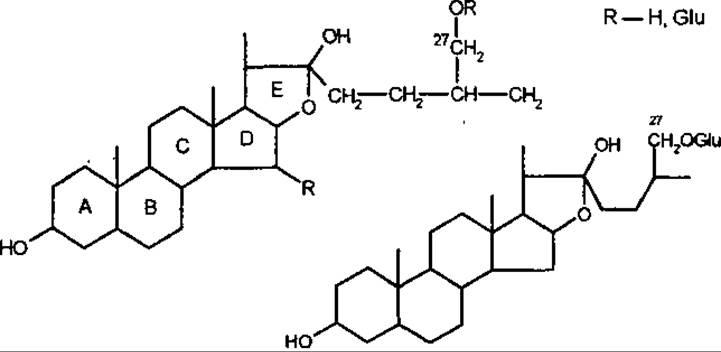
Фуростаноловий тип (бідесмозиди)
Сапогеніни мають ОН-групу у С-3 та G-16, а іноді у положеннях С-1, С-2, С-5. С-12. Особливістю будови, яка впливає на біологічну активність, є подвійний зв’язок в положенні С5-С6 (діосгенін). Групи СН3 частіше приєднані до С-10 та С-13.
Різноманіття стероїдних сапонінів пояснюється можливістю існування численних варіантів з’єднання та ізомеризації вуглеводних ланцюгів, які у спіростанолових глікозидів приєднані по С-3, а у фуростанолових — по С-27 положенню. Крім цього, сахара можуть приєднуватися й до інших вуглецевих атомів.
Сахарний компонент стероїдних сапонінів, який міститься у положенні С-3, має складнішу будову, ніж у серцевих глікозидів. В олігосахаридах буває до дев’яти моносахаридних залишків з лінійним з’єднанням або розгалуженням.
Відомі аналоги стероїдних сапонінів, які у спірокетальному угрупуванні містять азот замість кисню. Ці сполуки є похідними спіросалану. Вони виявляють лужні властивості та відносяться до глікоалкалоїдів.
Поширення у природі. Стероїдні сапоніни знайдені в обмеженій кількості родин — Lilaceae, Amaryllidaceae, Dioscoreaceae, Scrophulariaceae, Fabaceae, Ranunculaceae. Містяться вони й у деяких видах рослин Sołanaceae, Zygophyllaceae та Аrесасеае. На цей час відомо близько 35 стероїдних сапогенінів та понад 150 стероїдних глікозидів, сотня з яких належить до спіростанолового типу, а інші — фуростанолові. Дуже часто стероїдні сапоніни супроводжують у рослинах серцеві глікозиди.
Рослини, що синтезують сапогеніни, ростуть переважно у районах із сухим та жарким кліматом. Стероїдні сапоніни знайдені у листі наперстянки, кореневищах діоскореї, листі деяких видів агави та юки. Стероїдні сапоніни значно рідше зустрічаються у природі, ніж тритерпенові, але вивчені повніше.
Фізико-хімічні властивості та дослідження. Стероїдні сапоніни мають більшість властивостей, які притаманні тритерпеновим сапонінам: розчинність у воді, поверхнева та гемолітична активність. Водні розчини стероїдних сапонінів мають нейтральну реакцію, тому їх називають нейтральними сапонінами. Вони утворюють з вищими спиртами комплексні сполуки, що нерозчинні у воді. На відміну від тритерпенових сапонінів ця група сполук реагує з холестерином з утворенням нерозчинного у воді комплекса. Реакція має важливе значення для пояснення механізму фармакологічної дії стероїдних сапонінів.
Стероїдні сапоніни визначають за допомогою розподільної хроматографії (ПХ, ТШХ). Після висушування хроматограми обробляють розчином оцтового ангідриду у сірчаній кислоті.
Вміст стероїдних сапонінів визначають гравіметричним або фізико-хімічним методом. Аналіз поліспоніну-субстанції та лікарських (форм за ФС проводять ваговим методом після кислотного гідролізу суми глікозидів. Фотометричним методом визначають діосгенін після реакції з формальдегідом. З реактивом Саньє (розчин ваніліну у сірчаній кислоті) стероїдні сапоніни утворюють забарвлення, інтенсивність якого вимірюють на спектрофотометрі. Флуориметрично встановлюють величину УФ-флуоресценції похідних спіростану при проявленні на хроматограмах парами о-фосфорної кислоти.
Газорідинною хроматографією визначають вміст агліконів після реакції ацетилювання.
Біологічна дія та застосування. Стероїдні сапоніни в залежності від будови мають різну фармакологічну активність. Ті, що відносяться до спіростанолового ряду, діють фунгіцидно (чим більше сахарних залишків, тим сапоніни активніші). Ця ж група виявляє протипухлинну дію; сапоніни порушують функції ферментів, які регулюють окислювальне фосфорилювання у мембранах мітохондрій, що веде до загибелі аномальних клітин. Сила дії залежить від полярності аглікону; вуглеводна частина сприяє розчинності і транспорту сапонінів крізь клітинні мембрани. Особливо важливою властивістю стероїдних сапонінів є вплив на вміст холестерину у крові; препарати поліспонін, трибуспонін застосовують для лікування хворих на атеросклероз.
Стероїдні сапоніни виявилися найбільш економічною і доступною сировиною для напівсинтезу гормональних препаратів і в першу чергу, кортизону та його аналогів.
Повний синтез кортикостероїдів багатостадійний і малорентабельний, тому довгий час єдиним джерелом кортизону була кора надниркової залози великої рогатої худоби. Кількість цієї сировини не задовольняє потреби виробництва, тому вишукувались інші джерела стероїдних сполук.
Щоб підкреслити важливе промислове значення стероїдних сапонінів, достатньо відзначити, що 90 % усіх синтезованих гормональних препаратів виробляється з діосгеніну і близьких до нього стероїдних сапонінів рослинного походження. Джерелом отримання гормональних препаратів за кордоном є в основному різні види дюскореї, яка постачається з Мексики. Індії та інших країн. Україна досі не має власного виробництва кортикостероїдів.
Відомості про лікарську рослинну сировину і препарати, що містять стероїдні сапоніни, наведені в табл. 14 Додатків.