Фармакогнозія з основами біохімії рослин - Ковальов В. М. 2004
Спеціальна частина
Алкалоїди
Алкалоїди — це група органічних азотвмісних речовин, переважно рослинного походження, що мають лужний характер та високий фізіологічний вплив на організм людини і тварин.
Термін «алкалоїди» запропонував хімік-фармацевт В. Мейснер (W. Meissner) у 1819 р. Назва походить від двох слів: арабського alkali — луг і грецьк. eidos — вигляд, буквально — подібні до лугів. Вперше алкалоїд морфін виділено з опію на початку XIX ст.
Алкалоїди утворюються внаслідок вторинного обміну речовин. Всі вони містять азот, частіше у складі гетероциклічного кільця.
Присвоюючи назву алкалоїду, використовують видову або родову назву рослин-алкалоїдоносів з доданням суфікса «ін», наприклад, атропін з Atropa belladonna, стрихнін з Strychnos mix vomica, кокаїн — Erythroxylon coca. Іноді до назви алкалоїду додають префікс, щоб позначити інший алкалоїд з того ж рослинного джерела.
Типи класифікації
Класифікації алкалоїдів базуються на різних принципах. До останнього часу серед фахівців поширена модифікація класифікації О. П. Орєхова, заснована на побудові вуглецево-азотного скелета. Виділяють основні типи алкалоїдів, що містять азот за межами кільця або у складі гетероциклу: 1) піролідииу; 2) піперидину; 3) піридину: 4) піролізидину; 5) хінолізидину: 6) хіноліну; 7) ізохіноліну; 8) хіназоліну; 9) індолу; 10) дигідроіндолу, або беталаїну; 11) імідазолу. 12) акридину; 13) пурину; 14) ізопреноїдні алкалоїди, або псевдоалкалоїди; 15) екзоциклічні алкалоїди, або протоалкалоїди.
Алкалоїди ще систематизують за ботанічним або філогенетичним принципом, поєднуючи в одну групу всі сполуки, що виділені з рослин одного роду (наприклад, алкалоїд іпекакуани, кол- хіцинові алкалоїди, алкалоїди секурінеги тощо). Рослини, що близько розташовані в ботанічній систематиці, містять, як правило, близькі за будовою алкалоїди, утворюючи природну групу. Це спостерігається в ряді рослин з родин Solanaceae, Аросуnасеае, Papaveraceae. Філогенетичний принцип пошуку фізіологічно активних речовин допоміг О. П. Орєхову та його учням виявити понад 100 нових алкалоїдоносних рослин у флорі тоді ще СРСР.
Іноді алкалоїди поєднують за фармакологічними властивостями: алкалоїди — наркотичні анальгетики, м-холінолітики, алкалоїди, що збуджують ЦНС, та ін.
При розгляді алкалоїдів у курсі фармакогнозії використовується класифікація, яка бере до уваги шлях біосинтезу і відповідно до цього розподіляє їх на три групи:
істинні алкалоїди, що мають гетероциклічні кільця і біосинтетично походить з алкалоїдогенних амінокислот, або з кислоти нікотинової чи антранілової;
протоалкалоїди, що містять азот не у складі гетероциклів, але утворюються з амінокислот;
псевдоалкалоїди (ізопреноїдні алкалоїди), що утворюються без участі амінокислот і об’єднуються в групу незалежно від наявності гетероциклу (практично всі псевдоалкалоїди мають терпеноїдне походження).
Істинні алкалоїди утворюють групи сполук, до складу яких входять гетероцикли (табл. 14). Вони біогенетично походять від амінів, які утворюються внаслідок декарбоксилювання амінокислот.
![]()
На цей час відомі амінокислоти — біогенетичні попередники шести груп алкалоїдів:
до групи орнітину належать піролідинові, піролізидинові, тропанові і деякі піридинові алкалоїди;
лізин є попередником хінолізидинових алкалоїдів родини Fabaceae (тип лупінану) і деяких піперидинових алкалоїдів;
тирозин дає початок багатьом ізохіноліновим алкалоїдам;
триптофан — прекурсор індольних, хінолінових алкалоїдів цинхони, деяких піридинових та піперидинових алкалоїдів;
до біогенетичної групи гістидину належать імідазольні алкалоїди типу пілокарпіну;
з гліцину й аспарагінової кислоти будуються пуринові алкалоїди.
У синтезі деяких алкалоїдів бере участь нікотинова кислота.
Класифікація істинних алкалоїдів
Таблиця 14
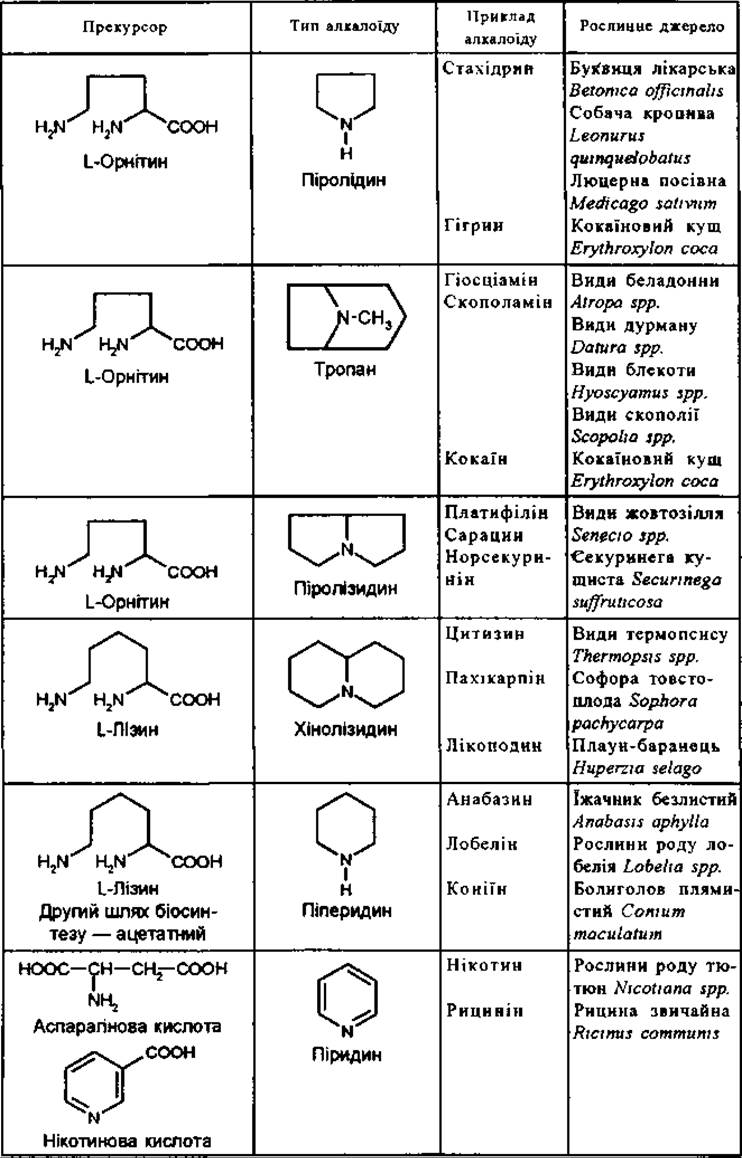
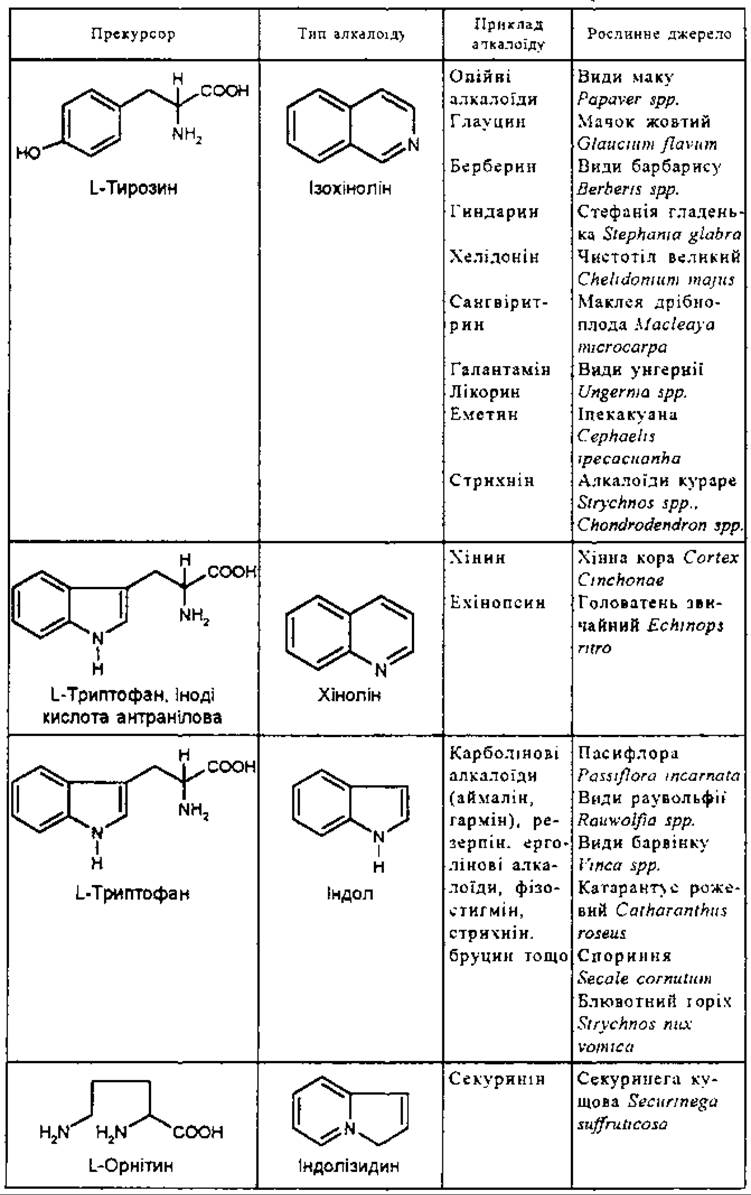
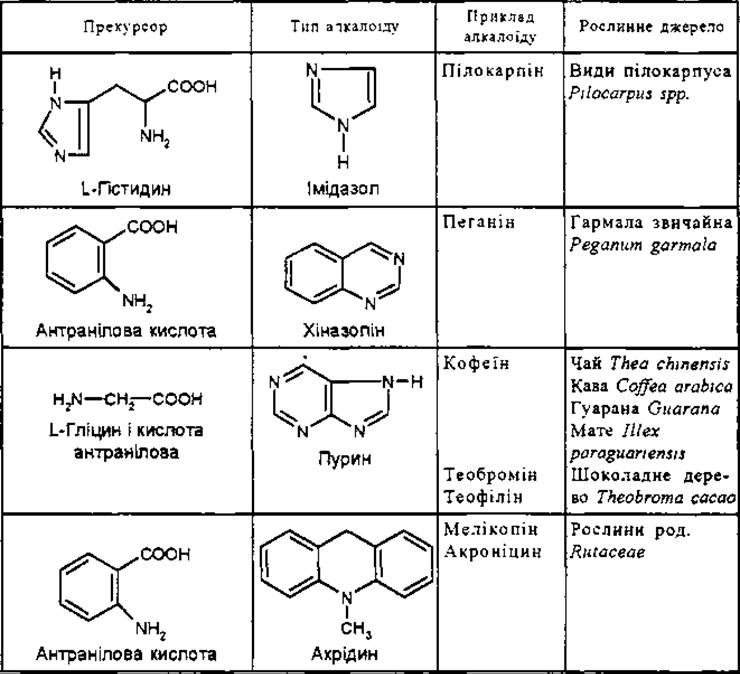
Біохімічна класифікація алкалоїдів не завжди дозволяє однозначно віднести той чи інший алкалоїд, особливо складної структури, до певної групи.
Біосинтез
Алкалоїди є продуктами азотистого обміну у рослинах і згруповані за формальним хімічним принципом — наявності в молекулі атома азоту. Попередниками істинних алкалоїдів і протоалкалоїдів є амінокислоти. У ролі прекурсорів виступають також антранілова та нікотинова кислоти, мультикарбонові одиниці (наприклад, ацетат) тощо. Вивчені шляхи біосинтезу протеїногенних амінокислот із пірувату СН3—СО—СООН (лізин, аланін), оксалоацетату (аспарагінова кислота), 2-оксоглутамінату (орнітин). Амінокислоти також утворюються у циклі Кальвіна або з шикімової кислоти. Між цими групами існують обмінні зв’язки.
Загальним для більшості алкалоїдів є наявність гетероциклів (піролідин, піперидин, піридин) чи поєднання цих простих гетероциклів з карбо- або іншими гетероциклами з утворенням складніших поліциклічних структур. Таким чином, основу будови алкалоїдів складає відносно невелика кількість структурних елементів, що синтезуються із загальних первинних прекурсорів.
Походження алкалоїдів має деякі універсальні риси, що експериментально доведено за допомогою специфічних мічених попередників, які вводили безпосередньо у рослину. Початковими реакціями біосинтезу у більшості випадків є декарбоксилювання, окислювальне дезамінування або переамінування амінокислот чи відповідних їм амінів. Далі звичайно йде пряме трансметилювання отриманих проміжних сполук, після чого відбувається циклізація аліфатичних ланцюгів попередників у різні гетеро- і карбоциклічні структури.
Універсальне значення мають реакції, які ведуть до утворення N-гетероциклічних структур, вони пов’язані з утворенням C-N-зв’язку. До цього призводять різні реакції, серед яких найважливішими є реакція утворення азометинів (шифових основ) і реакція типу конденсації Манніха.
Азометини можуть утворюватися спонтанно або ферментативно із сполук, що мають аміно- і карбонільні групи.
Реакції утворення С—N-зв’язку
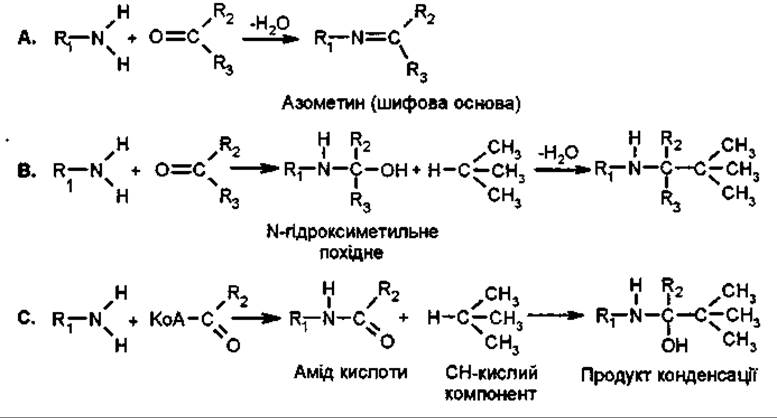
Аміни, які беруть участь в утворенні шиффових основ (А), звичайно синтезуються при декарбоксилюванні амінокислот. Карбонільні сполуки в багатьох випадках синтезуються внаслідок переамінування та окислювального дезамінування. При конденсації Манніха утворення С—N-зв’язку з тих самих функціональних груп проходить крізь проміжне створення N-гідроксиметильного похідного або кислого аміну в залежності від того, що використовують як карбонільну сполуку: альдегід (В) чи ацетил-КоА (С).
Процеси циклізації аліфатичних ланцюгів у гетероцикли на наступних етапах доповнюються процесами конденсації: окремі кільця поєднуються й утворюють складніші, іноді поліциклічні, структури. Бувають випадки коли утворення нових алкалоїдів поєднується з розщепленням (або розмиканням) раніше сформованих циклічних структур внаслідок розриву С—С-, С—N- чи С—О-зв’язків. Ускладнення скелета досягається внутрішньомолекулярними перегрупуваннями з розривом старих і утворенням нових С—С- і С—N-зв’язків.
Обмежені варіанти циклізації і перегрупувань при біосинтезі алкалоїдів у більшості випадків поєднуються з включенням функціональних груп і замісників на різних етапах метаболізму, що веде до виникнення у природі різноманітних структурних типів алкалоїдів.
Поширення та біологічні функції у рослинах
Відомо близько 6000 алкалоїдів, понад 50 з них виявлено у сировині тваринного походження. Алкалоїдоноси становлять понад 10 % усіх рослин. Алкалоїди рідко зустрічаються в нижчих рослинах (гриби Claviceps, Penicillium), серед голонасінних зустрічаються не часто (роди Ephedra та Taxus), серед покритонасінних розподіл нерівномірний. У порядках Salicales, Fagales, Cucurbitales та Oleales алкалоїди не знайдені. Більш за все вони поширені в родинах порядків: Caryophyllales (Chenopodiaceae), Magnoliales, Laurales, Ranunculales (Berberidaceae, Menispermaceae, Ranunculaceae), Papaverales (Pаpaveraceae, Fumariaceae), Rosales, Fabales, Rutales, Gentianales (Apocynaceae, Loganiaceae, Rubiaceae, Gentianaceae, Menyanthaceae, Asclepiadaceae), Convolvulales, Solanales, Campanulales (Companulaceae, Lobeliaceae), Asterales.
У ході еволюції вищі рослини виробили так звану метаболічну екстракцію, або можливість накопичення вторинних сполук поза метаболічними центрами — звичайно у вакуолях та клітинній стінці. Краще проілюструвати це на прикладі нікотину, який синтезується в коренях тютюнової рослини, а звідти надходить до листків, де й накопичується. Вторинні структурні модифікації часто відбуваються не там, де відбувається первинний синтез. Наприклад, циклічна система тропанових алкалоїдів формується в коренях дурману звичайного і звідти транспортується в листочки, де зазнає значних модифікацій.
Алкалоїди накопичуються головним чином у тканинах чотирьох типів: 1) у тих, що активно ростуть; 2) в епідермальних та гіподермальних; 3) в обкладці судинних пучків; 4) у латексних судинах. Алкалоїди знаходяться у вакуолях й тому не визначаються в молодих клітинах до вакуолізації. Вони рідко містяться в змертвілих тканинах, навіть у корі хінного дерева знаходяться виключно в паренхімі. Алкалоїди локалізуються переважно в певних органах рослин, наприклад, у хінного дерева — головним чином у корі, в аконіту — в бульбах, у кокаїнового куща — в листках, у болиголова — в плодах, у фізостигми — у насінні.
Алкалоїди, які знайдено у тварин, не завжди синтезуються самим організмом: іноді їх походження пов’язане з характером їжі. Так, бобри накопичують алкалоїд касторамін, який дуже близький до алкалоїду дезоксинуфарідину з кореневищ глечиків жовтих, і потрапляє він в організм тварин разом із їжею.
Як правило, в рослині міститься суміш декількох алкалоїдів, іноді до 15-20, часто близьких за будовою (в маткових ріжках, траві катарантуса рожевого тощо), однак у деяких рослин знаходять усього один алкалоїд (наприклад, рицинін у рицині).
Багато алкалоїдів, особливо складної будови, специфічні для певних родів і навіть родин, що використовуються в систематиці і класифікації. Вміст алкалоїдів у сировині звичайно складає десяті й соті долі відсотка й рідко досягає 10-15 % (кора хінного дерева).
Коливання вмісту алкалоїдів можливі при сушінні та зберіганні сировини. При повільному сушінні нестійкі алкалоїди (особливо складні ефіри) розкладаються. Наприклад, при швидкому сушінні протягом 5-6 год при температурі 60 °С листя дурману містить 0,54 % алкалоїдів, а після тривалого сушіння (7 діб у затінку) — тільки 0,35 %. Вміст алкалоїдів знижується при зберіганні сировини у вологих приміщеннях. Тривалий час біологічні функції алкалоїдів у рослинному світі були неясні. Частіш за все їх вважали кінцевими продуктами обміну речовин. Динаміка накопичення алкалоїдів у різних органах рослини є доказом їх використання як запасного азотистого матеріалу.
Пізніше було з’ясовано, що алкалоїди активно залучаються до обмінних процесів. Одна з теорій відводить їм роль рослинних гормонів та каталізаторів. Для доказу наводять факт існування N-оксидних форм алкалоїдів. При диханні рослин алкалоїд окислюється до пероксиду, який переходить до N-оксиду, а активний кисень використовується рослиною для подальшого фітохімічного процесу.
У підземних органах алкалоїди регулюють обмін речовин та ріст кореневої системи. Виділяючись у грунт, захищають рослину від грунтових бактерій, а можливо, й від поїдання тваринами, тобто вони — антифіданти.
Алкалоїди є сенсибілізаторами. Вони посилюють чутливість рослинних клітин до світла і прискорюють перебіг фази утворення й розвитку генеративних органів.
Через високі полярні властивості та розчинність у воді N-okсиди не видобувають при екстракції алкалоїдів неводними розчинниками. Можливо, такі форми алкалоїдів є артефактами, які утворюються при екстракції третинних алкалоїдів. Відомі N-оксиди піридинового, хинолізидинового, ізохінолінового, індольного ряду. Останні мають велике значення як галюциногени (резерпін, стрихнін).
Але яку б теорію не прийняли, все ж залишається невідомим, чому алкалоїди містяться тільки в деяких рослинах, а більшість може обходитися без них.
Фізико-хімічні властивості
У широкому розумінні алкалоїди є первинними (мескалін, тирамін), вторинними (ефедрин), третинними (атропін) амінами або похідними четвертинних амонієвих основ. Алкалоїди можна розглядати як складні похідні аміаку, в якому атоми водню заміщені радикалами:
![]()
Таким чином, алкалоїди можуть існувати у вільному стані (у вигляді основ) та у вигляді солей або алкалоїдів N-оксидів. Цей факт враховується при одержанні або виділенні алкалоїдів з рослинної сировини.
У рослинах алкалоїди містяться у формі солей органічних кислот: лимонної, щавлевої, янтарної, малонової, оцтової та ін. У лікарських препаратах це переважно гідрохлориди, нітрати, фосфати, іноді тартрати.
Розчинність, екстракція та розділення алкалоїдів залежать від форми знаходження їх у рослинній сировині. Алкалоїдні основи розчинні в органічних розчинниках (спирті, ефірі, хлороформі, бензолі та ін.) і, як правило, нерозчинні або мало розчинні у воді. Виняток становлять кофеїн, ефедрин, кодеїн, які розчинні у воді.
Солі алкалоїдів — білі кристалічні речовини, розчинні у воді і нерозчинні в органічних розчинниках (крім спирту). Розчинність у воді різна; наприклад, хініна сульфат — у співвідношенні 1:1000, а хініна гідрохлорид — усього 1:1. Деякі солі алкалоїдів (наприклад, папаверину гідрохлорид) розчинні в хлороформі.
Більшість алкалоїдів — тверді кристалічні сполуки, безбарвні або ледь забарвлені (наприклад, берберин жовтого кольору), гіркі на смак. До складу алкалоїдів входять атоми вуглецю, водню, кисню, азоту. Деякі алкалоїди не містять кисню (наприклад, коніїн з болиголова, нікотин, пахікарпін) і є рідинами, що переганяються з водяною парою, але солі цих алкалоїдів — тверді кристалічні сполуки.
Алкалоїди оптично активні. Ті, що обертають площину поляризованого променя ліворуч, більш фармакологічно активні. Ряд алкалоїдів в УФ-світлі мають характерну флуоресценцію.
Алкалоїди — досить слабкі основи. Константи дисоціації відомих алкалоїдів варіюються у значних межах, а їх солі мають різний ступінь стійкості. Алкалоїди з дуже малою величиною дисоціації не утворюють солей (кофеїн, колхіцин). До найсильніших основ відносять кодеїн (К = 9 ∙ 10-7), до найслабкіших — кофеїн (К = 4,1 ∙ 10-14). Алкалоїди у водних або водно-спиртових розчинах виявляють лужну реакцію. Звичайно pH водно-спиртових розчинів алкалоїдів не перевищує 8-8,5.
Алкалоїди з кислотами утворюють солі, причому один азот молекули приєднує один еквівалент одноосновної кислоти. По другому азоту приєднання йде важче, й такі алкалоїди, як правило, приєднують також один еквівалент одноосновної кислоти (стрихнін). Луги й розчин аміаку, а іноді карбонати й оксид магнію, розкладають солі алкалоїдів, витискуючи вільні основи.
Алкалоїди, які містять фенольний гідроксил, утворюють з лугами феноляти. Так, морфін випадає в осад під дією лугів, а потім розчиняється в їх надлишку, що дає можливість визначити його серед інших алкалоїдів. Алкалоїди, що є складними ефірами (атропін, кокаїн), під дією лугів омилюються.
Методи виділення та дослідження
Виділення. У рослинах алкалоїди знаходяться, як правило, групами (до 20 та більше), багато з них є схожими за хімічною будовою. Найчастіше виділяють суму алкалоїдів у вигляді солей або основ.
У рослинах головним чином знаходяться солі алкалоїдів. Для вилучення їх у вигляді основ рослинний матеріал спочатку обробляють слабким лугом — розчином аміаку або гідрокарбонатом натрію (сильні луги можуть зруйнувати деякі алкалоїди-ефіри). Далі екстрагують органічним розчинником, і алкалоїди-основи з супутніми речовинами переходять у розчин. Очищають, переводячи алкалоїди-основи в алкалоїди-солі і навпаки, доки органічний розчинник, що містить суму алкалоїдів-основ, не стане чистим.
Для розділення й очищення алкалоїдів використовують хроматографічні методи.
Рослинну сировину, яка містить алкалоїди-основи, обробляють водою та спиртом, до яких додають виннокам’яну кислоту для переведення усіх алкалоїдів у солі. Крім алкалоїдів, у розчин переходить велика кількість екстрактивних речовин: білків, смол, дубильних речовин тощо. Для очищення від супутніх домішок кислий витяг підлужують, алкалоїди-основи, що утворилися при цьому, вилучають відповідний органічним розчинником, до якого додають 1-5 % розчин кислоти. Алкалоїди-основи знов стають солями, які переходять у водно-кислий шар, а усі ліпофільні сполуки залишаються в органічному розчиннику.
Рідкі й леткі алкалоїди (нікотин, коніїн) одержують шляхом перегонки з водяною парою.
Зберігають сильнодіючу алкалоїдоносну сировину за списком Б. Виняток — бульбоцибулини пізньоцвіту і насіння чилібухи, які зберігають за списком А. Робота з цією токсичною сировиною потребує додержання певних правил безпеки.
Якісні реакції. Виявляють наявність алкалоїдів у рослинній сировині загальноосадовими реакціями, внаслідок яких утворюються важкорозчинні у воді осади (комплекси). Найчастіше застосовують такі реактиви: Майєра (розчин дихлориду ртуті та йодиду калію) — кремовий осад; Вагнера й Бушарда (розчин йоду в калію йодиді) — червоно-брунатний осад; Хагера (насичений розчин пікринової кислоти) — жовтий осад; Драгендорфа (розчин нітрату вісмуту основного в калі10 йодиді) — червоно-брунатний осад, а також свіжозготовлений розчин таніну, розчини фосфорномолібденової і фосфорновольфрамової кислот.
Слід враховувати, що ці реактиви дають осади з протеїнами, а кофеїн і деякі інші пуринові алкалоїди осадів не утворюють.
Для виявлення алкалоїдів використовують також реакції забарвлення з концентрованими неорганічними кислотами — азотною, сірчаною або їх сумішами. Й основу реакцій покладені особливості хімічної структури алкалоїдів, тому вони можуть виступати як специфічні для визначення груп алкалоїдів. Реакції забарвлення проводять як із чистими алкалоїдами, так і з їх сумішами в сухому вигляді.
Специфічні реакції. Кофеїн та інші пуринові алкалоїди визначають за допомогою мурексидної проби — утворюється червоно-пурпурове забарвлення. Колхіцин з мінеральними кислотами дає жовте забарвлення. При взаємодії алкалоїдів групи індолу (наприклад, алкалоїдів маткових ріжок) з 60 % сірчаною кислотою та n-диметиламінобензальдегідрм розчин набуває синьо-фіолетового або червоного кольору. Для тропанових алкалоїдів використовують реакцію Віталі — Морена. Її модифікація дозволяє визначити кокаїн по утворенню пурпурового забарвлення.
Алкалоїди, які містять фенольну групу (морфін), дають синє забарвлення з хлоридом заліза. Ванілін є реактивом на індольний цикл. Характерні кольорові реакції дають нітропрусид натрію з пілокарпіном, теофіліном, пахікарпіном, сферофізином.
Інколи для ідентифікації алкалоїдів використовують процес гідролізу з наступним виявленням артефактів. Так, фізостигмін при гідролізі у лужному середовищі утворює метиламін, сферофізин виділяє аміак. Кокаїн під дією концентрованої сірчаної кислоти розщеплюється на метиловий спирт та бензойну кислоту з подальшим утворенням метилового ефіру бензойної кислоти, який визначається за запахом.
Для виявлення і визначення якісного складу та кількості алкалоїдів часто використовують паперову та тонкошарову хроматографію в сумішах різних розчинників, головним чином кислих. Звичайно алкалоїди в УФ-світлі флуоресціюють блакитним, зеленим або жовтим кольором. При обробці хромогенними реактивами флуоресценція плям, як правило, змінюється й часто з'являється забарвлення, яке можна бачити при денному світлі.
Ідентифікацію алкалоїдів також проводять за допомогою фізико-хімічних методів: ультрафіолетової, інфрачервоної, ЯМР- і ПМР-спектроскопії.
Кількісне визначення. Для кожної сировини розробляють індивідуальну методику визначення вмісту алкалоїдів. Усі вони багато-етапні внаслідок тривалого очищення.
Довгий час кількісне визначення алкалоїдів проводили ваговим або об’ємним способом, тепер кількість алкалоїдів у сировині визначають фізичними, фізико-хімічними та об’ємними методами.
Найбільш поширена титрометрія: 1) пряме титрування алкалоїдів розчином кислоти; 2) зворотне титрування надлишку кислоти розчином лугу; 3) пряме титрування алкалоїдів розчином йоду або іншого комплексоутворюючого реактиву, при взаємодії з яким алкалоїди утворюють нерозчинні сполуки.
Більшість алкалоїдів визначають титруванням у неводних розчинниках (пахікарпін. тропанові алкалоїди, кокаїн, платифілін. Сальсолін, морфін, резерпін, сферофізин, ефедрин та ін.). Титрантом є розчин хлорної кислоти в оцтовій кислоті. Солі алкалоїдів титрують хлористоводневою, йодистоводневою та бромистоводневою кислотами в присутності ацетату ртуті.
Деякі алкалоїди (кофеїн та його солі) кількісно можна визначити за утворенням нерозчинних солей, наприклад, полійодидів. Надлишок йоду у фільтратах визначають титруванням тіосульфатом натрію. Алкалоїди пуринового ряду (теобромін, теофілін) утворюють солі з нітратами. Еквівалентну кількість азотної кислоти, що утворилася, визначають титруванням.
Багато алкалоїдів визначають методами фотометрії, спектрофотометрії. фотонефелометрії, полярографії, поляриметрії та іншими фізико-хімічними способами.
Біологічна дія та застосування
Стисло описати усі види фармакологічної активності алкалоїдів неможливо. Висвітлимо деякі з них. Механізми дії деяких алкалоїдів на організм людини добре вивчені. Ці речовини діють на специфічні рецептори або впливають на активність ферментів.
Рецептори отримали свою назву завдяки чутливості до природних медіаторів та їхніх антагоністів. Наприклад, чутливі до ацетилхоліну рецептори називають холінергічними, чутливі до адреналіну — адренергічними. У свою чергу холінергічні рецептори поділяють на м-холінорецептори (ті, що чутливі до мускарину) та н-холінорецептори (чутливі до нікотину ). Відомі різні підтипи адренергічних рецепторів, що позначаються літерами a1, а2, b1, b2. Виділяють H1- і Н2-гістамінові. дофамінові. серотонінові, опіоїдні та ін. Стимуляція або блокада рецепторів (у тому числі природними алкалоїдами чи синтетичними аналогами і похідними) призводить до попередження, а також лікування патологічних станів.
Алкалоїди досить сильно впливають на активність ферментів. Дія деяких з них пов’язана з індукцією або зниженням активності ензимів. Наприклад, фізостигмін, неостигмін та інші антихолінестеразні засоби знижують активність ацетилхоліну.
Алкалоїдианалептики безпосередньо або рефлекторно збуджують життєво важливі центри довгастого мозку. Їх застосовують при станах, що пов’язані з пригніченням ЦНС, при асфіксії, колапсі, серцевій недостатності тощо.
Накопичений десятиріччями досвід медичного використання алкалоїдів перевіряється експериментально, що веде до створення нових лікарських засобів. Відомості про рослинну сировину та лікарські препарати, які містять алкалоїди, наведені в табл. 16 Додатків.