Химия белка. Структура, свойства, методы исследования - Шендрик А.Н. 2022
Синтез пептидов
Защита карбоксильной группы
Этерификация
Основная цель защиты по карбоксильной группе сводится не только в ее блокированию, но и к разрушению цвиттерионной формы аминокислоты. Наиболее простой способ защиты карбоксильной группы - этерификация. Другие пути - это образование амида или гидразида. Последние два способа применяются относительно редко, из-за возникающих впоследствии сложностей со снятием защитной группы.
Метиловые и этиловые эфиры. Методика этерификации аминокислот сводится к обработке их избытком соответствующего спирта в присутствии кислоты как катализатора (HCl, тионилхлорид - SOCl2и др.). Существенных, с позиций пептидного синтеза, различий между этиловыми и метиловыми эфирами аминокислот нет.
Метиловые и этиловые эфиры N-защищенных аминокислот получают введением N-защитной группы в эфир, а не наоборот.
По завершению пептидного синтеза эфирные группировки расщепляют щелочным гидролизом. По мере удлинения пептидной цепи гидролиз эфиров затрудняется и требует более жестких условий проведения реакции. Это, в свою очередь, повышает вероятность рацемизации. Поэтому, в таких случаях, щелочной гидролиз заменяют кислотным.
Трет-бутиловые эфиры аминокислот и пептидов исключительно легко расщепляются кислотами, что делает их более предпочтительными перед метиловыми и этиловыми эфирами. Известно несколько способов получения трет-бутиловых эфиров аминокислот.
> В реакции этерификации свободных аминокислот с изобутиленом. Катализатор - серная кислота; растворитель - диоксан:
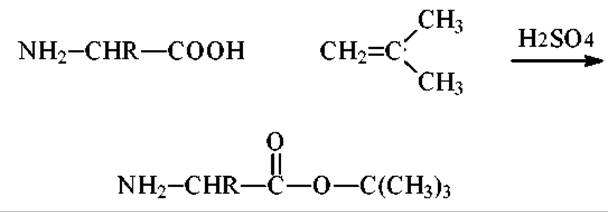
> В реакции переэтерификации свободных аминокислот трет-бутилацетатом. Катализатор - хлорная кислота:
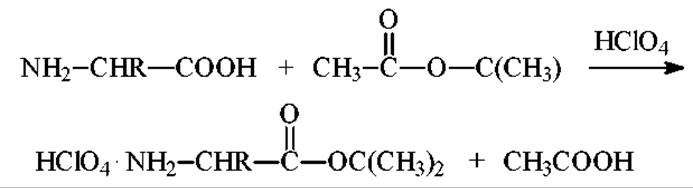
> В реакции N-защищенных ааминокислот с трет-бутанолом и хлорокисью фосфора в присутствии избытка пиридина.
Трет-бутиловые эфиры большинства аминокислот - устойчивые жидкости. Перегоняются без разложения. Не вступают в реакцию самоконденсации при хранении. Очень устойчивы к гидразинолизу и аминолизу.
Расщепляют трет-бутиловые эфиры хлористым водородом в этилацетате или хлористом метилене; толуолсульфокислотой в бензоле; трифторуксусной кислотой. Последнюю особенно часто используют при синтезе фрагментов биологически активных пептидов.
Бензиловые эфиры аминокислот получают по реакции хлоргидратов хлорангидридов аминокислот с бензиловым спиртом:
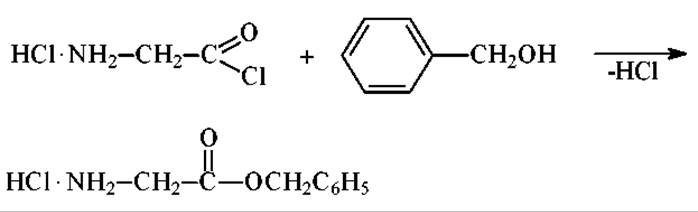
Выходы реакции, как правило, невелики.
При использовании в реакции незамещенных аминокислот процессу способствует бензилборат, связывая образующуюся воду.
Бензиловые эфиры можно получить также по реакции аминокислот с 5-10 кратным избытком дибензилсульфита в присутствии п-толуолсульфокислоты. Этот метод неприменим к аланину, лизину и пролину.
Расщепляют бензиловые эфиры ааминокислот и пептидов каталитическим гидрогенолизом в присутствии Pd. Избирательный гидрогенолиз бензиловых эфиров в присутствии карбобензоксигруппы невозможен. Бензиловые эфиры можно расщепить также действием натрия в жидком аммиаке. Крайне редко используется щелочной гидролиз бензиловых эфиров.
Модифицированные бензиловые эфиры
п-Нитробензиловые эфиры аминокислот получают кипячением карбобензоксиаминокислот с п-нитробензилбромидом или п-нитробензилхлоридом в этилацетате. Катализатор - третичный амин (X - карбобензоксигруппа). Карбобензоксигруппу отщепляют от продукта реакции бромистым водородом в ледяной уксусной кислоте.
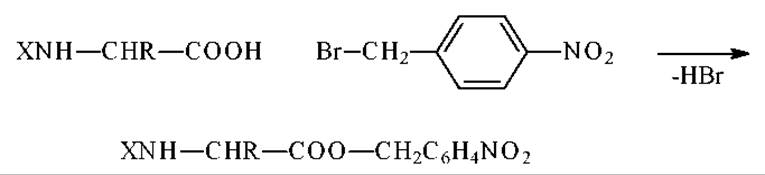
Второй метод получения п-нитробензиловых эфиров - этерификация свободных аминокислот п-нитробензиловым спиртом в присутствии толуолсульфокислоты в четыреххлористом углероде.
Третий способ - взаимодействие натриевых или триалкиламмониевых солей карбобензоксиаминокислот с п-нитробензиловым эфиром п-толуолсульфокислоты.
Для расщепления п-нитробензиловых эфиров прибегают к щелочному гидролизу или каталитическому гидрогенолизу.