БИОХИМИЯ - Л. Страйер - 1984
ТОМ 1
ЧАСТЬ I. КОНФОРМАЦИЯ И ДИНАМИКА
ГЛАВА 6. ВВЕДЕНИЕ В ЭНЗИМОЛОГИЮ
6.21. При связывании субстратов с ферментами образуются строго ориентированные водородные связи
Несмотря на то что многие субстраты не имеют заряда, они связываются с ферментами с высокой степенью специфичности и сродства. Основной вид взаимодействия таких субстратов, а также большинства заряженных субстратов с ферментами - это образование водородных связей. В водородной связи атом водорода связан сразу с двумя другими атомами. Тот атом, с которым водород связан более прочно, называют донором водорода, тогда как второй атом-акцептором водорода. По существу, водородную связь можно рассматривать как промежуточное взаимодействие, возникающее при переносе протона от кислоты к основанию. Атом-акцептор должен иметь частичный отрицательный заряд, который и притягивает водород. Короче говоря, водородная связь чем-то напоминает любовь втроем:
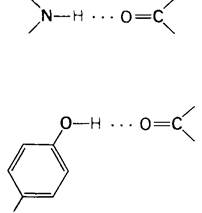
При образовании водородных связей в биологических системах атомами-донорами служат атомы азота или кислорода, ковалентно связанные с атомом водорода. Роль атомов-акцепторов выполняют кислород или азот. Типы водородных связей и их длины приведены в табл. 6.3. Энергия связей колеблется от примерно 3 до 7 ккал/ моль. Водородные связи прочнее, чем связи, обусловленные вандерваальсовыми взаимодействиями, но значительно слабее, чем ковалентные связи. По длине водородные связи занимают промежуточное положение между ковалентными связями и связями, обусловленными вандерваальсовыми взаимодействиями. Важная особенность водородных связей состоит в том« что их энергия зависит от геометрии. Водородная связь оказывается наиболее сильной, если донор, водород и акцептор лежат на одной прямой. Если же атом-акцептор расположен под углом по отношению к линии, соединяющей атом-донор и водород, то связь будет тем слабее, чем больше этот угол:

Таблица 6.3. Типичные размеры водородных связей

Мы уже упоминали о водородных связях при обсуждении структуры миоглобина и гемоглобина. В α-спирали водородная связь соединяет друг с другом —NН- и —СО-группы пептидной цепи. При этом атом азота служит донором водорода, а атом кислорода-акцептором. Расстояние между атомами азота и кислорода составляет 2,9 А; атом водорода находится ближе к азоту, чем к кислороду, на 0,9 А.
Другой пример водородной связи в миоглобине и гемоглобине - связь между гидроксильной группой тирозина НС2 и пептидным карбонилом FG4. Атом кислорода в гидроксильной группе тирозина является донором водорода, а атом кислорода в пептидной С=O-группе-акцептором :
Роль водородных связей во взаимодействии субстрата с ферментом хорошо видна на примере связывания уридинсодержащей части субстрата с панкреатической рибонуклеазой - ферментом, расщепляющим рибонуклеиновую кислоту (рис. 6.25). В этом случае образуются три водородные связи.
Рис. 6.25. Образование водородных связей при связывании субстрата рибонуклеазой
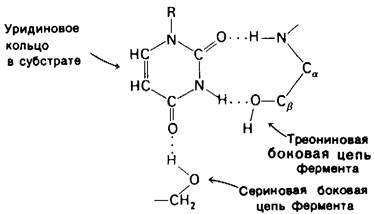
1. Одна из С—О-групп уридинового кольца соединена водородной связью с N—Н-группой пептидной цепи.
2. N—Н-группа уридинового кольца соединена водородной связью с —ОН-груп- пой остатка треонина.
3. Другая С=O-группа уридинового кольца соединена водородной связью с —ОН-группой остатка серина.
6.22. Белки обладают выраженной способностью к образованию водородных связей
Боковые цепи аминокислот и основная пептидная цепь могут давать большое число различных водородных связей. Так, из 20 встречающихся в белках аминокислот у 11 боковые цепи способны участвовать в образовании водородных связей. Удобно распределить эти аминокислоты на группы в зависимости от образуемых ими типов водородных связей.
1. Боковые цепи триптофана и аргинина могут служить только донорами водорода:
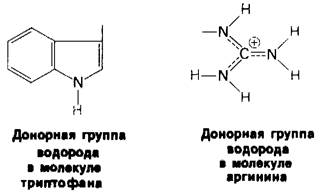
2. Боковые группы аспарагина, глутамина, серина и треонина могут служить как донорами, так и акцепторами водорода, и в этом отношении они подобны пептидной группе.
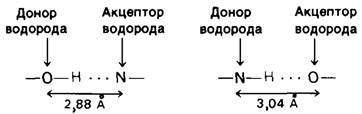
3. Способность образовывать водородные связи у лизина (и вообще у соединений с концевыми аминогруппами), у аспарагиновой и глутаминовой кислот (и у других соединений с концевыми карбоксильными группами), а также у пиридина и гистидина зависит от pH. В определенных границах pH они могут служить одновременно и донорами, и акцепторами водорода, тогда как при других значениях pH - либо донорами, либо акцепторами, как это показано для аспартата и глутамата на рис. 6.26. Иными словами, образуемый этими ионизирующимися остатками тип водородной связи зависит от pH.
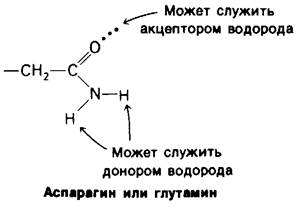
Рис. 6.26. Способность аспартата и глутамата к образованию водородных связей