БИОХИМИЯ - Л. Страйер - 1984
ТОМ 1
ЧАСТЬ I. КОНФОРМАЦИЯ И ДИНАМИКА
ГЛАВА 2. ОСНОВНЫЕ ПРЕДСТАВЛЕНИЯ О СТРУКТУРЕ И ФУНКЦИИ БЕЛКОВ
2.3. Аминокислоты, соединяясь пептидной связью, образуют полипептидные цепи
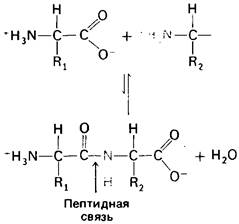
В белках α-карбоксильная группа одной аминокислоты соединена с α-аминогруппой другой аминокислоты пептидной связью (называемой также амидной связью). На рис. 2.17 показано, как из двух аминокислот образуется дипептид с высвобождением одной молекулы воды. Равновесие этой реакции сильно сдвинуто в сторону гидролиза, а не синтеза. Следовательно, биосинтез пептидных связей требует притока свободной энергии, тогда как гидролиз идет с высвобождением энергии.
Рис. 2.17. Образование пептидной связи
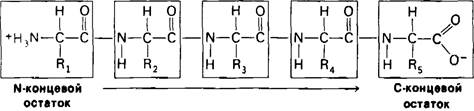
При соединении большого числа (обычно более сотни) аминокислот путем образования пептидных связей формируется полипептидная цепь, имеющая неразветвленную структуру (рис. 2.18). Каждую аминокислоту, входящую в состав полипептида, называют аминокислотным остатком. Полипептидная цепь имеет определенное направление, поскольку каждый из ее строительных блоков имеет разные концы-либо α-ами- но-, либо α-карбоксильная группа. Условились считать, что полипептидная цепь начинается с N-конца, т. е. с конца, несущего аминогруппу. При изображении последовательности аминокислот в полипептидной цепи начинают с N-концевого остатка. Так, в трипептиде аланин-глицин-триптофан аланин несет концевую аминогруппу, а триптофан-концевую карбоксильную группу. Обратите внимание, что триптофан- глицин-аланин-это уже другой трипептид.
Рис. 2.18. Пентапептид. Каждый аминокислотный остаток выделен рамкой. Пептидная цепь начинается с аминоконца
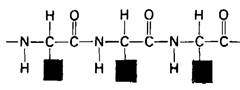
Полипептидная цепь состоит из регулярно повторяющихся участков, образующих основную цепь, и вариабельной части, включающей в себя характерные боковые цепи (рис. 2.19). Основную цепь называют иногда скелетом, или остовом, молекулы.
Рис. 2.19, Полипептидная цепь состоит из скелета, имеющего регулярную, повторяющуюся структуру, и отдельных боковых цепей (R1, R2, R3; показаны зеленым)
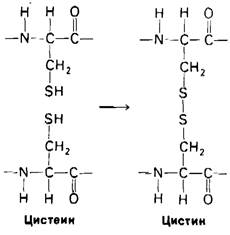
В ряде белков отдельные боковые цепи соединены между собой дисулъфидными связями (мостиками), которые образуются при окислении остатков цистеина. Возникающий при этом дисульфид называется цистином (рис. 2.20). Каких-либо других ковалентных связей в белках обычно не встречается.
Рис. 2.20. Дисульфидный мостик (— S — S —) образуется из сульфгидрильных групп (— SН) двух остатков цистеина. Продуктом реакции является остаток цистина