БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ II ГЕНЕРИРОВАНИЕ И ХРАНЕНИЕ МЕТАБОЛИЧЕСКОЙ ЭНЕРГИИ
ГЛАВА 11 МЕТАБОЛИЗМ: ОСНОВНЫЕ ПОЛОЖЕНИЯ И ОБОЗНАЧЕНИЯ
11.4. ATP-универсальная энергетическая валюта в биологических системах
Живые существа нуждаются в постоянном притоке свободной энергии для выполнения трех основных задач: 1) для преобразования механической работы в мышечное сокращение и другие формы клеточных движений, 2) для активного транспорта молекул и ионов и 3) для синтеза макромолекул, а также других биомолекул из простых предшественников. Используемая в этих процессах свободная энергия, которая поддерживает организм в состоянии, далеком от равновесия, поступает из окружающей среды. Хемотрофы получают эту энергию путем окисления пищевых веществ, тогда как фототрофы получают ее. улавливая световую энергию. Свободная энергия, высвобождающаяся при окислении питательных веществ и извлекаемая из световой энергии, прежде чем быть использованной в процессах движения, активного транспорта и биосинтеза, частично преобразуется в специальную форму. Таким специальным носителем свободной энергии, своего рода энергетической валютой, является аденозиптрифосфат (АТР). Центральную роль АТР в обмене энергии в биологических системах раскрыли Фриц Липман и Герман Калькар (Fritz Lipmann, Herman Kalkar) в 1941 г,
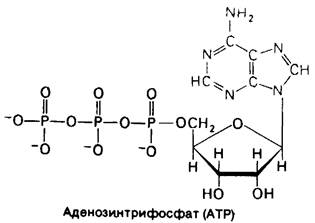
АТР-нуклеотид, состоящий из остатков аденина, рибозы и трифосфата (рис. 11.2; обсуждение номенклатуры нуклеотидов см. в разд. 22.1). Активная форма АТР - это обычно комплекс АТР с Mg2 + или Мn2+. Говоря о роли АТР как носителя энергии, мы фокусируем внимание на ее трифосфатном компоненте. АТР-молекула, богатая энергией, поскольку ее трифосфатный компонент содержит две фосфоангидридные связи. При гидролизе АТР до аденозиндифосфата (ADP) и ортофосфата (Рi) или до аденозинмонофосфата (АМР) и пирофосфата (PPi) высвобождается большое количество свободной энергии. ∆G0 для этих реакций зависит от ионной силы среды и от концентрации Mg2+ и Са2+. Мы будем использовать величину-7,3 ккал/моль. При условиях, существующих в клетке в норме, фактическое значение ∆G для этих процессов гидролиза составляет около — 12 ккал/моль.
Рис. 11.2. Аденозинтрифосфат состоит из остатков аденина (синий цвет), рибозы (желтый цвет) и трифосфата (красный цвет)
АТР + Н2O ⇄ ADP + Рi + Н+
∆G0 = - 7,3 ккал/моль,
АТР + H2O ⇄ АМР + РРi + Н+
∆G0 = - 7,3 ккал/моль.
АТР, АМР и ADP могут превращаться друг в друга. Фермент аденилаткиназа (называемый также миокиназой) катализирует реакцию
АТР + AMP ⇄ ADP + ADP.
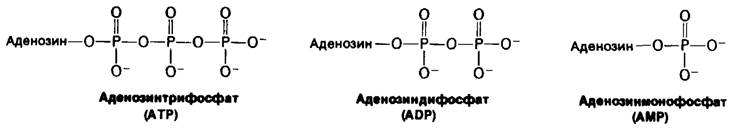
Рис. 11.3. Строение ATP, ADP и AMP. (Аденозин состоит из аденина, связанного с рибозой.)
Свободная энергия, высвобождающаяся при гидролитическом расщеплении ангидридной связи АТР, используется для запуска реакций, требующих притока свободной энергии, например, при мышечном сокращении. АТР в свою очередь образуется из ADP и Рi при окислении топливных молекул у хемотрофов или при утилизации света у фототрофов. Этот цикл АТР ADP представляет собой основной механизм обмена энергии в биологических системах.
Некоторые биосинтетические реакции запускаются нуклеотидами-аналогами АТР, а именно: гуанозинтрифосфатом (GTP), уридинтрифосфатом (UTP) и цитидинтри- фосфатом (СТР). Дифосфатные формы этих нуклеотидов обозначаются соответственно, как GDP, UDP и СОР. Ферменты катализируют перенос концевой фосфорильной группы от одного нуклеотида к другому:
АТР + GDP ⇄ ADP + GTP,
АТР + GMP ⇄ ADP + GDP.
11.5. АТР постоянно образуется и потребляется
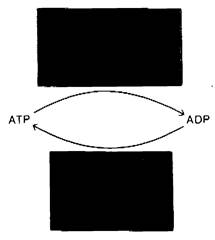
АТР является главным непосредственно используемым донором свободной энергии в биологических системах, а не формой запасания свободной энергии. В обычной клетке молекула АТР расходуется в течение одной минуты после ее образования. Оборот АТР очень высок. Например, человек в покое расходует около 40 кг АТР за 24 ч. Во время интенсивных упражнений скорость использования АТР может достигать 0,5 кг/мин. Движение, активный транспорт, усиление сигнала и процессы биосинтеза могут происходить только при условии непрерывного регенерирования АТР из ADP (рис. 11.4). Фотографы для генерирования АТР извлекают свободную энергию из солнечного света, тогда как хемотрофы образуют АТР при окислении молекул, выполняющих роль топлива.
Рис. 11.4. Цикл АТР-ADP-основной механизм обмена энергии в биологических системах
11.6. Структурная основа АТР, определяющая высокий потенциал переноса групп
Сравним стандартную свободную энергию гидролиза АТР со свободной энергией гидролиза такого фосфорного эфира, как глицерол-3-фосфат:
АТР + Н2О ⇄ ADP + Рi + Н+
∆G0' = — 7,3 ккал/моль,
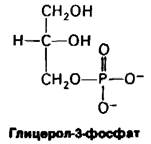
Глицерол-3-фосфат + Н2O ⇄ Глицерол + Рi
∆G0' = - 2,2 ккал/моль.
Значение ∆G0 для гидролиза глицерол-3- фосфата значительно меньше, чем для гидролиза АТР. Это означает, что АТР имеет более сильно выраженную тенденцию к переносу концевой фосфорильной группы на молекулу воды, чем глицерол-3- фосфат. Иными словами, АТР обладает более высоким потенциалом переноса фосфатных групп, чем глицсрол-3-фосфат.
Какова структурная основа присущего АТР высокого потенциала переноса фосфатной группы? Чтобы ответить на этот вопрос, следует проанализировать структуру АТР и продуктов его гидролиза ADP и Рi, потому что ∆G0 зависит от разности свободной энергии продуктов реакции и вступающих в нее соединений. Доказана важная роль двух факторов в этом аспекте: электростатического отталкивания и резонансной стабилизации. При pH 7 трифосфатный компонент АТР несет около четырех отрицательных зарядов. Эти заряды сильно взаимоотталкиваются, поскольку они находятся в тесной близости друг к другу. Электростатическое отталкивание между указанными отрицательно заряженными группами ослабляется при гидролизе АТР. Другой фактор, обусловливающий высокий потенциал переноса групп, которым обладает АТР-это большая резонансная стабилизация для ADP и Рi, чем для АТР. Например, ортофосфат имеет определенное число резонансных форм с одинаковой энергией (рис. 11.5). В противоположность ему концевой отрезок АТР имеет меньшее количество значимых резонансных форм в расчете на одну фосфатную группу. Резонансные формы такого типа, который показан на рис. 11.6, вряд ли существуют, поскольку в этом случае два атома фосфора будут конкурировать за электронные пары на кислороде. Кроме того, электростатически неблагоприятным является расположение положительного заряда на кислороде в близком соседстве с положительно заряженным атомом фосфора.
Рис. 11.5. Значимые резонансные формы ортофосфата
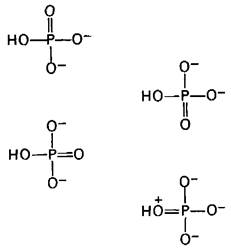
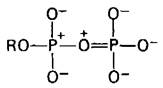
Рис. 11.6. Маловероятная резонансная форма концевой части АТР
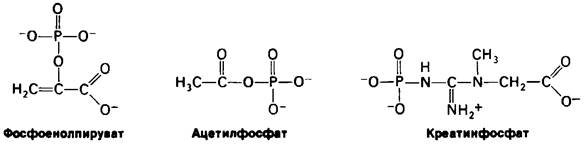
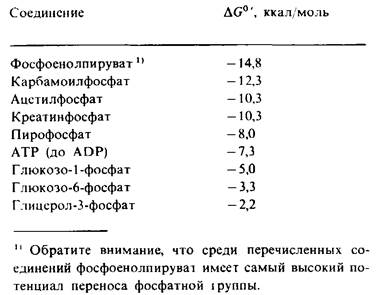
Различные другие соединения в биологических системах имеют высокий потенциал переноса фосфатной группы. Некоторые из них, такие, как фосфоенолпируват, aцетилфосфат и креатинфосфат (рис. 11.7), обладают более высоким потенциалом переноса фосфатной группы, чем АТР. Это означает, что фосфоенолпируват может переносить свою фосфорильную группу на ADP с образованием АТР. Действительно, таков один из путей синтеза АТР при расщеплении сахаров. Важное значение имеет тот факт, что по потенциалу переноса фосфатной группы АТР занимает промежуточное положение в ряду биологически важных фосфорилированных молекул (табл. 11.2). В силу этого промежуточного положения АТР эффективно функционирует в качестве переносчика фосфорильных групп.
Таблица 11.2. Свободная энергия гидролизанекоторых фосфорилированных соединений
АТР часто называют высокоэнергетическим фосфатным соединением и его фосфоангидридные связи относят к высокоэнергетическим связям. Следует отметить, что эти связи сами по себе не обладают какими-либо особыми свойствами. Они являются высокоэнергетическими связями в том смысле, что при их гидролизе высвобождается (по причинам, указанным выше) большое количество свободной энергии. Введенный Липманом (Lipmann) термин «высокоэнергетическая связь» и предложенный им символ ~ Р для обозначения соединений с высоким потенциалом переноса фосфатной группы являются выразительными, лаконичными и удобными обозначениями. Концепции Липмана сыграли большую роль в стимулировании интереса к биоэнергетике.
Рис. 11.7. Соединения, имеющие более высокий потенциал переноса фосфатной группы, чем АТР