БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ II ГЕНЕРИРОВАНИЕ И ХРАНЕНИЕ МЕТАБОЛИЧЕСКОЙ ЭНЕРГИИ
ГЛАВА 19. ФОТОСИНТЕЗ
19.5. Кислород, выделяющийся при фотосинтезе, происходит из воды
Обратимся теперь к химическим изменениям при фотосинтезе. Важное значение для выяснения механизма фотосинтеза имеет источник кислорода, выделяемого зелеными растениями. Сравнительные исследования фотосинтеза у многих организмов привели к открытию этого источника уже в 1931 г. Некоторые фотосинтезирующие бактерии в присутствии света превращают сероводород в серу. Корнелис ван Нил (Comelis Van Niel) обнаружил, что реакции фотосинтеза у зеленых растений и зеленых серных бактерий очень сходны:
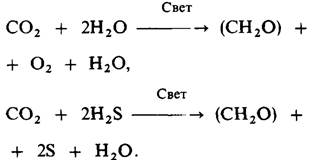
Сера, образуемая фотосинтезирующими бактериями, аналогична кислороду, который выделяется растениями. Ван Нил предложил общую формулу для фотосинтеза:
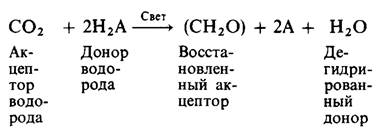
Донором водорода Н2А у зеленых растений является Н2O, у фотосинтезирующих серных бактерий-Н25. Таким образом, фотосинтез у зеленых растений может быть сформулирован как реакция восстановления СO2 водородом, происходящим из воды. Выделение кислорода будет тогда необходимым следствием этого процесса дегидрирования. Суть такого взгляда на фотосинтез может быть выражена следующим образом: вода расщепляется светом.
В 1941 г. стал доступен тяжелый изотоп кислорода, 18O, в связи с чем появилась возможность прямо проверить это положение. Действительно, при проведении фотосинтеза в воде, обогащенной 18O, этот изотоп обнаруживался в выделяемом кислороде. Полученный результат подтвердил предположение о том, что O2, образующийся при фотосинтезе, происходит из воды.
![]()
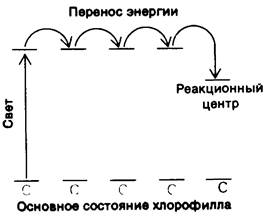
Рис. 19.8. Схематическое изображение энергетических уровней для возбужденного состояния хлорофиллов антенн и реакционного центра
19.6. Реакция Хилла: освещенные протопласты выделяют кислород и восстанавливают искусственный акцептор электронов
В 1939 г. Роберт Хилл (Robert Hill) обнаружил, что изолированные хлоропласты при их облучении в присутствии соответствующего акцептора электронов, например, феррицианида, выделяют кислород. Одновременно происходит восстановление ферри- цианида в ферроцианид. Реакция Хилла, это поворотный пункт в раскрытии механизма фотосинтеза по следующим причинам:
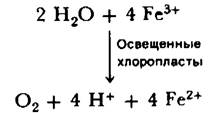
1. Она раскрыла сущность фотосинтеза, показав, что выделение кислорода может протекать без восстановления СO2. СO2 может быть заменен искусственными акцепторами электронов, такими, как феррицианид.
2. Она подтвердила, что выделившийся кислород происходит из воды, а не из СO2, поскольку СO2 в системе не было.
3. Она показала, что изолированные хлоропласты могут осуществлять значительную часть составляющих реакций фотосинтеза.
4. Она открыла, что первичным событием в фотосинтезе является активированный светом перенос электрона от одного вещества к другому против градиента химического потенциала. Восстановление ферри- иона в ферро-ион под действием света представляет собою превращение света в химическую энергию.
19.7. Фотосинтез требует взаимодействия двух видов фотосистем
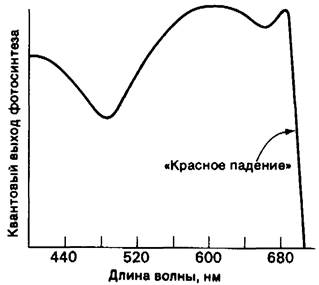
В результате многочисленных экспериментальных исследований было установлено, что в хлоропластах имеются две различные фотосистемы. Скорость фотосинтеза исследовалась как функция длины световой волны. Скорость фотосинтеза, разделенная на количество квантов при каждой длине волны, дает относительную квантовую эффективность процесса. Для единичного фоторецептора квантовая эффективность должна быть независимой от длины волны за пределами его полосы поглощения. Эта закономерность не имеет места при фотосинтезе: квантовая эффективность фотосинтеза резко падает при длинах волн, превышающих 680 нм, хотя хлорофилл все еще поглощает свет в диапазоне длин волн от 680 до 700 нм (рис. 19.9). Однако скорость фотосинтеза, протекающего с использованием длинноволнового света, может быть повышена при добавлении света с меньшей длиной волны, например, 600 нм. Скорость фотосинтеза в присутствии света с двумя длинами волн-600 и 700 нм-превышает сумму скоростей этого процесса при воздействии каждой из указанных световых волн в отдельности. Исходя из этих наблюдений, называемых «красным падением», и феномена усиления, Эмерсон (Еmerson) высказал предположение, что фотосинтез требует взаимодействия двух световых реакций: обе они запускаются светом с длиной волны менее 680 нм, но лишь одна из них протекает при свете с большей длиной волны.
Рис. 19.9. Квантовый выход фотосинтеза резко падает, когда длина возбуждающей световой волны превышает 680 нм
19.8. Роль двух фотосистем
Фотосистема I, которая может быть возбуждена светом с длиной волны менее 700 нм, генерирует сильный восстановитель, приводящий к образованию NАDРН. В противоположность ей фотосистема II, требующая присутствия света с длиной волны менее 680 нм, образует сильный окислитель, приводящий к образованию O2. Кроме того, фотосистема I продуцирует слабый окислитель, а фотосистема II-слабый восстановитель. Результатом взаимодействия этих систем является образование АТР. Этот компонент процесса фотосинтеза, открытый Дэниелем Арноном (Daniel Amon), называется фотосинтетическим фосфорилированием, или фотофосфорилированием.
Рис. 19.10. Взаимодействие фотосистем I и II при фотосинтезе
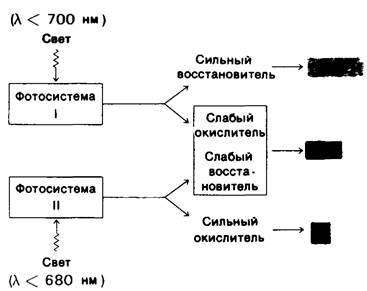
Таблица 19.1. Состав фотосистем I и II

Фотосистемы I и II различаются по своей структуре. При обработке мембран тилакоидов детергентами освобождаются преимущественно частицы, содержащие фотосистему I. Методом центрифугирования в градиенте плотности можно разделить частицы, обладающие только активностью фотосистемы I, и частицы, обогащенные активностью фотосистемы II. Большинство молекул хлорофилла связано со специфическими белками. Из частиц, содержащих фотосистему I, выделен комплекс, состоящий из 14 молекул хлорофилла а, связанных с белком 110 к Да. Второй вид комплекса, образованный частицами фотосистемы II, содержит 3 молекулы хлорофилла а и 3 молекулы хлорофилла Ь, связанные с белком 28 кДа. Наиболее хорошо охарактеризованный хлорофилл-белковый комплекс, выделенный из зеленых бактерий, состоит из трех субъединиц 50 кДа, каждая из которых содержит семь молекул бактериохлорофилла (рис. 19.11). Одна из функций белка в этих комплексах заключается в поддержании оптимальной геометрии для переноса энергии между хлорофиллами.
Рис. 19.11. Структура бактериохлоро- филлбелкового комплекса из фотосинтезирующей зеленой бактерии