БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
ЧАСТЬ V. МОЛЕКУЛЯРНАЯ ФИЗИОЛОГИЯ
ГЛАВА 36. МЕМБРАННЫЙ ТРАНСПОРТ
36.9. Транспорт кальция осуществляется другой АТРазой
Ионы кальция играют важную роль в регуляции мышечного сокращения (разд. 34.10), а также во многих других физиологических процессах. В скелетной мышце содержится сложная сеть связанных с мембраной трубочек и везикул. Эта мембранная система, называемая саркоплазматическим ретикулумом, регулирует концентрацию Са2+ в среде, окружающей сократительные мышечные волокна. В состоянии покоя Са2+ насасывается в саркоплазматический ретикулум, так что непосредственно вокруг миофибрил концентрация Са2+ бывает очень низкой. Возбуждение мембраны саркоплазматического ретикулума под влиянием нервного импульса ведет к мгновенному высвобождению больших количеств Са2+, и это запускает мышечное сокращение. Другими словами, Са2+ служит промежуточным звеном между нервным импульсом и сокращением мышечного волокна.
Рис. 36.10. Наперстянка

Транспорт Са2+ через мембрану саркоплазматического ретикулума происходит за счет энергии АТР. В саркоплазматическом ретикулуме имеется АТРаза, которую активирует Са2+. Эта Са2+-АТРаза является составной частью Са2+-насоса подобно тому, как (Na+ + К+)-АТРаза - часть (Na+ + К+)-насоса. Са2+-АТРаза также подвергается фосфорилированию в ходе гидролиза АТР:
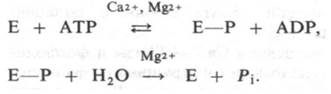
Рис. 36.11. Мембранные везикулы, образованные из очищенной Са2+-АТРазы. Глобулярные частицы на поверхности мембраны - участки молекулы АТРазы, пронизывающей мембрану
Цикл конформационных изменений, обусловленных фосфорилированием и дефосфорилированием, обеспечивает перенос двух ионов Са2+ при расщеплении одной молекулы АТР. Благодаря очень высокому сродству этой АТРазы к Са2+ (К ~107 М) фермент эффективно транспортирует Са2+ из цитозоля (где [Са2+] <10-5 М) в саркоплазматический ретикулум (где [Са2+] ~ 10-2 М).
Плотность молекул Са2+-насоса в мембране саркоплазматического ретикулума очень велика, а именно около 20 000 в расчете на 1 мкм2. В сущности, Са2+-АТРаза составляет более 80% общего количества интегральных белков мембраны и занимает треть ее поверхности. Большая субъединица (100 кДа) Са-насоса пронизывет мембрану и содержит участок фосфорилирования; как и в (Na+ + К+)-насосе, таким участком является специфическая боковая цепь, представленная остатком аспартата. Еще одна общая черта обоих насосов - это наличие гликопротеина: в Са2+-насосе гликопротеин массой 55 кДа связан с большой субъединицей.
Из очищенной Са2+-АТРазы и фосфолипидов удалось реконструировать функционально активный Са2+-насос. В этом эксперименте Са2+-АТРазу выделяли из мембран саркоплазматического ретикулума после их солюбилизации детергентом холатом. Очищенный солюбилизированный фермент добавляли к фосфолипидам из соевых бобов. После удаления детергента путем диализа образовывались мембранные везикулы. Эти реконструированные везикулы с высокой скоростью накапливали Са2+ в присутствии АТР и Mg2+.
36.10. Поток Na+ обеспечивает энергией активный транспорт сахаров и аминокислот в животных клетках
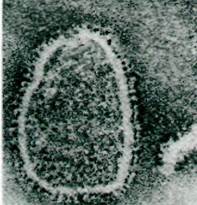
Многие транспортные процессы не зависят непосредственно от гидролиза АТР, а сопряжены с потоком ионов по электрохимическому градиенту. Так, во многих животных клетках насасывание глюкозы обеспечивается одновременным входом Na+. При этом ионы натрия и глюкоза связываются со специфическим транспортным белком и проникают в клетку одновременно. Согласованный перенос двух компонентов называют котранспортом; при симпорте имеет место перенос обоих компонентов в одном направлении, а при антипорте - в противоположных направлениях. Ионы натрия, которые входят в клетку вместе с молекулами глюкозы посредством симпорта, выводятся из клетки (Na+ + К+)-АТРазой (рис. 36.12). Количество транспортируемой глюкозы и скорость ее транспорта зависят от трансмембранного градиента концентрации Na+.
Рис. 36.12. Источником энергии для активного транспорта глюкозы служит градиент концентрации Na+. Эта система симпорта свойственна плазматическим мембранам клеток кишечника и почек
Зависящий от Na+ симпорт широко используется в животных клетках для накопления аминокислот. В некоторых клетках, например, в микроворсинках щеточной каемки кишечника (рис. 36.13), посредством симпорта осуществляется активный транспорт сахаров. Кроме того, в тонком кишечнике существует специализированный Na+-зависимый симпорт, обеспечивающий перенос ионов Cl- против градиента концентрации. Во многих клетках ионы натрия служат также движущей силой в процессах антипорта, направленных на выведение ионов кальция. Таким образом, градиент концентрации ионов натрия, создаваемый (Na+ + К+)-АТРазой, обеспечивает энергией большинство симпортов и антипортов в животных клетках.
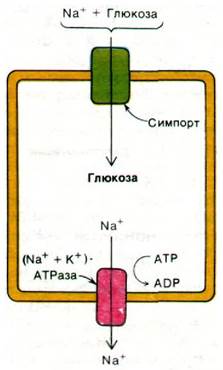
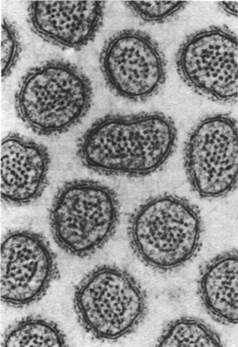
Рис. 36.13. Электронная микрофотография поперечного среза микроворсинок кишечника. Наличие микроворсинок во много раз увеличивает площадь поверхности, через которую происходит транспорт питательных веществ
36.11. Поток протонов служит движущей силой во многих процессах транспорта у бактерий
Симпорты и антипорты - эволюционно очень древние механизмы молекулярного транспорта. Так, движущей силой многих транспортных систем у бактерий служит поток протонов через плазматическую мембрану. Наиболее изученная бактериальная система симпорта - перенос лактозы у E. coli (рис. 36.14). У этой обитательницы нижних отделов кишечника млекопитающих выработался высокоэффективный механизм концентрирования лактозы. Насос для этого дисахарида, выделенный Юджином Кеннеди (Eugene Kennedy), представляет собой одиночную полипептидную цепь массой 30 кДа и называется пермеазой для лактозы (или М-белком). Это интегральный мембранный белок, который кодируется геном у, входящим в lac-оперон (разд. 28.3). В индуцированных клетках на его долю приходится около 4% белков мембраны.
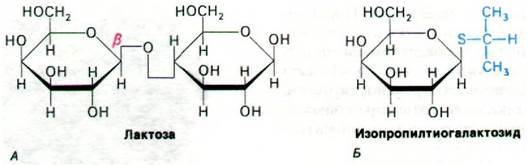
Рис. 36.14. Пермеаза для лактозы транспортирует β-галактозиды. в частности лактозу (А) и изопропилтиогалактозид (Б). Тиогалактозиды оказались очень удобными для изучения этой системы, так как они транспортируются пермеазой для лактозы, но не подвергаются гидролизу β-галактозидазой
Раскрытию механиза функционирования лактозного насоса способствовало изучение мутантов по гену у, а также исследования везикул (пузырьков), полученных из бактериальных мембран. Везикулы очень удобны для изучения процессов транспорта, поскольку они значительно проще устроены, чем целая бактерия. В везикулах есть система окислительного фосфорилирования и другие связанные с мембраной белки, но отсутствуют цитоплазматические компоненты интактной клетки. Сами по себе везикулы не накапливают лактозы, но если добавить субстрат окисления, обеспечивающий поток обладающих высоким потенциалом электронов по дыхательной цепи, то накопление лактозы имеет место. Этот же эффект можно получить и иным способом, а именно созданием градиента рН с помощью образуемой вне клеток кислоты. Создание мембранного потенциала градиентом концентрации К+также приводит к насасыванию лактозы. Все эти данные показывают, что активный транспорт лактозы обеспечивается протонодвижущей силой в плазматической мембране. Транспорт молекул лактозы сопряжен с движением протона в клетку. При физиологических условиях протонный градиент, необходимый для этого активного транспорта, возникает за счет потока электронов от донора, обладающего высоким потенциалом (например, NADH), по дыхательной цепи. Симпорт протонов и лактозы иллюстрирует обобщающую концепцию Питера Митчелла (Peter Mitchell) о «преобразовании энергии посредством протонного градиента» (разд. 14.18).