БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
ЧАСТЬ V. МОЛЕКУЛЯРНАЯ ФИЗИОЛОГИЯ
ГЛАВА 32. ОБОЛОЧКИ БАКТЕРИАЛЬНЫХ КЛЕТОК
32.2. Стадии синтеза пептидогликана
Синтез пептидогликана происходит в пять стадий.
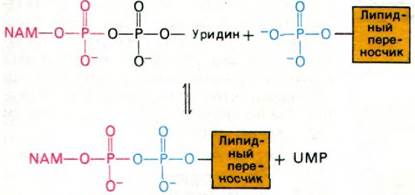
1. На остатке NAM, присоединенном к уридиндифосфату, выстраивается пептидное звено.
2. Образовавшееся NAM-пептидное звено переносится на липид-переносчик. Значение этой стадии для синтеза клеточной стенки состоит в следующем. Конечный полимеризованный продукт расположен вне клетки (с наружной стороны клеточного барьера проницаемости), тогда как его предшественник синтезируется внутри клетки. UDP, будучи соединением полярным, не проникает сквозь клеточную мембрану. Липидный же переносчик как совершенно неполярное соединение способен совершать челночные движения через мембрану.
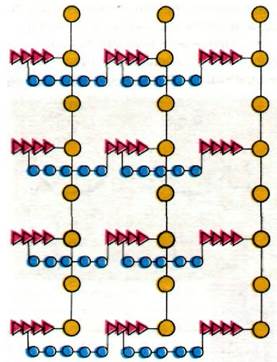
Рис. 32.4. Схематическое изображение пептидогликана. Сахара показаны желтым цветом, тетрапептиды - красным, пентаглициновые мостики синим. Благодаря обилию перекрестных сшивок клеточная стенка представляет собой одну огромную мешковидную макромолекулу
3. К NAM-пептидной единице, связанной с липидным переносчиком, присоединяются NAG и пентаглициновый мостик.
4. Образовавшееся дисахарид-пептидное звено переносится от липидного переносчика на растущую полисахаридную цень.
5. Отдельные полисахаридные цепи поперечно связываются пентаглициновыми мостиками в ходе реакции транспептидации.
32.3. Синтез UDP-углевод-пептидного звена
Биосинтез пептидогликанов начинается с образования активированных сахаров. Уридиндифосфат-N-ацетилглюкозамин (UDP- NAG) синтезируется из N-ацетилглюкозамин-1-фосфата и UTP в реакции, протекающей за счет гидролиза пирофосфатной связи (рис. 32.5). Уридиндифосфат-N-ацетилмурамовая кислота (UDP-NAM) образуется из UDP-NAG и фосфоенолпирувата (рис. 32.6).
Рис. 32.5. Синтез UDP-NAG
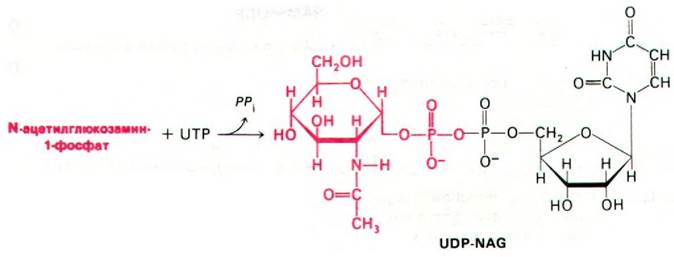
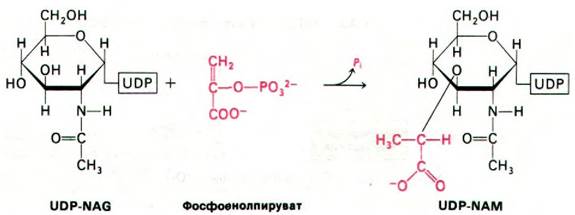
Рис. 32.6. Синтез UDP-NAM
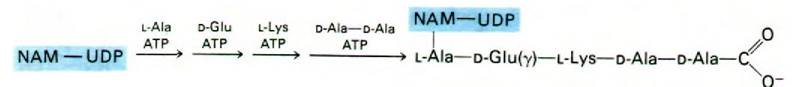
Рост пептидной цепи начинается с образования пептидной связи между аминогруппой L-аланина и карбоксильной группой остатка N-ацетилмурамовой кислоты в UDP-NAM. Далее последовательно присоединяются D-глутамат, L-ЛИЗИН и дипептид D-аланил-D-аланин (рис. 32.7). D-аминокислоты образуются из соответствующих L-изомеров под действием рацемаз, содержащих в качестве простетической группы пиридоксальфосфат. Образование каждой из этих пептидных связей протекает за счет энергии АТР. Подчеркнем, что синтез в данном случае осуществляется не по обычному механизму синтеза белков на рибосомах, а специальными ферментами. Следовательно, информация относительно последовательности аминокислот определяется только специфичностью ферментов, а не нуклеотидной последовательностью информационной РНК. Пептид такого рода не мог бы быть синтезирован обычным путем на рибосомах, поскольку он включает D-аминокислоты и γ-пептидную связь.
Рис. 32.7. Синтез пентапептида на UDP-NAM
32.4. Перенос углеводпептидного звена на липидный переносчик
На следующем этапе происходит перенос активированного углеводпептидного звена от UDP на липидный переносчик (рис. 32.8). Последний представляет собой длиннонепочечный спирт, содержащий 11 изопреновых единиц и потому высокогидрофобный в отличие от UDP. По-видимому, именно благодаря гидробофному характеру этого С55-липида новообразованное углеводпептидное звено преодолевает барьер проницаемости, которым служит клеточная мембрана.
Рис. 32.8. Структура липидного переносчика, участвующего в биосинтезе клеточных стенок
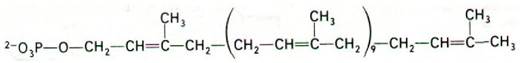
Вспомним, что другой высокогидрофобный переносчик - долихолфосфат - участвует в синтезе олигосахаридов, составляющих сердцевину (олигосахаридного «ядра») гликопротеинов у эукариот (разд. 29.31).