БІОХІМІЯ - Підручник - Остапченко Л. І. - 2012
Розділ 10. МЕТАБОЛІЗМ НУКЛЕЇНОВИХ КИСЛОТ
10.5. Біосинтез нуклеотидів
10.5.1.Біосинтез пуринових нуклеотидів
Біосинтез пуринових нуклеотидів de novo. Дослідження сполук, які містять мічені ізотопи 14C та 15N, дозволили виявити попередників нуклеотидів. Було з'ясовано, що у формуванні пуринового ядра беруть участь амінокислоти аспартат, гліцин, глутамін, СО2 та дві одновуглецеві похідні тетрагідрофолієвої кислоти: мете- ніл-Н4-фолат і форміл-Н4-фолат (рис. 10.7).
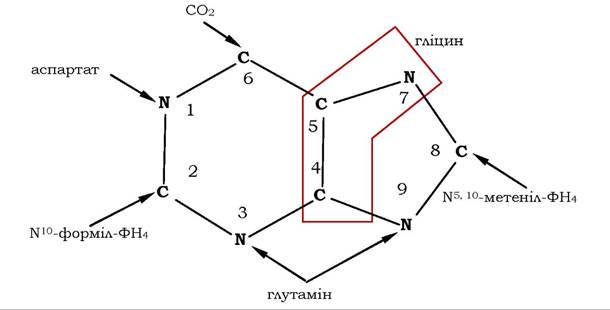
Рис. 10.7. Джерела атомів пуринів
Шлях біосинтезу пуринових нуклеотидів загалом аналогічний у ссавців, птахів, дріжджів і бактерій. Процес складається із серії послідовних реакцій, які проходять за участю специфічних ферментів. У синтезі пуринових нуклеотидів не утворюється вільна азотиста основа, а пуринове кільце формується на залишку рибозо-5-фосфату. Перша реакція починається з перенесення амідної групи глутаміну на ФРПФ з утворенням 5-фосфорибозил- 1-аміну. Цю реакцію каталізує регуляторний фермент синтазу пуринових нуклеотидів глутамін-ФРПФ-амідотрансфераза. Потім до аміногрупи 5-фосфорибозил-1-аміну приєднується залишок гліцину, N5,10-метеніл-Н4-фолату, а також одна амідна група глутаміну, діоксид вуглецю, аміногрупа аспарагінової кислоти та формільний залишок N10-форміл- Н4-фолату (рис. 10.8).
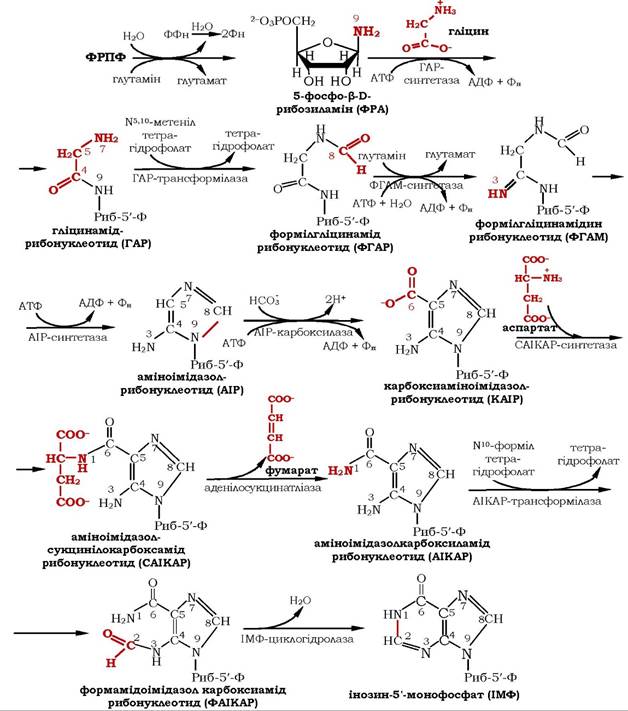
Рис. 10.8. Синтез інозин-5'-монофосфату
Характерною особливістю синтезу інозин-Б'-фосфату (ІМФ) є участь тетрагідрофолату (ФН4) у двох окремих реакціях одно- вуглецевого перенесення. В одній використовується N10-метеніл-ФН4, в іншій - N10-форміл- ФН4. Останній утворюється з N5,10-метеніл-ФН4, який у свою чергу є продуктом НАДФ-залежного дегідрогенування N5,10-метилен- ФН4. Якщо N5,10-метилен-ФН4 є джерелом однокарбонових фрагментів для багатьох акцепторів, то N5,10-метеніл-ФН4 постачає однокарбонову групу (або безпосередньо, або через стадію утворення N10-форміл- ФН4) тільки в пуринові основи.
Завершується вся десятистадійна серія утворенням першого пуринового нуклеотиду - ІМФ, на синтез якого витрачається не менше шести молекул АТФ. ІМФ є загальним попередником для синтезу аденілової та гуанілової кислот. Крім того, його в невеликій кількості виявляють у тРНК як один із мінорних нуклеотидів.
Перетворення ІМФ у АМФ і ГМФ. З інозинової кислоти шляхом модифікації гіпоксантинового кільця синтезуються АМФ та ГМФ і в кожному випадку це відбувається у дві стадії (рис. 10.9).
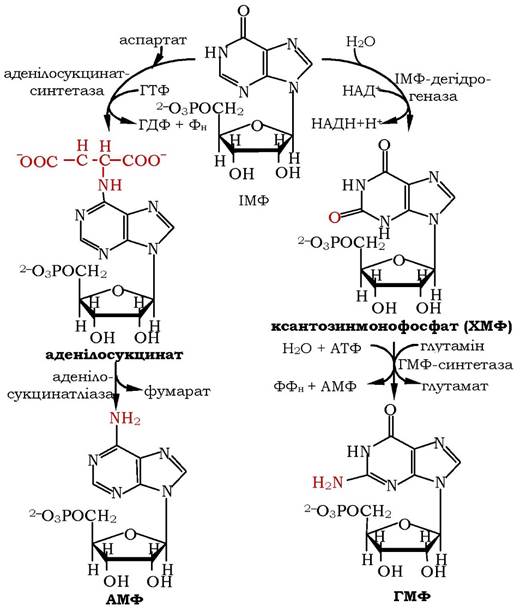
Рис. 10.9. Синтез АМФ і ГМФ із ІМФ
Синтез АМФ каталізується аденілосукцинатсинтетазою за рахунок енергії ГТФ шляхом заміщення кисню при С-6 атомі пурину на аміногрупу, донором якої є аспарагінова кислота з утворенням аденілосукцинату. На другому етапі за дії аденілосукцинатліази відбувається розщеплення аденілосукцинату з вивільненням фумарату й утворенням АМФ.
Синтез другого пуринового нуклеотиду - ГМФ - відбувається також у два етапи. Спочатку ІМФ окиснюється НАД-залежною ІМФ-дегідрогеназою з утворенням ксантилової кислоти, а потім відбувається заміщення кисню при С-2 атомі на аміногрупу, донором якої є амідна група глутаміну. Трансамідування каталізує ГМФ-синтетаза з використанням енергії АТФ.
Важливо зазначити, що при утворенні пуринових нуклеотидів АТФ витрачається на синтез гМф, а ГТФ - на синтез АМФ. Подібне перехресне використання пуринових нуклеозидфосфатів на утворення кінцевих продуктів синтезу допомагає підтримувати в клітинах еквівалентне співвідношення пуринових нуклеотидів.
Щоб синтезовані пуринові нуклеозидмонофосфати брали участь у синтезі нуклеїнових кислот, деяких коферментів і багатьох інших синтетичних і енергетичних реакціях, вони мають набути активної форми. Активовані нуклеотиди являють собою нуклеозид-5'-ди- та трифосфати.
Утворення фосфорильованих форм пуринових нуклеотидів (АДФ, ГДФ, АТФ, ГТФ) відбувається з відповідних монофосфатів (АМФ і ГМФ) шляхом їхньої взаємодії з АТФ за участю специфічних до азотистої основи нуклеозидмонофосфаткіназ. Так, аденілаткіназа каталізує реакцію
![]()
Утворений таким чином АДФ далі фосфорилюється та перетворюється в АТФ або шляхом субстратного фосфорилювання при гліколізі, або за рахунок окисного фосфорилювання в дихальному ланцюзі.
Аналогічно відбувається фосфорилювання ГМФ, однак, на відміну від АМФ, де утворюється дві молекули АДФ, формується ГДФ і АДФ:
![]()
На наступному етапі ГДФ фосфорилюється за участю АТФ і ферменту нуклеозиддифосфаткінази:
![]()
Синтез пуринових нуклеотидів шляхом реутилізації. Синтез пуринових нуклеотидів основним шляхом (de novo) не здатний компенсувати всю необхідну кількість цих сполук. Велика потреба у пуринових нуклеотидах привела до розвитку "запасних" шляхів синтезу.
Джерелом пуринових основ для такого синтезу є пуринові основи та нуклеозиди. Їхня реутилізація відбувається двома шляхами:
1. ФРПФ-залежне фосфорибозилювання пуринових основ. Цей механізм здійснюють два ферменти. Так, аденін взаємодіє з ФРПФ за допомогою ферменту аденозинфосфорибозилтрансферази й перетворюється в АМФ:
![]()
Реутилізація гуаніну відбувається аналогічно, але за участю іншого ферменту - гіпоксантингуанінфосфорибозилтрансферази:
![]()
Цей самий фермент бере участь у реутилізації гіпоксантину (утворюється за рахунок дезамінування аденіну), який при цьому перетворюється в інозинову кислоту:
![]()
Цей спосіб реутилізації пуринів є найдієвішим, оскільки утворений за рахунок гіпоксантингуанінфосфорибозилтрансферази ІМФ, залучається в синтез АМФ і ГМФ.
2. Фосфорилювання пуринових рибонуклеозидів. Нуклеозиди, які утворюються під час катаболізму нуклеїнових кислот із нуклеотидів за дії нуклеотидаз, можуть удруге фосфорилюватися, утворюючи нуклеозид-5'-монофосфати за рахунок перенесення γ-фосфатного залишку АТФ на відповідний субстрат. Реакцію фосфорилювання каталізує фермент аденозинкіназа:
![]()
Аденозинкіназа, крім того, фосфорилює 2'-дезоксіаденозин, вона виявляє також деяку активність щодо гуанозину, інозину та їхніх 2'-дезоксипохідних.
Регуляція синтезу пуринових нуклеотидів. На синтез молекули ІМФ витрачається енергія гідролізу шести молекул АТФ, при цьому як попередники беруть участь гліцин, глутамін, попередники тетрагідрофолієвої кислоти й аспартат. Для економії енергетичних і харчових ресурсів важлива ефективна регуляція процесу біосинтезу пуринових нуклеотидів de novo.
Основною сполукою, від якої залежить синтез пуринових нуклеотидів, є ФРПФ. Внутрішньоклітинна концентрація ФРПФ залежить від швидкості його синтезу, утилізації та деградації. Кількість ФРПФ визначається двома факторами: наявністю субстратів синтезу, у першу чергу рибозо-5-фосфату, та активністю ФРПФ-синтетази, чутливої до концентрації неорганічного фосфату й пуринових нуклеотидів. Фермент активується фосфатом та інгібується пуриновими нуклеозидмоно-, ди- і трифосфатами, які за ефективністю інгібування розподіляються наступним чином: НМФ > > НДФ > НТФ (рис. 10.10). Активність глутамін-ФРПФ-амідо- трансферази за механізмом від'ємного зворотного зв’язку гальмується кінцевими продуктами ланцюга реакцій - ІМФ, АМФ і ГМФ.
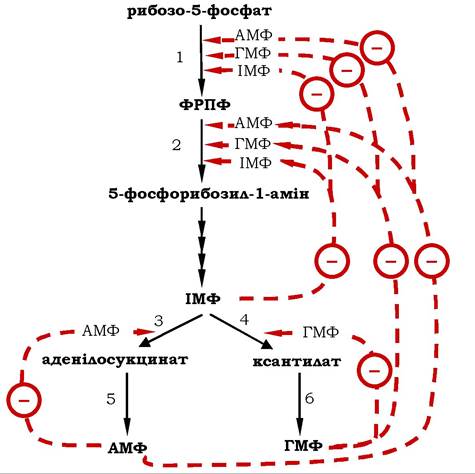
Рис. 10.10. Схема регуляції синтезу пуринових нуклеотидів:
1 - ФРПФ-синтетаза; 2 - глутамін-ФРПФ-амідотрансфераза; 3 - аденілосукцинатсинтетаза; 4 - ІМФ-дегідрогеназа;
5 - аденілосукцинатліаза; 6 - ГМФ-синтетаза. О інгібування кінцевими продуктами за принципом зворотного зв'язку
Синтез АМФ і ГМФ de novo регулюється також у місцях їхніх розгалужень: АМФ інгібує активність аденілосукцинатсинтетази, а ГМФ - реакцію утворення ксантилату, яку каталізує ІМФ-дегідрогеназа. Таким чином, за цим механізмом надлишок АМФ чи ГМФ пригнічує власний синтез з ІМФ, але не впливає на синтез іншого нуклеотиду. Але, як уже зазначалося вище, існує і перехресна регуляція дивергентних шляхів метаболізму ІМФ: утворення аденілосукцинату з ІМФ на шляху до АМФ стимулюється ГТФ, а утворення ГМФ із ксантилату вимагає присутності АТФ. Подібна регуляція гальмує біосинтез одного з пуринових нуклеотидів у разі нестачі іншого.