БОТАНИКА ТОМ 1 - КЛЕТОЧНАЯ БИОЛОГИЯ. АНАТОМИЯ. МОРФОЛОГИЯ - 2007
1. МОЛЕКУЛЯРНЫЕ ОСНОВЫ— СТРОИТЕЛЬНЫЕ «КИРПИЧИКИ» КЛЕТОК
1.5. Липиды
Хотя липиды нельзя отнести к макромолекулам, мы обсуждаем их здесь из-за особого значения в построении клеточных мембран и, соответственно, в структуре клетки. Наряду со структурными липидами в клетке имеются также запасные липиды — главная форма накопления органического углерода (биосинтез липидов см. 6.11; метаболизм липидов см. 6.12) в запасающих жиры семенах (например, у подсолнечника и льна).
1.5.1. Запасные липиды
В качестве запасных липидов, которые служат промежуточным депо энергии и углерода для обмена веществ, встречаются прежде всего неполярные и потому не растворимые в воде триацилглицерины (=триглицериды: рис. 1.21). Если при комнатной температуре они твердые, то говорят о жирах, а если жидкие — о маслах. Триацилглицерин состоит из одной молекулы глицерина, три гидроксильные группы которой образовали эфирные связи с жирными кислотами. Жирные кислоты могут быть одинаковыми, но обычно есть определенные различия. В запасных липидах встречаются насыщенные жирные кислоты (пальмитиновая и стеариновая) и ненасыщенные жирные кислоты (олеиновая, линолевая и линоленовая). Насыщенные жирные кислоты — это алканкарбоновые кислоты, ненасыщенные — алкенкарбоновые, содержащие одну или несколько двойных углеродных связей С=С (рис. 1.21; о синтезе жирных кислот см. в разделе 6.11.1). Запасные липиды аккумулируются либо в форме масляных телец диаметром 0,5 — 2 мкм (олеосом; см. рис. 6.101) в цитоплазме накапливающих жиры клеток или в виде масляных капель (пластоглобулы) в пластидах. Олеосомы состоят из масляной капли, окруженной простой липидной мембраной, отделяющейся от гладкого эндоплазматического ретикулума (ЭПР), места синтеза триацилглицеридов в клетке (см. 6.12, рис. 6.101). В мембрану встраиваются особые белки, олеозины, функция которых состоит в мобилизации запасных липидов (см. 6.11.3; 6.12).
Рис. 1.21. Структуры запасных и мембранных липидов
Запасные липиды — это неполярные (гидрофобные) триглицериды Мембранные липиды являются амфифильными молекулами их «головки», показанные цветом полярны (гидрофильны) (Долю липидов в построении разных клеточных мембран см в табл 1.4)

Таблица 1.4. Доля, %, разных классов липидов в составе клеточных мембран
Хлоропласты |
Митохондрии |
Мембрана пероксисом |
|||
Класс* липида |
Оболочка |
Тилакоид |
Внутренняя мембрана |
Плазмалемма |
|
Моногалактозил-диглицериды MGDG |
35 |
51 |
0 |
0 |
0 |
Дигалактозил-диглицериды DGDG |
30 |
26 |
0 |
0 |
0 |
Сульфолипиды SL |
6 |
7 |
0 |
0 |
0 |
Фосфатидилхолин PC |
20 |
3 |
27 |
32 |
52 |
Фосфатидилэтаноламин РЕ |
1 |
0 |
29 |
46 |
48 |
Фосфатидилсерин PS |
0 |
0 |
25 |
0 |
0 |
Другие |
8 |
13 |
19 |
22 |
0 |
* Сокращения, как на рис. 1.21 (по J.Joyard, H.W. Heidt).
Запасные липиды гидрофобны. Молекулы вытесняются из полярной водной фазы, они также нарушают структуру воды вследствие неспособности образовать водородные связи (см. 1.1). Это обусловливает несмешиваемость с водой неполярных органических растворителей (например, бензола, бензина, петролейного эфира). Самое бедное энергией и самое стабильное состояние смеси гидрофильных и гидрофобных жидкостей достигается, когда в результате расслоения поверхность соприкосновения гидрофильной (полярной) и гидрофобной (неполярной) фаз стала минимальной. На этом основано, например, откладывание запасных липидов в клетках в виде сферических олеосом. Агрегацию гидрофобных веществ в гидрофильном окружении называют гидрофобным эффектом: гидрофобные молекулы в водной среде собираются в наименьшем пространстве так, как если бы их сильно притягивало друг к другу. В действительности межмолекулярное притяжение у неполярных соединений очень мало. Его, однако, вполне достаточно, чтобы и неполярные соединения могли агрегироваться не только в жидком, но даже в твердом состоянии. Высказанное впервые И.Вандер-Ваальсом, а в 1930 г. объясненное Ф. Лондоном положение о существовании межмолекулярных сил (принято называть их силами Лондона—Вандер-Ваальса), обусловленных слабыми электрическими диполями, которые образуются вследствие неравномерного распределения обобществленных электронов. Содержащие белки однослойные мембраны олеосом препятствуют тому, чтобы капельки триглицеридов в клетке слипались благодаря гидрофобному эффекту в одну каплю, так как для ферментативной мобилизации резервного жира преимуществом оказывается большая поверхность (см. 6.12). Слой из
белков-олеозинов мешает сливаться и масляным капелькам
Силу химических связей можно охарактеризовать как энергию, которую надо приложить для их разрушения (энергия связей) — при ковалентных связях нужно более 100 кДж моль1 (в случае очень прочной тройной связи в молекуле азота (N2), к примеру 946 кДж моль-1), для водородных связeй — от 12 до 2S кДж моль1 и в случае сил Лондона —Ван-дер-Ваальса — 4 — 8 кДж моль чуть больше энергии теплового движения молекул в пределах физиологических температур (2,5 кДж моль-1)
1.5.2. Структурные липиды — образование липидного бислоя мембран
В отличие от неполярных запасных липидов в построении биологических мембран принимают участие амфиполярные (синонимы амфифильные, амфипатические) молекулы структурных липидов (см рис 1.21) Они имеют как гидрофобные, так и гидрофильные группы Этой особенностью строения молекул обусловлена способность мембранных липидов образовывать в жидкой среде плоские структуры На поверхности воды молекулы ориентируются так, что их гидрофильные группы погружены в воду, и при этом образуются гидратные оболочки, тогда как неполярные радикалы не контактируют с водной средой При достаточно плотном расположении молекул липидов это получается даже при мономолекулярном липидном слое (monolayer, англ. layer — слой) Однако внутри водной фазы образуется бимолекулярный липидный слой в результате такого взаимного расположения двух мономолекулярных слоев, когда гидрофильные «головки» амфиполярного мембранного липида гидратированы и обращены в сторону водной фазы, а гидрофобные «хвосты» направлены навстречу друг другу внутрь двойного слоя, в котором нет воды (рис 1.22) и который стабилизируется благодаря неполярным взаимодействиям (силам Лондона —Ван-дер- Ваальса).
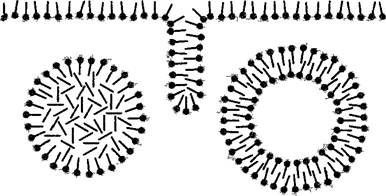
Рис. 1.22. Липидные моно- и бислои
Поверхность соприкосновения с водной средой образована гидрофильными головками, неполярные остатки жирных кислот направлены чаще всего перпендикулярно к этой поверхности Справа внизу, в водной фазе — липосома слева — масляная капелька (олеосома) поверхность которой образована монослоем из мембранных липидов, в то время как внутри преобладают неупорядоченные нейтральные липиды Липосомы можно получить экспериментально путем воздействия на подходящие смеси мембранных липидов ультразвуком Мембранные белки могут встраиваться в искусственные мембраны липосом, что используют для определения свойств транспортных белков в эксперименте
В связи с тем, что у структурных липидов (в отличие от запасных) из-за гидрофильных «головок» существует сильная адгезия (сцепление) с водой, поверхность соприкосновения не минимизирована, а максимальна, и образуются очень тонкие плоские липидные пленки Липидные молекулы двойных слоев направлены хотя и однотипно, однако располагаются все же не столь упорядоченно, как молекулы в кристаллической решетке. Чаще липидные слои жидкие, т.е. в них очень высока латеральная подвижность липидных молекул. Зато смещение молекулы мембранного липида на противоположную сторону двойного слоя происходит редко (Flip- Flop, период обмена половиной молекул между слоями составляет несколько часов). Состав липидов обеих сторон двойного липидного слоя поэтому, как правило, различен.
Мембранные липиды, как и запасные, представлены глицеролипидами. Здесь две соседние гидроксильные группы глицерина образуют эфирную связь с жирными кислотами, а третья гидроксильная группа несет полярную «головку». Если последняя является эфиром фосфорной кислоты, говорят о фосфолипидах, если гликозид образуется с сахаром, получается гликолипид. В растительных клетках гликолипиды можно обнаружить в мембранах пластид. В качестве сахара обычно присутствуют галактоза (галактолипиды) или сульфохиновоза (сульфолипнды) (см. рис. 1.21). Состав липидов разных клеточных мембран может быть весьма различным. Это четко видно из данных, приведенных в табл. 1.4.