Фізіологія людини - Вільям Ф. Ґанонґ 2002
Функції нервової системи
Центральне регулювання вісцеральних функцій
Гіпоталамус - Регулювання секреції задньої частки гіпофіза
Вазопресин і окситоцин
У більшості ссавців гормонами задньої частки гіпофіза є аргініновий вазопресин (AVP) і окситоцин. У молекулі вазопресину гіпопотамів і більшості видів свиней аргінін заміщений лізином (лізиновий вазопресин). Задня частка гіпофіза деяких видів свиней і сумчастих містить суміш аргінінового і лізинового вазопресину. Гормони задньої частки гіпофіза - це дев’ятиамінокислотні сполуки з дисульфідним кільцем на одному з кінців молекули (рис. 14-10).
Біосинтез, внутрішньонейронне транспортування і секреція
Гормони задньої частки гіпофіза синтезуються в тілах великоклітинних нейронів надзорового і пришлуночкового ядер, їх транспортують аксони цих нейронів до нервових закінчень, розміщених у задній частці гіпофіза, де вони виділяються у відповідь на електричні сигнали, що надходять до нервових закінчень. Деякі нейрони синтезують окситоцин, а інші - вазопресин. Окситоцин- і вазопресинвмісні нервові клітини є в обох ядрах.
Окситоцин і вазопресин — це типові нервові гормони, тобто гормони, що їх виділяють нервові клітини в кров’яне русло. Цей тип нервового регулювання для порівняння з
іншими показано на рис. 14-11. Термін нейросекреція початково стосувався процесу секреції гормонів нервовими клітинами, проте інколи його можна зрозуміти помилково, оскільки виявляється, що всі нейрони продукують певні хімічні речовини — нервові трансмітери (див. Розділ 1).
Гормони задньої частки гіпофіза, як і інші пептидні, синтезуються у вигляді великої молекули-попередника (прекурсора). В гранулах нейронів, де відбувається синтез, як окситоцин, так і вазопресин з’єднані з особливою сполукою - нейрофізином. У випадку окситоцину - це нейрофізин 1, а у випадку вазопресину - нейрофізин II. Спочатку вважали, що нейрофізини становлять зв’язувальні поліпептиди, які утворюють слабкі нетривкі зв’язки з молекулами вазопресину або окситоцину. Сьогодні з’ясовано, що вони є частинами молекули-попередника. Прекурсор аргінінового вазопресину - препропресофізин - містить лідерну послідовність, утворену 19 амінокислотними залишками, а також аргініновий вазопресин, нейрофізин II і, врешті, глікопептид (рис. 14-12). Молекула препрооксифізину - прекурсора окситоцину - менша за розміром, оскільки не містить глікопептиду.
Молекули-попередники синтезуються в рибосомах клітинних тіл нейронів. Їхні лідерні послідовності переходять в ендоплазматичну сітку. Сполуки накопичуються в секреторних гранулах у комплексі Ґольджі і переміщуються за допомогою аксоплазматичного транспортування до закінчень у задній частці гіпофіза. Секреторні гранули, які називають тільцями Геррінґа, легко піддаються дослідженню, оскільки добре зафарбовуються на гістологічних зрізах. Розщеплення молекули-попередника відбувається під час аксонного транспортування, внаслідок чого гранули нервових закінчень містять вже вільні окситоцин і вазопресин, відповідні нейрофізини, а також глікопептид - фрагмент прекурсора вазопресину. Функція цих сполук, що беруть участь у синтезі гормонів задньої частки гіпофіза, не з’ясована.
Електрична активність великоклітинних нейронів
Нейрони, у яких синтезуються окситоцин і вазопресин, також генерують і передають потенціали дії. Ці потенціали, досягаючи нервових закінчень нейронів, зумовлюють вивільнення гормону шляхом Са2+-залежного екзоцитозу. Принаймні в щурів після анестезії в цих нейронах не простежується електричних явищ у стані спокою або ж виникають низького рівня нерівномірні потенціали (0,1- 3,0 піки за 1 с). Однак реакція таких нейронів на подразнення буває різною (див. рис. 14-13). Подразнення сосків спричинює синхронні високочастотні потенціали в окситоцинових нейронах, які виникають після відповідного латентного періоду. Ці потенціали зумовлюють вивільнення окситоцину і, як наслідок,-виділення молока (див. нижче). З іншого боку, стимулювання вазопресинових нейронів, наприклад у разі крововтрати, зумовлює спочатку стійке посилення збуджень з наступним пролонгованим фазовим збудженням, під час якого періоди високочастотного збудження чергуються з періодами електричного спокою (фазові спалахи). Ці фазові спалахи переважно не синхронізуються в різних вазопресиносинтезувальних нейронах. Такий тип збудження забезпечує пролонговане посилюване виділення вазопресину, що відрізняється від синхронного порівняно короткочасного і високочастотного збудження окситоцинсинтезувальних нейронів.
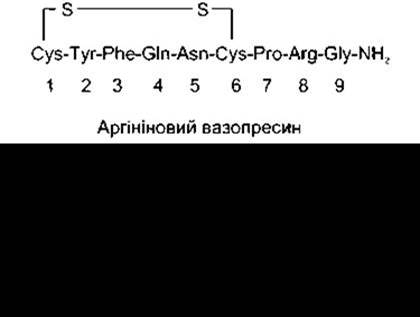
Рис. 14-10. Аргініновий вазопресин і окситоцин.
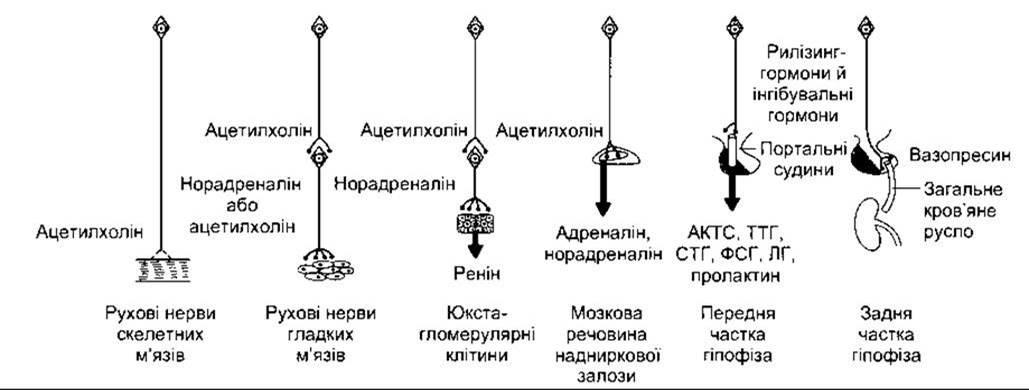
Рис. 14-11. Механізми нервового регулювання. Два крайні шляхи ліворуч: нейротрансмітери діють на нервові закінчення м’язів. Два шляхи посередині: нейротрансмітери регулюють секрецію ендокринних залоз. Два крайні шляхи праворуч: нейрони продукують гормони, що виділяються в судини гіпофізарної портальної системи або в загальне кров’яне русло.
Вазопресин і окситоцин інших ділянок
Вазопресиносинтезувальні нейрони містяться в надперехресних ядрах, а вазопресин і окситоцин - також у закінченнях нейронів, аксони яких проходять з пришлуночкових ядер до стовбура головного мозку і спинного мозку. Ці нейрони, очевидно, беруть участь у регулюванні серцево- судинної діяльності. Крім того, вазопресин і окситоцин в статевих залозах і кірковій речовині наднирникової залози, а окситоцин виявлений ще й у загрудинній залозі. Функція пептидів у цих органах невідома.
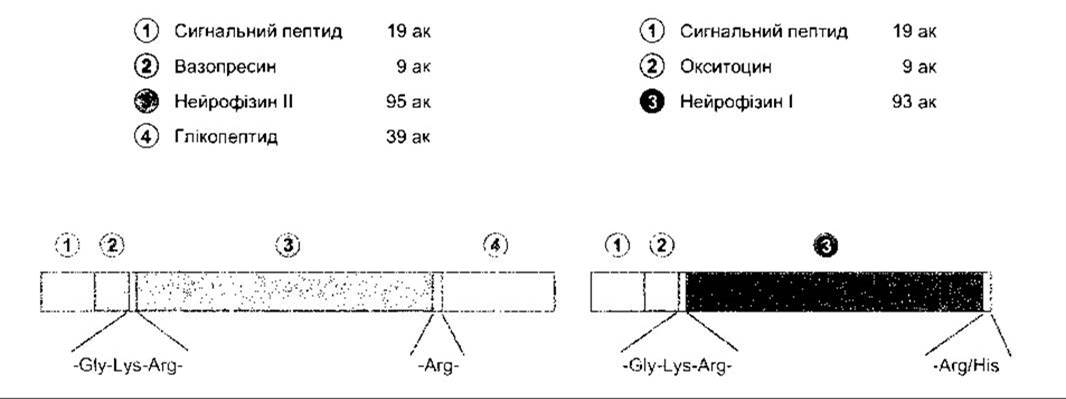
Рис. 14-12. Структура препропресофізину (ліворуч) і препрооксифізину (праворуч) бика. Гліцин у положенні 10 обох пептидів необхідний для амінування гліцинового залишку в положенні 9; ак - амінокислотні залишки (відтворено за дозволом з Richter D: Molecular events in expression of vasopressin and oxytocin and their cognate receptors).
Регулювання секреції вазопресину: осмотичні подразники
Вазопресин накопичується в задній частці гіпофіза і виділяється в кров’яне русло у відповідь на імпульси, що надходять нервовими волокнами, які містять цей гормон. Фактори, що впливають на секрецію, наведені в табл. 14-2. З підвищенням ефективного осмотичного тиску в плазмі понад нормальний рівень (285 мосмоль/кг) частота імпульсів у нейронах збільшується і, відповідно, зростає рівень секреції вазопресину (рис. 14-14). За рівня 285 мосм/кг концентрація вазопресину у плазмі є біля або на межі чутливості наявних методів, проте очевидно, що вона ще менша у випадку зменшення осмоляльності плазми нижче від нормального рівня. Секрецію вазопресину регулюють осморецептори передньої ділянки гіпоталамуса. Вони є поза гематоенцефалічним бар’єром і, вірогідно розміщені в навколошлуночкових органах, головно в судинному органі кінцевої пластинки (див. Розділ 32). Осмотичний поріг спраги (див. рис. 14-8) перебуває на тому ж рівні або незначно вищому від рівня порогу збудження, що забезпечує зростання секреції вазопресину (див. рис. 14-14), проте досі незрозуміло, чи ті ж самі рецептори опосередковують обидві реакції.
Отже, регулювання секреції вазопресину відбувається за допомогою чутливого механізму зворотного зв’язку, що забезпечує постійність осмоляльності плазми. Рівень секреції вазопресину помітно змінюється у разі зміни осмоляльності вже на 1%. Тому осмоляльність плазми практично здорових людей перебуває на рівні, дуже близькому до 285 мосмоль/л.
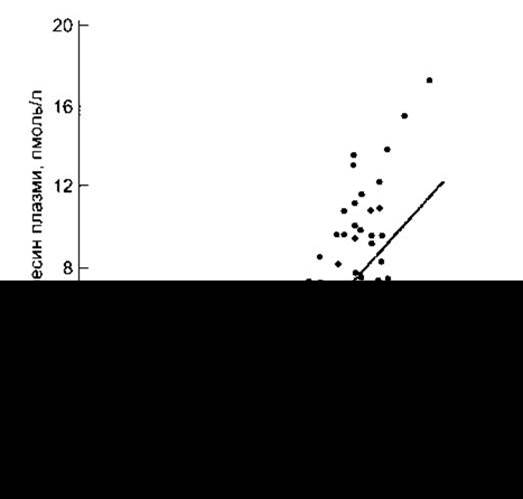
Рис. 14-14. Співвідношення осмоляльності плазми і концентрації вазопресину в плазмі практично здорових людей під час уведення гіпертонічного розчину. MB-межа визначення (відтворено за дозволом з Thompson CJ et al: The osmotic thresholds for thirst and vasopressin are similar in healthy humans. Clin Sei [Colch] 1986;71:651).
Таблиця 12-2. Фактори впливу на секрецію вазопресину
Підвищують секрецію вазопресину |
Знижують секрецію вазопресину |
Підвищений ефективний осмотичний тиск плазми Зменшений об’єм позаклітинної рідини Біль, емоції, «стрес», фізичні вправи Нудота і блювання Стояння Клофібрат, карбамазепін Ангіотензин II |
Знижений ефективний осмотичний тиск плазми Збільшений об’єм позаклітинної рідини Алкоголь |
Вплив об’єму
Зміна об’єму ПКР, як зазначено вище, зумовлює зміну секреції вазопресину. Секреція вазопресину підвищується зі зменшенням об’єму ПКР і знижується у разі її збільшення (див. табл. 14-2). Є обернена залежність між рівнем секреції вазопресину і частотою імпульсів в аферентних нейронах, що проходять від рецепторів розтягування судинної системи в її відділах з низьким і високим тиском. Рецептори низького тиску містяться в стінках великих вен, правому і лівому передсердях, а також у легеневих судинах; рецептори високого тиску - це рецептори сонної пазухи і дуги аорти (див. Розділ 31). Крива експоненціального підвищення концентрації вазопресину в плазмі, зумовленого зниженням кров’яного тиску, показана на рис. 14-15. Проте рецептори низького тиску реагують на наповнення судинної системи. Незначне зменшення об’єму крові знижує тиск у великих венах без зниження тиску артеріального, а також підвищує рівень вазопресину в плазмі.
Отже, рецептори низького тиску є важливими ініціаторами впливу, зумовленого наповненням судинного русла, на секрецію вазопресину. Імпульси від цих рецепторів поширюються блукаючим нервом до ядра поодинокого шляху (ЯПШ). З ЯПШ гальмівні імпульси проходять до каудального відділу вентролатеральної частини довгастого мозку (КВЛМ), а звідси починається безпосередній збуджувальний шлях до гіпоталамуса. Ангіотензин II, впливаючи на навколошлуночкові органи (див. Розділ 32), підвищує секрецію вазопресину, посилюючи цим реакцію на гіповолемію і гіпотензію.
У разі гіповолемії та гіпотензії, зумовлених, зокрема, крововтратою, виділяються значні кількості вазопресину, і у випадку гіповолемії крива осмотичності зміщується ліворуч (рис. 14-16); її кут теж зростає. Наслідком дії вазопресину є затримання води і зменшення осмоляльності плазми. У цьому разі простежується зменшення концентрації в плазмі Na+, розвивається гіпонатріємія.
Інші фактори впливу на секрецію вазопресину
Окрім зміни осмотичного тиску й об’єму ПКР, факторами впливу на секрецію вазопресину є біль, нудота, хірургічний стрес і деякі емоції (див. табл. 14-2). Особливо значна кількість вазопресину виділяється в разі нудоти. Алкоголь знижує секрецію вазопресину.
Клінічні аспекти
За умов різних клінічних ситуацій зміна об’єму рідини чи інші неосмотичного типу подразники впливають на осмотичне регулювання секреції вазопресину. Наприклад, у пацієнтів після хірургічного втручання може підвищуватися рівень вазопресину в плазмі внаслідок болю і гіповолемії, що спричинить зниження осмоляльності плазми і дилюційну гіпонатріємію. В пацієнтів з гіперсекрецією вазопресину високий рівень споживання рідини може зумовити водну інтоксикацію.
У разі синдрому «невідповідної» гіперсекреції антидіуретичного гормону (SIADH - від англ. syndrome of «inappropriate» hypersecretion of antidiuretic hormone) вазопресин спричинює не тільки дилюційну гіпонатріємію, а також, зменшуючи секрецію альдостерону (див. Розділ 20), - втрату солей з сечею, якщо процес утримання води достатній, щоб поповнювати об’єм ПКР. Такий стан є в хворих з мозковими («церебральна втрата солей») або легеневими патологіями («легенева втрата солей»). Гіперсекреція вазопресину в хворих з легеневими патологіями, зокрема в разі раку легень, може бути частково зумовлена припиненням гальмівних імпульсів в аферентних волокнах блукаючого нерва, що Генеруються в рецепторах розтягування передсердь і великих вен. Однак відомо, що значна кількість пухлин легень і деякі інші новоутворення продукують вазопресин. Пацієнтів з невідповідною гіперсекрецією вазопресину можна успішно лікувати демеклоцикліном - антибіотиком, що послаблює реагування нирок на вазопресин.

Рис. 14-15. Співвідношення артеріального тиску і концентрації вазопресину в плазмі практично здорових людей, у яких уведенням сумірних доз гангліоблокатора триметафану спричинено поступове зниження кров’яного тиску. Крива співвідношення більше експоненційна, ніж лінійна (за даними з Baylis PH: Osmoregulation and control of vasopressin secretion in healthy humans. Am J Physiol 1987; 253:R671).
Нецукровий діабет - це синдром, зумовлений недостатністю вазопресину або нечутливістю до нього епітелію ниркових канальців.
Причини недостатності вазопресину - патологічні процеси в надзоровому і пришлуночковому ядрах, у гіпоталамогіпофізарному тракті або в задній частці гіпофіза. З’ясовано, що 30% клінічних випадків спричинені ушкодженням гіпоталамуса пухлинним процесом (як первинним, так і метастазами); 30% є наслідком отриманої травми; 30% мають ідіопатичний характер; решта зумовлені ушкодженням судин, інфекціями, системними захворюваннями, зокрема саркоїдозом, що ушкоджує гіпоталамус, або мутаціями в гені препропресофізину. Порушення, що виникають після хірургічного видалення задньої частки гіпофіза, можуть бути тимчасовими, якщо ушкоджено лише дистальні кінці волокон, що відходять з надзорового і пришлуночкового ядер, оскільки ці волокна регенерують, налагоджують нові зв’язки з судинами і відновлюють виділення вазопресину. Симптомами нецукрового діабету є виділення великої кількості розведеної сечі (поліурія), споживання великої кількості рідини (полідипсія) за умови, що механізми контролювання спраги не порушені. Полідипсія в цьому випадку позитивна. За умов гальмування відчуття спраги з будь-якої причини споживання води зменшується, з’являється дегідратація, яка може мати фатальні наслідки.
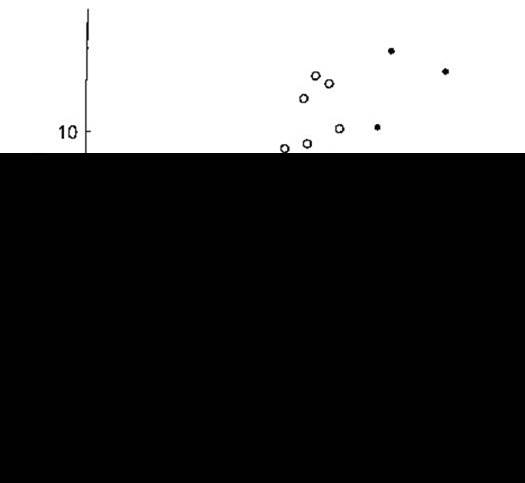
Рис. 14-16. Вплив гіповолемії і гіперволемії на співвідношення між концентрацією вазопресину в плазмі (АДГ) і осмоляльністю плазми (посмоль). Сім зразків крові взяті в різний час від десяти практично здорових людей, у яких утриманням від пиття води спричинено гіповолемію, а згодом - гіперволемію введенням гіпертонічного розчину (чорні кружки, суцільна лінія). За допомогою лінійного регресивного аналізу виявлено співвідношення АДГ=0,52 (посмоль - 283,5) у випадку утримання від споживання води і АДГ=0,38 (посмоль - 285,6) у разі введення гіпертонічного розчину. MB - межа визначення. Зверніть увагу на збільшення кута кривої та переміщення кривої ліворуч у разі гіповолемії (CJ Thompson).
Інша причина нецукрового діабету - нечутливість епітелію ниркових канальців до вазопресину (нефрогенний нецукровий діабет). У випадку одної з форм захворювання природжений дефект V2-рецептора, що виникає внаслідок різних мутацій гена цього рецептора, призводить до порушеності утворення цАМФ. Ця вада Х-залежна, оскільки V2-ген розміщений у Х-хромосомі. В іншій формі мутації в аутосомному гені аквапорину 2 зумовлюють утворення нефункційних водних каналів. Цікаво, що аквапорин 2 у нормі наявний у сечі, а в разі нецукрового діабету, зумовленого дефіцитом вазопресину, ін’єкція агоніста вазопресину спричинює швидке збільшення концентрації аквопорину 2 в сечі. Однак у випадку нефрогенного нецукрового діабету такого зростання не простежується.
Вплив на перебіг нецукрового діабету супутньої недостатності передньої частки гіпофіза розглянуто в Розділі 22.
Дія окситоцину
Окситоцин діє головно на молочну залозу і матку, хоча може також брати участь і в процесі лютеолізу (див. Розділ 23). Зв’язані з G-білком серпентинові окситоцинові рецептори виявлені в міометрії людини, а ідентичні або подібні рецептори - також у тканинах молочної залози і яєчника. Ці рецептори зумовлюють зростання внутрішньоклітинної концентрації Са2+.
У ссавців окситоцин спричинює скорочення міоепітеліальних клітин - клітин, подібних до гладком’язових, що вистилають протоки молочної залози. Під час лактації це зумовлює витискання молока з альвеол залози в молочний синус і витікання його через сосок (виділення молока). Багато гормонів, взаємодіючи, забезпечують процес зростання молочної залози і секрецію молока (див. Розділ 23), проте виділення молока в більшості видів регульоване окситоцином.
Рефлекс виділення молока
Виділення молока ініційоване нейрогуморальним рефлекторним шляхом. Рецепторами слугують нервові закінчення дотику, яких багато в молочній залозі, особливо навколо соска. Імпульси, що генеруються в цих рецепторах, проходять соматичними шляхами дотику до над зорового і пришлуночкового ядер. Збудження в окситоциновмісних нейронах приводить до виділення окситоцину задньою часткою гіпофіза (див. рис 14-13). Немовля, смокчучи груди, подразнює рецептори дотику, внаслідок чого відбувається стимулювання нейронів надзорового і пришлуночкового ядер, виділяється окситоцин, молоко надходить у молочні синуси і далі до ротової порожнини зголоднілого немовляти. В період лактації подразнення статевих органів, а також емоції теж можуть зумовити виділення окситоцину, інколи спричинюючи витікання молока.
Інші функції окситоцину
Окситоцин спричинює скорочення гладких м’язів матки. Чутливість мускулатури матки до окситоцину підсилює естроген і пригнічує прогестерон. Гальмівний вплив прогестерону зумовлений безпосередньою дією стероїдів на окситоцинові рецептори матки. В пізній період вагітності чутливість матки до окситоцину посилюється, що супроводжується помітним збільшенням кількості окситоцинових рецепторів і мРНК окситоцинових рецепторів (див. Розділ 23). Секреція окситоцину збільшується під час пологів. Після розкриття шийки матки просування плоду пологовим каналом ініціює імпульси в аферентних нервах, які проходять до надзорового і пришлуночкового ядер, зумовлюючи секрецію тієї кількості окситоцину, що потрібна для посилення родової діяльності (див. рис. 23- 41). Кількість окситоцину є нормальною на початку пологів. Можливо, що помітне в цей період збільшення кількості окситоцинових рецепторів за нормального рівня окситоцину ініціює скорочення і забезпечує позитивний зворотний зв’язок. Проте кількість окситоцину в матці у цей період збільшена і, отже, локальне продукування окситоцину теж може відігрівати деяку роль.
Окситоцин може так само впливати і на невагітну матку, сприяючи рухові сперми. Проходження сперми через жіночі статеві шляхи до маткових труб, де переважно відбувається запліднення, залежить не тільки від рухливості сперматозоїдів, а й, принаймні в деяких випадках, від скорочення матки. Подразнення геніталій під час статевого акту зумовлює виділення окситоцину, однак не доведено, що саме окситоцин у цьому разі ініціює спеціфічні рухи матки, які сприяють переміщенню сперми. Секрецію окситоцину стимулюють стресові подразники і пригнічує, як і вазопресину, алкоголь.
Кількість окситоцину в крові, що циркулює, збільшується в чоловічому організмі під час еякуляції, і можливо, це зумовлює посилене скорочення гладких м’язів сім’явиносної протоки, а, отже, просування сперми в напрямі сечівника.