Фізіологія людини - Вільям Ф. Ґанонґ 2002
Ендокринна система, метаболізм і репродуктивна функція
Енергетичний баланс, метаболізм і живлення
Проміжний обмін
Загальні поняття
Кінцеві продукти процесу травлення (див. Розділи 25 та 26) - це здебільшого амінокислоти, а також продукти розщеплення жирів і гексози: фруктоза, галактоза та глюкоза. Всмоктування і метаболізування цих сполук в організмі відбувається різними шляхами. Деталі їхнього метаболізму стосуються біохімії, тому ми їх не розглядаємо. Та оскільки деякі знання шляхів метаболізму важливі для розуміння дії тиреоїдних, панкреатичних і надниркових гормонів, то в цьому розділі описано загальні принципи обміну вуглеводів, білків і жирів.
Загальна схема обміну речовин
Коротколанцюгові фрагменти, що утворюються внаслідок розщеплення гексози, амінокислоти і жиру, подібні. З цього спільного метаболічного пулу проміжних продуктів можуть синтезуватись вуглеводи, білки і жири, хоча перетворення жирів у вуглеводи обмежене (див. нижче). Проміжні продукти також входять у цикл лимонної кислоти - кінцевий спільний шлях катаболізму, у якому вони розщеплюються до атомів водню і СО2, Атоми водню окиснюються з утворенням води в ланцюгу флавопротеїнових і цитохромних ензимів.
Перенесення енергії
Більшість енергії, що вивільняється під час катаболізму, не використовують безпосередньо клітини, вона витрачається на утворення зв’язків між залишками фосфорної кислоти і деякими органічними сполуками. Оскільки для утворення такого типу зв’язку потрібно багато енергії, то під час наступного гідролізу цього зв’язку відбувається вивільнення енергії також у відповідно великих кількостях (10-12 ккал/моль). Сполуки, що містять такі зв’язки, називають високоенергетичними фосфатними сполуками. Не всі органічні фосфати є високоенергетичними сполуками. Багато з них, зокрема глюкозо-6-фосфат, належать до низькоенергетичних фосфатів, і під час їхнього гідролізу вивільняється лише 2-3 ккал/моль.
Окремі проміжні продукти, що утворюються внаслідок метаболізму вуглеводів, є високоенергетичними, проте найважливіша високоенергетична фосфатна сполука - аденозинтрифосфат (АТФ). Ця молекула (рис. 17-3) є головним носієм енергії в організмі.
Під час гідролізу АТФ до аденозиндифосфату (АДФ) вивільняється енергія для виконання таких процесів, як м’язові скорочення, активне транспортування і синтез багатьох хімічних сполук. Відщеплення ще одного фосфату з утворенням аденозинмонофосфату (АМФ) теж зумовлює вивільнення великої кількості енергії. Інша високоенергетична фосфатна сполука, що міститься в м’язах, - креатинфосфат (КФ; фосфокреатин) (див. нижче).
Важливими фосфорильованими сполуками, які зрештою теж можуть слугувати донорами енергії, є трифосфатні похідні інших піримідинових і пуринових основ (див. рис. 17-22), а саме: похідна гуаніну - гуанозинтрифосфат (ГТФ), важлива сполука для передавання сигналів (див. Розділ 1); похідна цитозину - цитидинтрифосфат (ЦТФ), похідна урацилу - уридинтрифосфат (УТФ), похідна гіпоксантину - інозинтрифосфат (ІТФ). З утворенням високоенергетичних фосфатів пов’язана значна кількість катаболічних реакцій.
Іншою групою високоенергетичних сполук є тіоефіри - ацильні похідні меркаптанів. Коензим А (КоА) - це поширений меркаптан, що містить аденін, рибозу, пантотенову кислоту і тіоетаноламін (рис. 17-4).
Відновлений КоА (HS-KoA) реагує з ацильними групами (R-CO-), утворюючи похідні R-CO-S-KoA. Прикладом може бути реакція HS-KoA й ацетатної кислоти з утворенням ацетилкоензиму А (ацетил-КоА) - однієї з головних сполук проміжного обміну. Оскільки ацетил-КоА є високоенергетичнішою сполукою, ніж ацетатна кислота, то він легко сполучається з речовинами в реакціях, що в інших випадках потребували б значних зовнішніх затрат енергії. Тому ацетил-КоА часто називають «активним ацетатом». З погляду енергетики утворення 1 моля будь-якої сполуки ацетил-КоА еквівалентне утворенню 1 моля АТФ.
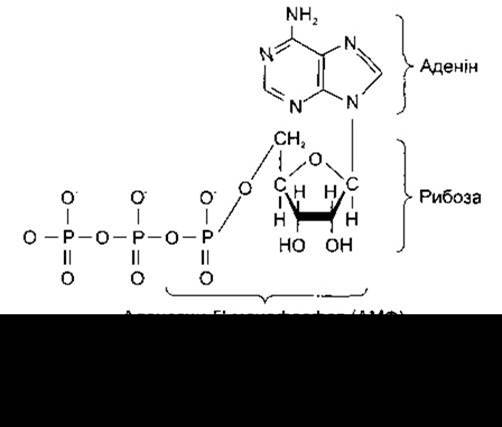
Рис. 17-3. Високоенергетичні похідні аденозину (відтворено за дозволом з Murray RK et al: Harper’s Biochemistry, 25th ed. McGraw-Hill, 2000).
Біологічне окиснення
Окиснення - це сполучення речовини з О2 або відщеплення від неї водню чи електронів. Зворотні процеси називають відновленням. Біологічне окиснення каталізують спеціальні ензими. Кофактори, або коензими (органічні небілкові сполуки), є допоміжними речовинами, що слугують переважно для перенесення продуктів реакції. Як і ензими, коензими теж можуть каталізувати різноманітні реакції.
Багато коензимів є акцепторами водню. Одна з найпоширеніших форм біологічного окиснення - відщеплення водню від R-OH груп з утворенням R=О. У таких реакціях дегідрогенізації нікотинамідаденіндинуклеотид (НАД+) і нікотинамідаденіндинуклеотидфосфат (НАДФ+) приєднують водень, перетворюючись на відновлений нікотинамідаденіндинуклеотид (НАДхН) або нікотинамідаденіндинуклеотидфосфат (НАДФхН) (рис. 17-5). Далі водень переходить у флавопротеїнцитохромну систему, а коензими реоксидується до НАД+ і НАДФ+. Флавінаденіндинуклеотид (ФАД) виникає шляхом фосфорилювання рибофлавіну, і утворений таким способом флавінмононуклеотид (ФМН) далі сполучається з АМФ, формуючи динукдеотид. ФАД може подібно приєднувати водень, утворюючи гідро- (ФАДхН) і дигідропохідні (ФАДхН2).
Флавопротеїнцитохромна система - це ланцюг ензимів, що переносять водень (протони й електрони) до кисню з утворенням води. Цей процес відбувається в мітохондріях. Під час перенесення водню кожен ензим ланцюга почергово відновлюється й окиснюється. Кожен ензим ланцюга - це білкова молекула, до якої приєднана небілкова простетична група. Останнім ензимом у ланцюзі є цитохром-оксидаза, яка переносить електрони до О2 з утворенням Н2О. Цей ензим містить два атоми Fe і три атоми Cu. Він має 13 субодиниць.
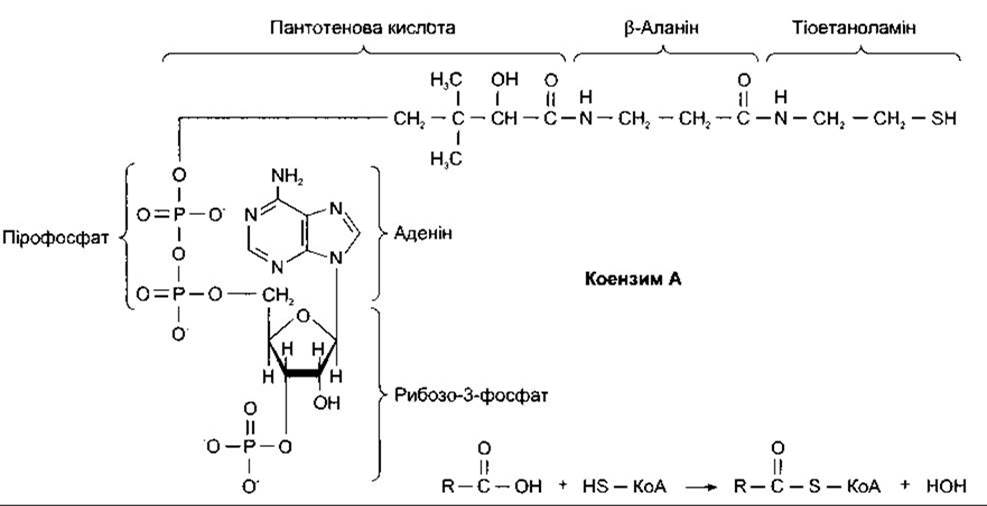
Рис. 17-4. Ліворуч: формула відновленого коензиму A (HS-KoA). Праворуч: реакція коензиму А та біологічно активних сполук з утворенням тіоефірів; R - залишок молекули.
Окисне фосфорилювання
Утворення АТФ, пов’язане з окисненням у флавопротеїнцитохромній системі, називають окисним фосфорилюванням. АТФ може утворюватись і в інших умовах, коли хімічні реакції відбуваються з вивільненням значної кількості енергії. Ці реакції називають фосфорилюванням на субстратному рівні. У разі окисного фосфорилювання протони переносяться через внутрішню мембрану, що утворює кристи мітохондрій, і відбувається це одночасно з окисненням у дихальному ланцюгу (рис. 17-6). У мембрані виникає електрохімічний градієнт протонів, а зворотне переміщення протонів у матрикс є рушійною силою процесу сполучення АДФ та неорганічного фосфату (Рі) з утворенням АТФ, що його каталізує АТФ-аза мембрани (АТФ-синтаза, F-АТФ-аза) (рис. 17-7). Цей складний ензим, або подібний до нього, міститься в мембранах бактерій, де його активує окиснення, і в рослинах, де його активує світло (фотосинтез). Він має F1 та F0 частини і містить більше, ніж дванадцять субодиниць.

Рис. 17-5. Угорі: Окиснена форма нікотинамідаденіндинуклеотиду (НАД+). Нікотинамідаденіндинуклеотидфосфат (НАДФ+) має додаткову фосфатну групу, позначену зірочкою. Внизу: Реакція, у якій НАД+ і НАДФ+ відновлюються з утворенням НАДхН і НАДФхН; R - залишок молекули; R’ - донор водню.
Окисне фосфорилювання залежить від забезпечення молекулами АДФ і, отже, частково регульоване шляхом зворотного зв’язку; інтенсивніше використання тканинами АТФ зумовлює більше накопичення АДФ і, відповідно, вищий рівень окисного фосфорилювання. Іншими чинниками регулювання рівня утворення АТФ є рівень постачання жирів, лактату і метаболітів глюкози до матриксу мітохондрій, а також наявність О2.
Здебільшого 90% спожитого О2 використовується в процесах, що відбуваються в мітохондріях, а 80% цієї кількості - для синтезування АТФ. Близько 27% АТФ використовується для синтезування білків, майже 24% - Na+-K+- АТФ-азою, 9 - для глюконеогенезу, 6 - Са2+ АТФ-азою, 5 - міозин АТФ-азою і 3% - для синтезування сечовини. Крім функції перенесення енергії, АТФ є молекулою-попередником цАМФ (див. Розділ 1).