Фізіологія людини - Вільям Ф. Ґанонґ 2002
Кровообіг
Рідини, що циркулюють в організмі
Кров - Лейкоцити
У нормі в мікролітрі крові людини міститься 4 000-11 000 лейкоцитів (табл. 27-1). З них найчисленнішими є гранулоцити (поліморфонуклеарні лейкоцити (ПМН)).
Молоді гранулоцити мають сідлоподібне ядро, яке стає мультилобулярним у разі дозрівання клітин (рис. 27-2). Більшість із них містять нейтрофільні гранули (нейтрофіли), однак деякі - гранули, що сприймають кислі барвники (еозинофіли); частина клітин містить базофільні гранули (базофіли). До інших двох клітинних типів, що в нормі виявляються у периферійній крові, належать лімфоцити, які мають велике округле ядро та незначну цитоплазму, і моноцити з агранулярною цитоплазмою та ядром, форма якого нагадує нирку (див. рис. 27-2). Взаємодія цих клітин забезпечує ефективний захист організму від пухлин, вірусів, бактерій та паразитів.
Гранулоцити
Усі гранулоцити мають цитоплазматичні гранули, що містять біологічно активні речовини, задіяні у запальних та алергійних реакціях. Середня тривалість напівжиття нейтрофіла у периферійній крові становить 6 год. Отже, для підтримки нормальної кількості цих клітин потрібне утворення 100 мільярдів нейтрофілів за день. Багато нейтрофілів проникає у тканини. Їх приваблюють до поверхні ендотелію селектини, і вони котяться вздовж цієї поверхні. Пізніше формується щільний зв’язок між ендотелієм та лейкоцитами за допомогою адгезивних молекул нейтрофілів з родини інтегринів. Наступним процесом є проникнення нейтрофілів через стінку капілярів між ендотеліальнимими клітинами. Цей процес називають діапедезом. Значна частина клітин, що виходить з крові, надходить у шлунково-кишковий тракт і виводиться з організму. Інвазія бактерій в організм зумовлює запальну відповідь. Кістковий мозок стає активним, продукує та виділяє значну кількість нейтрофілів. Унаслідок взаємодії бактеріальних продуктів та плазмових факторів і клітин крові утворюються сполуки, що приваблюють нейтрофіли в інфіковану ділянку (хемотаксис). Хемотаксичні фактори, що є представниками великої та поширеної родини хемокінів (див. нижче), охоплюють компоненти системи комплементу (С5а), лейкотрієни та поліпептиди лімфоцитів, мастоцитів та базофілів. Стимулювальний вплив С5а на хемотаксичну активність посилює Gс-глобулін. Цей білок міститься на мембрані нейтрофілів і бере участь у зв’язуванні та транспортуванні вітаміну D у плазмі (див. Розділ 21). Інші плазмові фактори, діючи на бактерії, роблять їх поживними для фагоцитів (опсонізація). Головними опсонінами, що вкривають бактерії, є імуноглобуліни певного класу (IgG) та білки системи комплементу (див. нижче). Вкриті бактерії пізніше приєднуються до рецепторів на мембрані нейтрофілів, що зумовлює посилення рухової активності клітини, екзоцитоз і так званий кисневий вибух. Наведені реакції опосередковує гетеротримерний G-білок. Посилена рухова активність призводить до швидкого перетравлення бактерії шляхом ендоцитозу (фагоцитоз). У випадку екзоцитозу з гранул нейтрофілів виділяються сполуки, що надходять у фагоцитарну вакуолю, де розміщені бактерії, та частково в інтерстиційний простір (деґрануляція). Гранули містять різноманітні протеази й антимікробні білки, які називають дефензинами. У ссавців є два типи дефензинів - а та ß; у безхребетних та рослин виявлено інші типи. Крім того, відбувається активування мембранозв’язаного ензиму НАДФ-оксидази, що супроводжується утворенням токсичних похідних кисню. Комбінація токсичних метаболітів кисню та протеолітичних ензимів гранул робить нейтрофіл дуже ефективним знаряддям знищення мікроорганізмів.
Таблиця 27-1. Показники кількості клітинних елементів у крові людини в нормі
Клітини |
Клітини/мкл, середнє значення |
Приблизні межі норми |
Відсотки від загальної кількості лейкоцитів |
Загальна кількість лейкоцитів |
9000 |
4000-11000 |
|
Ґранулоцити Нейтрофіли |
5400 |
3000-6000 |
50-70 |
Еозинофіли |
275 |
150-300 |
1-4 |
Базофіли |
35 |
0-100 |
0,4 |
Лімфоцити |
2750 |
1500-4000 |
20-40 |
Моноцити |
540 |
300-600 |
2-8 |
Еритроцити Жінки |
4,8 X 106 |
||
Чоловіки |
5,4 X 106 |
||
Тромбоцити |
300 000 |
200 000-500 000 |
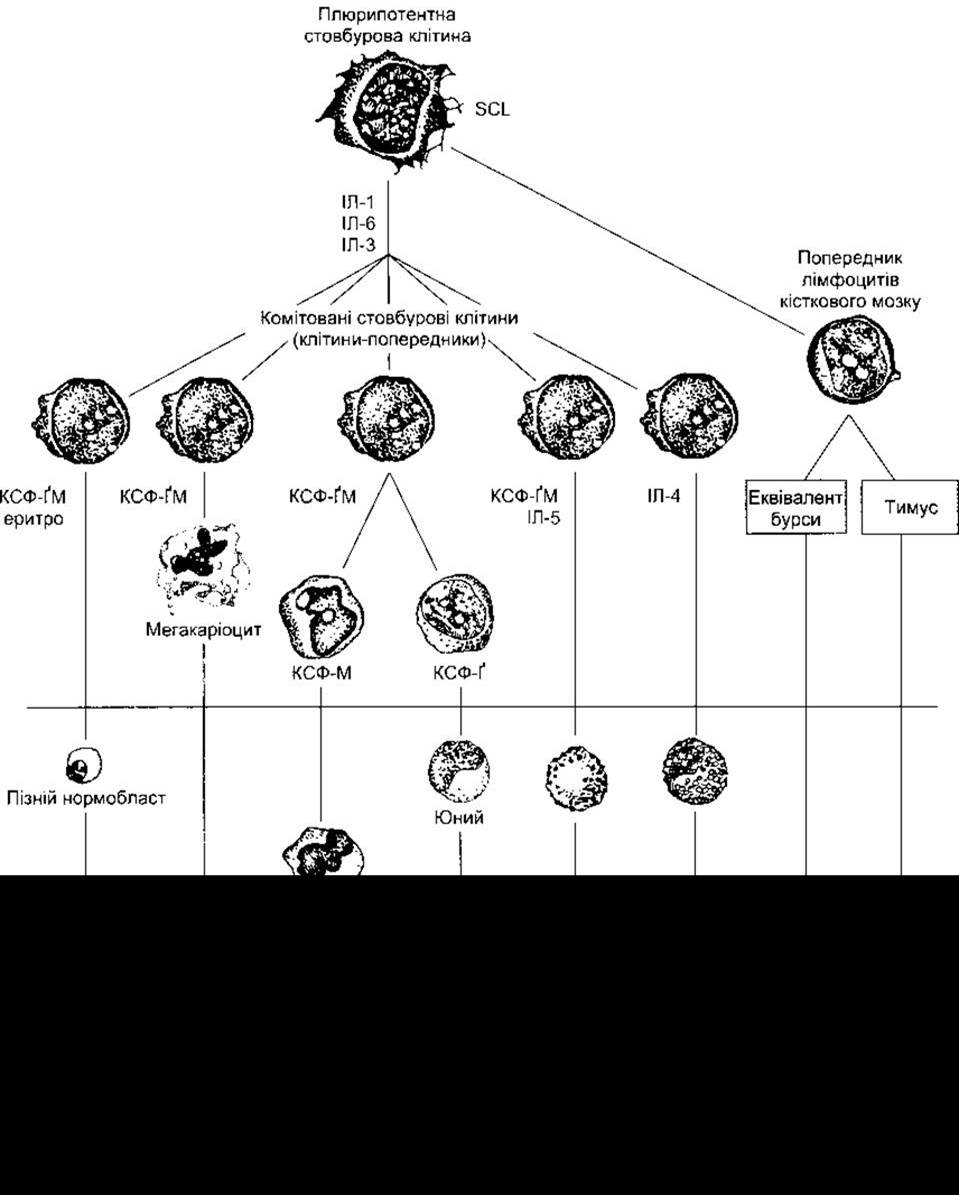
Рис. 27-2. Розвиток різних формених елементів крові з клітин кісткового мозку Клітини під горизонтальною лінією виявляються у периферійній крові в нормі. Позначені головні місця дії еритропоетину (еритро) та різноманітних колонієстимулювальних факторів (КСФ), що забезпечують диференціювання клітин; Ґ - ґранулоцити; М - макрофаги; ІЛ - інтерлейкін; див. табл. 27- 2 та 27-3.
Активування НАДФ-оксидази супроводжується значним посиленням поглинання та метаболізму О2 у нейтрофілі (респіраторний вибух) та утворенням О2 унаслідок таких реакцій:
![]()
Зазначимо, що О2 є вільним радикалом, який утворюється внаслідок додавання одного електрона до О2, це інколи позначають додаванням крапки для утворення символу О2.
Два О2 спонтанно реагують з двома Н+, утворюючи Н2О2 у реакції, яку каталізує цитоплазматична форма супероксиддисмутази (СОД):
![]()
Отже, стойхіометрія електронів (е ) буде такою:
![]()
Обидва - О2 та Н2О2 - є оксидантами зі значною бактерицидною активністю, однак Н2О2 перетворює у Н2О ензим каталаза. Цитоплазматична форма СОД містить Zn та Cu. Її фіксують у різних ділянках організму людини. У випадку родинної форми аміотрофічного бокового склерозу (АБС) (див. Розділ 16) простежується дефектна форма ензиму внаслідок генетичної мутації. Тому, можливо, під час цього прогресуючого, фатального захворювання О2 нагромаджується у моторних нейронах, зумовлюючи їхню загибель. У людей виявлено ще дві форми ензиму, кодовані принаймні одним іншим геном.
Нейтрофіли містять також ензим мієлопероксидазу, що каталізує перетворення Cl, Br, І та SCN у відповідні кислоти (НОСl, НОВr та ін.). Ці кислоти є також потенційними оксидантами. Оскільки Сl в рідинах організму є найбільше, то головним продуктом буде НОСl.
Крім мієлопероксидази та дефензинів, гранули нейтрофілів містять еластазу, дві металопротеїнази, що руйнують колаген, і різноманітні протеази, які допомагають знищити мікроорганізми. Ці ензими діють спільно з O2, Н2O2 та НОСl, що утворюються внаслідок дії НАДФ-оксидази та мієлопероксидази, формуючи зону знищення навколо активованого нейтрофіла. Ця зона є ефективною для знищення мікроорганізмів, однак у разі деяких захворювань, наприклад ревматоїдного артриту, нейтрофіли можуть спричинити місцеву деструкцію тканин організму.
Рухи клітини під час фагоцитозу, як і міграція у місце інфікування, забезпечені участю мікротрубочок та мікрофіламентів (див. Розділ 1). Нормальна діяльність мікрофіламентів передбачає взаємодію актину, який вони містять, з міозином І на внутрішній поверхні клітинної мембрани (див. Розділ 1). Нейтрофіли виділяють також тромбоксани, що є вазоконстрикторами, та фактори агрегації тромбоцитів, лейкотрієни, що підвищують проникність судин і приваблюють інші нейтрофіли у місце запалення, та інші простагландини, які виявляють помірну протизапальну активність.
Подібно до нейтрофілів, еозинофіли теж мають короткий період півжиття у периферійній крові, теж їх приваблюють до поверхні ендотеліальних клітин селектини, теж вони приєднуються до інтегринів, що зв’язують їх з судинною стінкою, та проникають у тканини шляхом діапедезу. Як і нейтрофіли, вони виділяють білки, цитокіни та хемокіни, що зумовлюють запалення та спроможні знищити мікроорганізми. Однак є деяка специфічність у селектинах та інтегринах, що забезпечують взаємодію клітин, та у молекулах, які виділяються для знищення мікроорганізмів. Дозрівання й активування еозинофілів у тканинах частково стимульоване ІЛ-3, ІЛ-5 та КСФ-ҐМ (див. нижче). Особливо багато цих клітин у слизовій шлунково-кишкового тракту, де вони забезпечують захист від паразитів, та у слизових дихальних шляхів і сечовидільних органів. Кількість еозинофілів, що циркулюють, збільшується в разі алергічних захворювань, таких як астма, та у випадку різноманітної патології дихальних шляхів і шлунково-кишкового тракту.
Базофіли також проникають у тканини та виділяють білки і цитокіни. Вони подібні, однак не є ідентичними до мастоцитів (тканинних базофілів), та, як і ті, містять гістамін та гепарин (див. нижче). Базофіли виділяють гістамін та інші трансмітери запалення в разі активування фактора виділення гістаміну, що його секретують Т-лімфоцити (див. нижче), які є важливими під час реакцій гіперчутливості негайного типу. Діапазон таких реакцій охоплює незначну кропивницю й анафілактичний шок.
Тканинні базофіли
Тканинні базофіли (мастоцити) - це гранульовані мобільні клітини, які виявляють у ділянках, багатих на сполучну тканину, і особливо під епітеліальними поверхнями. У гранулах клітин міститься гістамін, гепарин та багато протеаз. Ці клітини також утворюють і виділяють лейкотрієни та простагландини. На їхній клітинній мембрані розміщені IgE-рецептори, і, подібно до базофілів, після приєднання до їхньої поверхні антигену, вкритого IgE, відбувається деґрануляція. Клітини беруть участь у запальній реакції, ініційованій IgE та IgG (див. нижче). У випадку запалення вони знищують збудників, що зробили інвазію в організм. Крім участі у реакціях набутого імунітету, клітини виділяють ФНП-a у відповідь на появу бактеріальних продуктів, використовуючи антілонезалежні механізми. Отже, вони беруть участь у неспецифічних імунних реакціях, спрямованих проти інфекційних агентів (див. нижче). Виражена деґрануляція тканинних базофілів зумовлює клінічні прояви алергії, у тім числі анафілактичні реакції.
Моноцити
Моноцити потрапляють у кров з кісткового мозку і циркулюють протягом 72 год. Потім вони проникають у тканини і стають тканинними макрофагами (рис. 27-3).
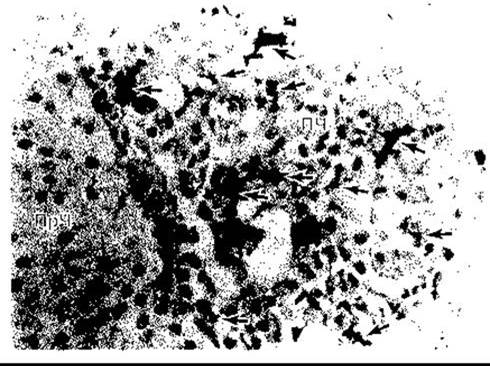
Рис. 27-3. Тканинні макрофаги у гіпофізі. Макрофаги, позначені стрілками, були пофарбовані імуногістохімічним методом з використанням моноклональних антитіл, специфічних для цих клітин; ПЧ - передня частка; ПрЧ - проміжна частка (за дозволом S Gordon)
Тривалість їхнього існування у тканинах невідома, однак дані, одержані внаслідок трансплантації кісткового мозку у людини, свідчать про те, що вони можуть існувати близько трьох місяців. Виявляється, що вони не повертаються у систему кровообігу. Деякі з них закінчують існування у вигляді багатоядерних велетенських клітин, що виявляються в разі хронічних запальних процесів, наприклад, туберкульозу. До тканинних макрофагів належать клітини Купфера у печінці, альвеолярні макрофаги (див. Розділ 34) та мікроглія головного мозку; всі вони виходять з кровоносної системи. Раніше їх називали ретикулоендотеліальною системою, проте загальний термін система тканинних макрофагів точніший.
Т-лімфоцити виділяють макрофаги, які активують лімфокіни. Активовані макрофаги мігрують у відповідь на вплив хемотактичних стимулів, де вони поглинають та знищують бактерії за допомогою механізмів, подібних до тих, що відбуваються у нейтрофілах. Макрофаги відіграють провідну роль у забезпеченні імунітету (див. нижче). Вони також виділяють близько 100 різноманітних сполук, у тім числі фактори, що впливають на лімфоцити й інші клітини, простагландини групи Е та фактори зсідання крові.
Колонієстимулювальні фактори ґранулоцитів та макрофагів
Утворення еритроцитів та лейкоцитів, що чітко регульоване у здоровому організмі, швидко і значно посилюється в разі інфекцій. Проліферація та відновлення плюрипотентних клітин у мишей та, вірогідно, у людей залежить від утворення клітинами білка, кодованого геном sei (від англ. stem cell leukemia - лейкемія стовбурових клітин). Задіяними є також інші фактори. Проліферація і дозрівання клітин, що потрапляють у кров з кісткового мозку, регульовані глікопротеїнами факторів росту або гормонами, які спричинюють проліферацію та дозрівання клітин з однієї або декількох детермінованих клітинних ліній (див. рис. 27-2, табл. 27-2). Регулювання утворень еритроцитів еритропоетином описане у Розділі 24. Три додаткові фактори називають колонієстимулювальними факторами (КСФ), оскільки вони зумовлюють проліферацію однієї відповідної клітини на м’якому агарі, утворюючи колонії на цьому середовищі. До факторів, що стимулюють утворення детермінованих стовбурових клітин, належать КСФ ґранулоцитів та макрофагів (КСФ-ҐМ), КСФ гранулоцитів (КСФ-Ґ), та КСФ макрофагів (КСФ-М). Інтерлейкіни (з англ. interleukins) ІЛ-1, ІЛ-6, а потім ІЛ-3 (див. табл. 27-2) діють послідовно, призводячи до перетворення плюрипотентних недетермінованих стовбурових клітин у детерміновані клітини-попередники (див. рис. 27-2). Інтерлейкін ІЛ-3 відомий також як мульти-КСФ. Кожний з КСФ виконує головну функцію, проте, крім неї, усі КСФ та інтерлейкіни мають інші впливи. Вони можуть активувати та підтримувати зрілі клітини крові. Цікаво стосовно цього, що гени, які кодують більшість описаних факторів, розміщені разом на довгому відрізку 5-ї хромосоми, і їхнє походження може бути пов’язане з подвоєнням гена-попередника. Цікаво також, що в мишей у нормі простежується базальний гемопоез, за якого ген, що кодує КСФ-ҐМ, пригнічений. Це означає, що втрату одного з факторів можуть компенсувати інші. З іншого боку, відсутність КСФ- ҐМ зумовлює нагромадження сурфактанту у легенях (див. Розділ 34).
Таблиця 27-2. Фактори, що регулюють гемопоез
Назва |
Клітинні джерела |
Тип клітини, що утворюється в збільшеній кількості |
SCL |
? |
Плюрипотентні клітини |
Еритропоетин |
Клітини нирки, клітини Купфера |
Еритроцити |
КСФ-Ґ |
Моноцити, фібробласти, ендотеліальні клітини |
Нейтрофіли |
КСФ-М |
Моноцити, фібробласти, ендотеліальні клітини |
Моноцити |
КСФ-ҐМ |
Т-клітини, моноцити, фібробласти, ендотеліальні клітини |
Нейтрофіли, моноцити, еозинофіли, мегакаріоцити, еритроцити |
ІЛ-1 |
Макрофаги, фібробласти, ендотеліальні клітини |
Нейтрофіли, моноцити, еозинофіли, базофіли, мегакаріоцити, еритроцити |
ІЛ-3 |
Т-клітини |
|
ІЛ-4 |
Т-клітини |
Базофіли |
ІЛ-5 |
Т-клітини |
Еозинофіли |
ІЛ-6 |
Макрофаги, фібробласти, ендотеліальні клітини |
Нейтрофіли, моноцити, еозинофіли, базофіли, мегакаріоцити, еритроцити |
Як зазначено у Розділі 24, еритропоетин частково продукують клітини нирок, і він є гормоном, що циркулює. Інші фактори утворювані макрофагами, що активовані Т- клітинами, фібробластами та ендотеліальними клітинами. Здебільшого фактори діють місцево у кістковому мозку.
Порушення функції фагоцитозу
Описано понад 15 первинних дефектів діяльності нейтрофілів і ще щонайменше 30 інших станів, за яких простежується вторинне порушення функції нейтрофілів. Хворі з такими ураженнями схильні до інфекцій, які мають легкий перебіг за умови порушення функції лише нейтрофілів; якщо ж уражена і система моноцитів - тканинних макрофагів, то захворювання важкі. У випадку одного із синдромів (послаблення рухової активності нейтрофілів) не відбувається нормальної полімеризації актину, і рух клітини стає повільним, у разі іншого простежується вроджена недостатність лейкоцитарних інтегринів. За умов серйозніших захворювань (хронічні ґранулематозні хвороби) фіксують неспроможність утворювати O2 як у нейтрофілах, так і у моноцитах, унаслідок чого клітини не можуть знищити фагоцитовані бактерії. За вираженої вродженої недостатності глюкозо-6-фосфатдегідрогенази виникають множинні інфекції, оскільки неможливим стає утворення НАДФ, потрібного для продукування O2. У випадку вродженої недостатності мієлопероксидази ефективність знищення мікробів знижується внаслідок неспроможності утворювати йони гіпогалідів; однак вона не зникає повністю, оскільки інші бактерицидні механізми збережені.
Лімфоцити
Лімфоцити є ключовими елементами у формуванні імунітету (див. нижче). Після народження частина лімфоцитів утворюється у кістковому мозку, проте більшість з них формується у лімфовузлах, тимусі та селезінці з клітин-попередників. Клітини-попередники потрапляють у ці органи з кісткового мозку, пройшовши попереднє диференціювання у тимусі та місцях, еквівалентних бурсі Фабріціуса (див. нижче) для того, щоб стати попередниками Т- та В- клітин (рис. 27-4). Лімфоцити проникають у кров переважно через лімфатичні судини. За звичайних умов тільки 2% лімфоцитів організму містяться у периферійній крові. Більшість інших лімфоцитів перебувають у лімфоїдних органах. Було підраховано, що у людини 3,5 х 1010 лімфоцитів задень надходить у кров тільки через грудну протоку; хоча ця кількість охоплює лімфоцити, які надходять у грудну протоку повторно. Впливи гормонів надниркових залоз на лімфоїдні органи, лімфоцити, що циркулюють у крові, та гранулоцити розглянуто у Розділі 20.