Фізіологія людини - Вільям Ф. Ґанонґ 2002
Кровообіг
Серцево-судинний гомеостаз у нормі та в разі патології
Запалення та загоєння ран
Місцеве ушкодження
Запалення - це складна місцева реакція на впливи сторонніх факторів, таких як бактерії, або іноді на сполуки, що утворюються в організмі. Воно передбачає послідовність реакцій з початковим активуванням цитокінів, нейтрофілів, адгезивних молекул, комплементу та IgG. Деяку роль відіграє також PAF, сполука, що посилює запальну реакцію (див. Розділ 27). Пізніше приєднуються моноцити та лімфоцити. В ділянці запалення простежується розширення артеріол та збільшення проникності капілярної стінки (див. Розділи 31 та 32). Якщо запалення розвивається у шкірі або під нею (рис. 33-5), то типовим буде почервоніння, набрякання, посилена чутливість та біль. В інших органах запалення стає ключовим патогенетичним чинником астми, виразкового коліту та багатьох інших захворювань.
Дані досліджень свідчать про те, що важливу роль у запальній реакції відіграє фактор транскрипції - ядерний фактор кВ (NF- кВ - від англ. nuclear factor кВ). Фактор NF- кВ є гетеродимером, який у нормі міститься в цитоплазмі клітин у комплексі з ІкВа, що дає змогу йому перебувати у неактивному стані. Такі стимули, як цитокіни, віруси й оксиданти, зумовлюють відділення NF-кB від ІкВа з наступним руйнуванням їхніх Ва, NF- кВ рухається до ядра, де сполучається з ДНК генів, що кодують численні трансмітери запалення. Внаслідок цього посилюється синтез та виділення трансмітерів. Глюкокортикоїди пригнічують активування NF-КB, зменшуючи утворення ІкВа. Напевно, цей ефект є головним у механізмі протизапальної дії глюко- кортикоїдів (див. Розділ 20).
Системна відповідь на ушкодження
Цитокіни, що утворюються в разі запалення та інших ушкоджень, зумовлюють також системні прояви, до яких належать зміни кількості білків гострої фази (білки, концентрація яких збільшується або зменшується щонайменше на 25% після ушкодження). Значна кількість із цих білків утворюється в печінці; вони наведені у табл. 27-10. Їхній вміст показаний на рис. 33-6. Причини змін концентрації цих білків остаточно не з’ясовані, однак можна зазначити, що більшість з них має гомеостатичне значення. Наприклад, збільшення кількості С-реактивного білка активує моноцити і зумовлює подальше утворення цитокінів.
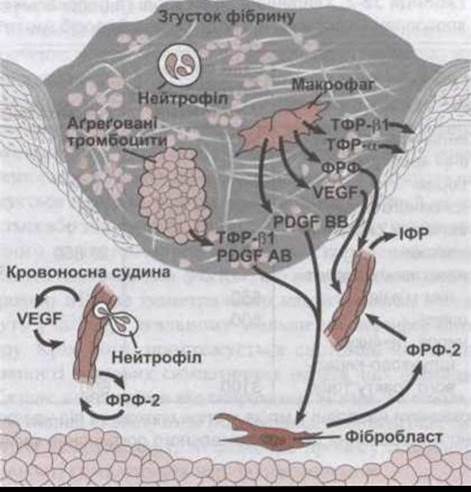
Рис. 33-5. Рана шкіри через три дні після ушкодження. Численні цитокіни та фактори росту регулюють процеси загоєння; VEGF (від англ. vascular endothelial growth factor) - судинний ендотеліальний фактор росту. Інші абревіатури див. у Додатку. Зверніть увагу на епітелій, що росте під згустком фібрину для поступового відновлення шкіри (модифіковано з Singler AJ, Clark RAF: Cutaneous wound healing. N Engl J Med 1999; 341: 738).
До інших змін, що виникають у відповідь на ушкодження, можна зачислити сонливість, негативний баланс азоту і гарячку.
Загоєння ран
У випадку ушкодження тканини тромбоцити прилипають до оголеного матриксу внаслідок взаємодії інтегринів з колагеном та ламініном (див. рис. 33-5). У процесі зсідання крові утворюється тромбін, який посилює агрегацію тромбоцитів та їхню дегрануляцію. Сполуки, що містяться в гранулах тромбоцитів, генерують запальну реакцію. Лейкоцити приваблювані селектинами і приєднуються до інтегринів ендотеліальних клітин, що зумовлює їхню міграцію через судинну стінку. Цитокіни, що їх виділяють лейкоцити, стимулюють інтегрини на макрофагах, які внаслідок цього мігрують у вогнище запалення. Активовані також рецептори фібробластів та епітеліальних клітин, які беруть участь у загоєнні та формуванні рубця. Плазмін сприяє загоєнню, видаляючи надлишок фібрину. Це приводить до мігрування кератиноцитів у рану та відновлення епітелію під струпом. Відбувається синтез колагену та утворення рубця. Рани набувають 20% їхньої кінцевої міцності через три тижні. Процес триває й далі, однак міцність у ділянці рани ніколи не перевищує 70% від міцності нормальної шкіри.
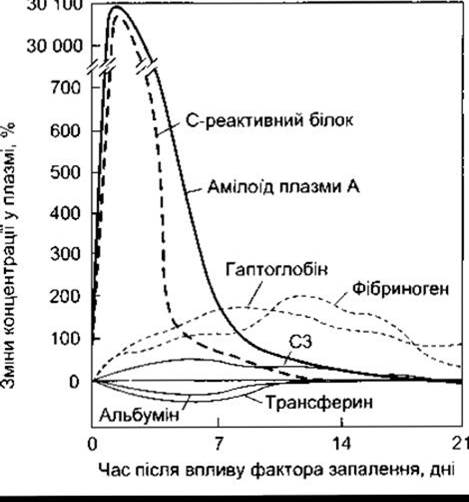
Рис. 33-6. Динаміка змін вмісту основних білків гострої фази; СЗ - компонент СЗ комплементу (модифіковано і відтворено за дозволом з Glitlin JD, Colten HR: Molecular biology of acute phase plasma proteins. In Pick F et al [editors]. Lymphokines, vol 14, pages 123-153 Academic Press, 1987).