Фізіологія людини - Вільям Ф. Ґанонґ 2002
Фізіологія нервових і м'язових клітин
Збудлива тканина: м'язова
Серцевий м'яз (міокард) - Механічні властивості
Скоротливість
Скоротлива відповідь міокарда починається відразу ж після початку деполяризації і триває майже в півтора раза довше, ніж потенціал дії (див. рис. 3-14). Роль Са2+ у координації збудження та скорочення є такою ж, як і в скелетних м’язах (див. вище). Проте, як зазначено вище, власне надходження всередину клітини Са2+ з позаклітинної рідини, що відбувається шляхом активування дигідропіридинових каналів у Т-системі, а не сама по собі деполяризація спричинює вивільнення йонів Са2+ з їхнього депо у саркоплазматичній сітці.
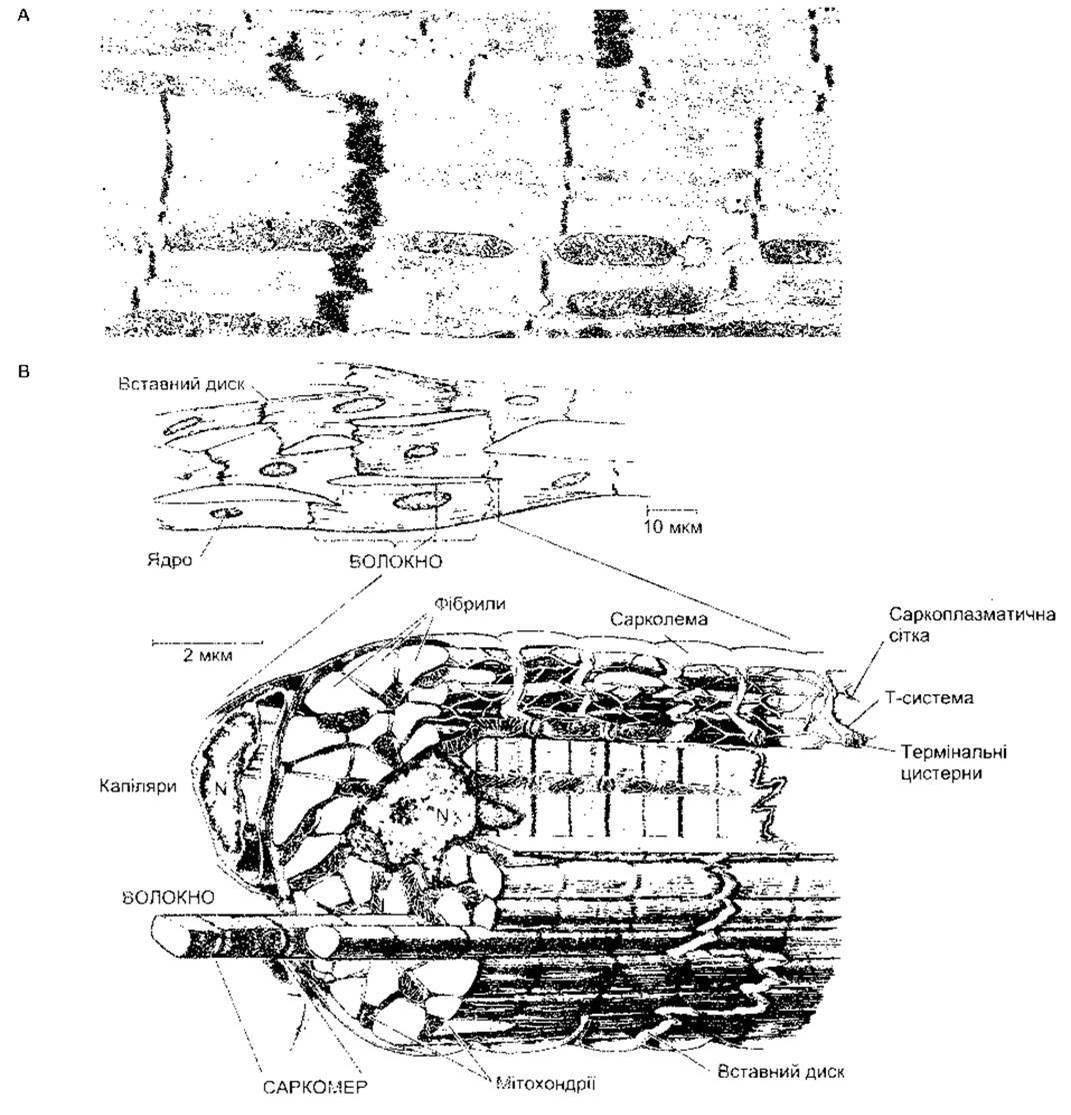
Рис. 3-13. А: електронна мікроскопія серцевого м’яза. Розпливчасті товсті лінії є вставними дисками (збільшення у 12 000 разів) (відтворено за дозволом з Bloom W, Fawcett DW: A Textbook of Histology, 10th ed. Saunders, 1975). В: схематичне зображення серцевого м’яза у разі світлової та електронної мікроскопії; N - ядро (відтворено за дозволом з Braunwald Е, Ross J, Sonnenblick EH: Mechanisms of contraction of the normal and failing heart. N Engl J Med 1967;277:794. Courtesy of Little, Brawn, Inc.)
Під час фаз 0-2 й упродовж близько половини фази 3 (доки під час реполяризації мембранний потенціал не досягне близько -50 мВ) серцевий м’яз не може бути знову
збудженим, тобто перебуває в періоді абсолютної рефрактерності (див. рис. 3-4). Він є порівняно рефрактерним до настання фази 4. Отже, тетанус у тому вигляді, в якому його спостерігають у скелетних м’язах, у серцевому м’язі неможливий. Зрозуміло, що перехід міокарда у стан тетанусу навіть на нетривалий час міг би мати смертельні наслідки, і з цього погляду неспроможність серцевого м’яза до тетанусу є засобом безпеки.
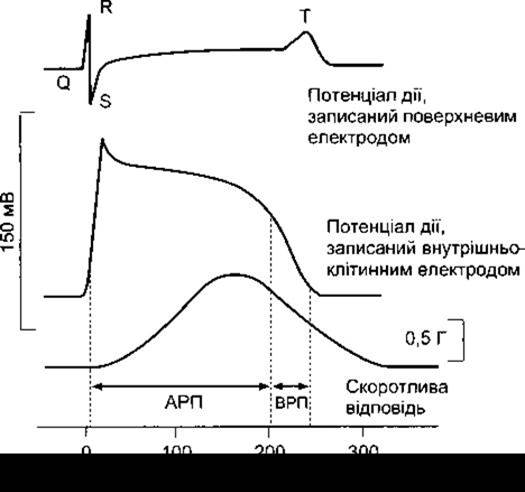
Рис. 3-14. Потенціали дії і скоротливі відповіді серцевого м’яза ссавців зображені у вигляді кривих потенціал-час; АРП - абсолютний рефракторний період; ВРП - відносний рефракторний період.
Ізоформи
Серцевий м’яз загалом повільний і має порівняно низьку активність АТФ-ази. Його робота залежить від окисного метаболізму, а отже, від надходження О2. Серцевий м’яз людини містить як а-, так і ß-ізоформи важких ланцюгів міозину (а-ВЛМ і ß-BЛM). Ланцюг ß-ВЛМ має нижчу активність міозинової АТФ-ази, ніж а-ВЛМ. Обидві ці ізоформи наявні в передсерді, де переважає а-ізоформа, тоді як у шлуночку виявлена лише ß-ізоформа. Вплив гормонів щитовидної залози на ізоформи ВЛМ розглянуто в Розділі 18. Тиреоїдні гормони також спричиняють зміни в ізоформах ВЛМ скелетних м’язів, проте в цьому випадку їхній ефект є складнішим, багатокомпонентним.
Співвідношення між довжиною м’язових волокон та напруженням, яке вони спричинюють
Співвідношення між початковою довжиною м’язового волокна і загальним напруженням, що виникає в серцевому м’язі, ідентичне до того, яке простежується в скелетному м’язі. Є певна довжина спокою, за якої напруження, що виникає під впливом зовнішнього стимулювання, максимальне. Початкова довжина волокон визначена діастолічним наповненням камер серця, а тиск, що виникає в шлуночку, пропорційний до його загального напруження (закон Старлінґа для серцевого м’яза, див. Розділ 29). Отже, сила скорочення (рис. 3-16) збільшується зі збільшенням діастолічного об’єму, доки не досягне максимального значення (висхідна частина кривої Старлінґа), а згодом починає зменшуватись (низхідна частина кривої Старлінґа) Однак, на відміну від скелетних м’язів, зменшення сили скорочення в разі значного розтягнення не зумовлене зменшенням кількості поперечних містків між актином та міозином тому, що навіть у випадку значного розширенню камер серця розтягнення міокарда до такого ступеня не зафіксовано. Низхідна частина кривої Старлінга відповідає початку руйнування серцевих волокон. Гомеостатичне значення закону Старлінга розглянуто в Розділі 29.
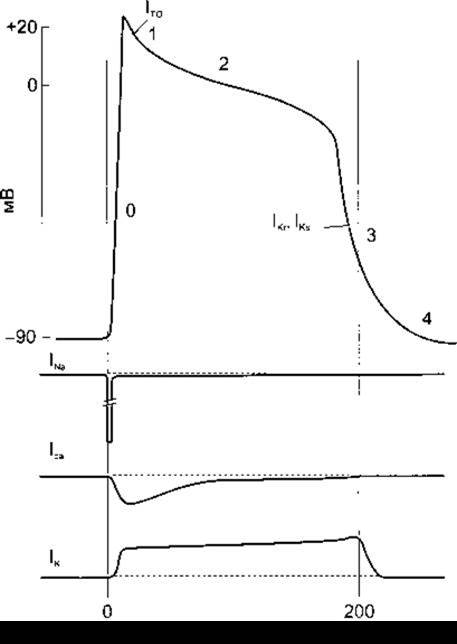
Рис. 3-15. Угорі: фази потенціалу дії серцевого волокна: 0 - деполяризація; 1 - початкова швидка реполяризація; 2 - фаза плато; 3 - пізня швидка реполяризація; 4 - базальний рівень потенціалу. Унизу: графіки, що відображають потоки Na+, К та Са2+ під час потенціалу дії. Внутрішній потік - крива донизу зовнішній потік - крива догори. Потоки К+ позначені безпосередньо на кривій потенціалу дії в ті моменти, коли вони відіграють вирішальну роль. Див. текст підручника.
Таблиця 3-5. Йонні канали в серцевому м’язі

Катехоламіни також здатні збільшувати силу скорочення серцевого м’яза (див. Розділи 13 і 20), не змінюючи його довжини. Таке посилення сили скорочення називають позитивним інотропним ефектом катехоламінів. Він опосередкований ß1-адренергічними рецепторами та цАМФ (див. Розділ 1). Серце теж містить позбавлені іннервації ß2 -адpeнергічні рецептори, які діють через цАМФ. Однак притаманний їм інотропний ефект значно слабший і здебільшого виявляється в міокарді передсердь; цАМФ активує білок кіназу А, що призводить до фосфорилювання потенціалозалежних Са2+-каналів, унаслідок чого ті тривалий час перебувають у відкритому стані, а також посилює процес активного транспортування Са2+ у саркоплазматичну сітку, прискорюючи розслаблення міокарда і, отже, вкорочуючи систолу. Цей механізм відіграє важливу роль у разі тахікардії, оскільки забезпечує за цих умов адекватне діастолічне наповнення камер серця (див. Розділ 29).
Глікозиди наперстянки (дигіталіс) посилюють силу скорочення серцевого м’яза, інгібуючи Na+-К+-АТФ-азу у клітинних мембранах м’язових волокон. Унаслідок цього: збільшується внутрішньоклітинний вміст Na+, і відповідно, зменшується градієнт концентрації Na+ з різних боків клітинної мембрани; зменшується надходження до клітини Na+ з позаклітинної рідини і, отже, втрата внутрішньоклітинного Са2+ через Na-Са2+-обмінну помпу, що міститься в клітинній мембрані м’язових волокон (див. Розділ 1); збільшується внутрішньоклітинна концентрація Са2+ і це, відповідно, посилює скорочення серцевого м’яза. Іншим ефектом глікозидів наперстянки є посилення повільного внутрішньоклітинного потоку Ca2+ всередину клітини під час потенціалу дії, що також збільшує концентрацію Са2+ всередині клітини.
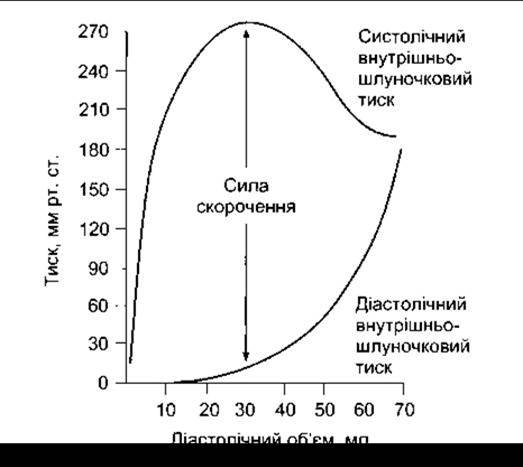
Рис. 3-16. Співвідношення між довжиною та напруженням серцевого м’яза собаки.
Гіпертрофія міокарда
Серцевий м’яз, як і м’язи скелетні, гіпертрофується, коли впродовж тривалого часу постійно працює за умов збільшеного навантаження, наприклад, у разі артеріальної гіпертензії. Гіпертрофія міокарда простежується й у випадку мутацій генів, які кодують різноманітні білки, що утворюють скоротливий апарат. До таких станів належить вроджений дефіцит дистрофіну, що виникає у разі м’язових дистрофій Дюшена або Бекера. Кінцевим наслідком є надмірна гіпертрофія, що призводить до розвитку серцевої недостатності (гіпертрофічна кардіоміопатія; див. Розділ 33). Більшість таких генетичних дефектів виявляються кардіоміопатією вже в ранньому віці, проте деякі з них простежуються у середньому або літньому віці. Нещодавно з’ясовано, що кальциневрин-NF-АТ-шлях, раніше описаний для Т-клітин імунної системи, є також одним з трансмітерів гіпертрофії серцевого м’яза. Детально функціювання імунної системи, яку блокує циклоспорин, описано в Розділі 27. Є докази того, що цей шлях відіграє важливу роль у гіпертрофії скелетних м’язів.