БІОТЕХНОЛОГІЯ - В. Г. Герасименко - 2006
Частина ІІ. Спеціальні біотехнології
Розділ 22. БІОТЕХНОЛОГІЇ УТИЛІЗАЦІЇ І БІОКОНВЕРСІЇ ВІДХОДІВ АГРОПРОМИСЛОВОГО КОМПЛЕКСУ
22.3.НЕТРАДИЦІЙНІ МЕТОДИ. БІОТЕХНОЛОГІЯ ОДЕРЖАННЯ БІОГАЗУ ШЛЯХОМ АНАЕРОБНОГО ЗБРОДЖУВАННЯ ВІДХОДІВ
22.3.2.Фактори, які впливають на біометаногенез і їх оптимізація
Кількість біогазу, яку можна отримати з різноманітних сільськогосподарських відходів, залежить від багатьох факторів: складу субстрату, умов проходження процесу анаеробного зброджування і особливо від тривалості знаходження субстрату в біореакторі та мікробіального складу в ньому.
У природних умовах швидкість метаногенезу під впливом асоціації анаеробних мікроорганізмів, які містяться в гнойовій
або іншій біомасі, доволі низька. Факторами, які впливають на біометаногенез є температура, склад і рН середовища, достатня концентрація поживних речовин, відсутність або низька концентрація токсичних речовин тощо.
Для інтенсифікації процесу метанового зброджування ці фактори потрібно оптимізувати.
1. Склад середовища
Сприятливим для життєдіяльності метаноутворюючих мікроорганізмів є середовище, в якому концентрація сухої речовини знаходиться на рівні 8-12 %. Ця кількість сухої речовини забезпечує таку в’язкість субстрату, що дає змогу вільно переміщатися твердим частинкам субстрату і мікробним клітинам. Більша концентрація твердих частин підвищує в’язкість субстрату, що погіршує інтенсивність перемішування і знижує вихід біогазу.
Натомість при низькій концентрації органічної речовини і високій вологості (понад 97 %) зменшується вихід біогазу і збільшуються витрати енергії на підігрів біомаси.
Оптимізувати цей фактор можна шляхом контролю вмісту сухої речовини (8-12 %) і довжини частинок біомаси - не більше 30 мм.
2. Вміст поживних елементів (С і N)
Біомаса метаноутворюючих мікроорганізмів має у своєму складі до 54 % вуглецю, 20 - кисню, 10 - водню, 12 - азоту, 2 - фосфору, 1 % сірки, а також деякі макро- і мікроелементи (K, Na, Ca, Mg, Co, Mo, Ni).
Тому для забезпечення росту мікроорганізмів і високої інтенсивності анаеробного зброджування біомаси необхідно, щоб у ній були в достатній кількості елементи, які сприяють росту бактерій. Найбільш важливими з них є вуглець та азот. Оптимальним співвідношенням цих елементів є 10-30 : 1 (С : N). Якщо це співвідношення завелике, тобто коли багато вуглецю, то в цьому випадку дефіцит азоту буде фактором, який обмежує процес бродіння. Якщо ж це співвідношення мале, тобто коли багато азоту, то утворюється велика кількість аміаку, що є токсичним для бактерій. Для підтримки співвідношення С : N в оптимальних межах у виробничих умовах гнойову біомасу змішують з відходами, які містять або велику кількість азоту (курячий послід), або велику кількість вуглецю (подрібнена солома).
Органічні підходи,» які використовуються для метанового зброджування, мають різні співвідношення С : N. що не завжди є оптимальними для процесу (табл. 22.1).
Таблиця 22. 1.
Співвідношення С: N у сільськогосподарських відходах
(за Баадером В., 1982)
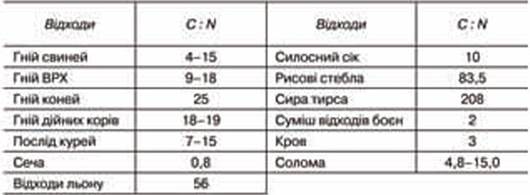
Для оптимізації співвідношення С: N змішують різні підходи і одержують більший вихід біогазу (таблиця 22.2).
Таблиця 22.2.
Збільшення виходу біогазу при змішуванні різних відходів
(за Баадером Μ В. та ін., 1982; Бієстром У та їн., 1987)
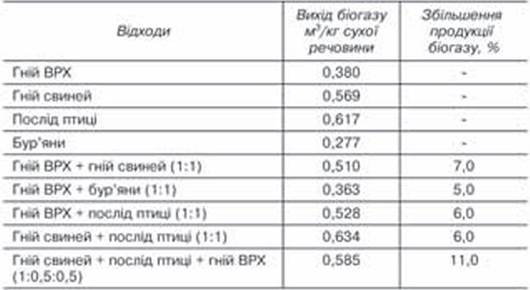
3. Реакція поживного середовища
Суттєвий вплив на швидкість метаногенезу має реакція поживного середовища. У процесі метанового бродіння можна виділити кислу і лужну фази. Кисла фаза або воднева - це перший і другий етапи біометаногенезу, а лужна - це третя метанова фаза. Протягом першої фази значення рН знижується внаслідок утворення низькомолекулярних летких жирних кислот. В подальшому відбувається розщеплення метаноутворюючими бактеріями летких кислот (3-й етап) та нейтралізація кислих продуктів до слаболужної реакції (7,2-7,6).
Встановлено, що найбільш інтенсивне утворення метану проходить при значеннях рН, близьких до нейтральних або слаболужних. Метаноутворюючі бактерії добре розвиваються і метаболізують субстрат у метан при рН 6-8, тоді як для кислоутворюючих необхідно рН 4,0-6,5. Створення умов, які були б задовільними для кислотоутворюючих бактерій, забезпечується підтримкою рН 6,8-7,4, що й вважаються оптимальними. З точки зору забезпечення необхідного діапазону рН бажані системи з належною буферною ємністю для підтримки стабільності процесу зброджування. Поживне середовище в реакторі має буферні властивості завдяки таким реакціям:
1) утворення гідроксилу амонію з аміаку і води NH3 + H2O → NH4OH, яка після нейтралізації кислих продуктів першої фази зумовлює характерне для метанового бродіння слаболужне середовище (рН 7,2-7,6). Ця природна буферна система виникає при високій концентрації в субстраті азотомістких поживних речовин і може використовуватися за умови, що концентрація вільного аміаку не досягає токсичних значень;
2) реакція утворення вуглекислого і двовуглекислого амонію з аміаку і вуглекислоти.
При підвищенні активності кислотоутворюючих мікроорганізмів збільшується кількість кислот до такого рівня, коли буферна ємність втрачається на нейтралізацію кислих продуктів і рН зменшується нижче допустимих величин, у зв’язку з чим гальмується утворення метану.
За відсутності амонійного буферу підлужування може здійснюватися гідроксидами, карбонатами або гідрокарбонатами. В цьому випадку утворюється буферна система карбонат/гідро- карбонат.
Висока швидкість утворення біогазу досягається при концентрації у середовищі летких кислот у межах 50-500 мг/л. При збільшенні їх концентрації вище наведеного рівня й одночасному зниженні рН можна підлужувати середовище хімічними речовинами (наприклад вапном). Кількість лугу може сягати до 6000 мг/л. Бажано, щоб співвідношення ЛЖК до лугу, наприклад до СаСО3, було 1 : 6.
Необхідно враховувати, що в консорціумі мікроорганізмів, які беруть участь в утворенні метану, кислотоутворюючі бактерії краще адаптовані до зміни умов і мають вищу продуктивність порівняно з метановими бактеріями.
Метаногенні бактерії - найбільш примхлива з погляду культивування група серед симбіонтів, які беруть участь в анаеробному бродінні. Для росту вони потребують широкого спектра поживних речовин, включаючи вуглець, фосфор, азот, кальцій, сірку, магній, калій, амінокислоти, вітаміни та мікроелементи.
4. Концентрація в середовищі токсичних речовин
Швидкість розмноження метаноутворюючих мікроорганізмів залежить від концентрації у середовищі іонів важких металів, амонію, натрію, калію, кальцію, магнію, нітратів, сульфідів, а також різних ксенобіотиків, які при великих концентраціях можуть бути токсичними для мікроорганізмів.
Джерелом токсичних речовин можуть бути відходи тварин, які одержували великі дози антибіотиків або сполук металів (наприклад, Cu, Zn, Mn, Fe), що використовуються у тваринництві для балансування раціонів тварин за цими факторами живлення.
Для подолання токсичності можна використати такі прийоми: видалення токсичної рідкої фази, розчинення біомаси (водою, чистою біомасою) для зниження концентрації токсичних речовин, додавання антагоніста виявленого токсина, осадження токсичних речовин, адсорбція токсинів, наприклад, активованим вугіллям тощо, зв’язування токсинів у хелатний комплекс. Це дає можливість знизити концентрацію токсичних речовин до рівня, який не буде перешкоджати бродінню. В іншому випадку біомаса не використовується для одержання біогазу.
При анаеробному зброджуванні курячого посліду потенційну токсичність, яка виникає внаслідок підвищеного вмісту аміаку, усувають шляхом додавання біомаси з високим умістом вуглецю (частіше подрібненої соломи) або розчиняють водою. В іншому випадку висока концентрація вільного аміаку на початковій стадії анаеробної ферментації може призвести до загибелі метаноутворюючих мікроорганізмів. Рівень токсичності іонів аміаку становить 1500-2000 мг/л; К, Na, Ca - 3000-6000 мг/л; ціаніду - 0,5—1,0 мг/л.
5. Температурний режим
Температурний режим є одним із суттєвих параметрів, які впливають на метаболічну активність і швидкість розмноження метаноутворюючих мікроорганізмів та вихід біогазу.
У природі зустрічаються різні метаноутворюючі мікроорганізми, які відрізняються між собою за температурним оптимумом - психрофіли (0-20 оС), мезофіли (20-40 оС) і термофіли (40-60 оС), які виживають навіть при температурі 97 оС. Тому і метан у природі утворюється при широкому діапазоні температур - від 0 до 97оС. За даними Дубровіна В. та ін. (2004), метанова ферментація починається при температурі 6 оС. При нижчій температурі виділення метану припиняється.
Але оптимальними температурами, за яких життєдіяльність мікроорганізмів відбувається найбільш активно, є: для психрофітів - 6-20 оС, мезофілів - 32-33 оС, а для термофілів 52-54 оС.
Розрізняють три температурних режими одержання біогазу:
1) психрофільний - від 0 до 20 оС;
2) мезофільний - від 20 до 40 оС;
3) термофільний - від 40 до 60 оС.
Кожен температурний режим сприяє росту і підвищенню метаболічної активності певної групи метаногенів. Краще анаеробне зброджування біомаси проходить при температурі 30-40 оС і 50-60 оС (при розвитку мезофільної і термофільної мікрофлори). Термофільні бактерії продуктивніші, ніж мезофільні.
При утилізації біомаси в термофільних умовах швидкість утворення біогазу у 2,5-3 рази вища, ніж при мезофільному режимі.
В установках, що працюють у мезофільному режимі, добовий вихід біогазу складає 1,0 м3, у термофільному режимі - 2,0 м3 біогазу з 1 м3 робочого об’єму метантенка.
Термофільні бактерії за час зброджування протягом 12-14 днів мінералізують стільки ж органічних речовин, скільки мезофільні бактерії за 21-36 днів (Дубровін В. та ін., 2004). Завдяки цьому при однаковій кількості біомаси для зброджування місткість реактора буде меншою при термофільному режимі роботи БГУ порівняно з мезофільним. Але при мезофільному режимі досягається економія енергії, необхідної для підігрівання зброджуваної біомаси, і мікробна популяція, яка культивується при цьому режимі, менш чутлива до складу поживного середовища. Проте є дані, що в біогазі, добутому за термофільних умов, зменшується частка метану.
Тривалість процесу ферментації біомаси при одержанні біогазу залежно від температурного режиму і конструкційних особливостей БГУ складає від 5 до 30-40 діб і більше. За мезофільних температурних умов процес зброджування найчастіше триває 24-28 діб, а при температурі в біореакторі 10 оС тривалість зброджування - до 4 місяців і більше.
Час зброджування також залежить від хімічного складу біомаси. Найтривалішим він буде при підвищеному вмісті целюлози та геміцелюлози, коротшим - у разі наявності білків і жирів, а найкоротшим - для цукрів.
6. Хімічний склад біомаси
Максимальний вихід біогазу на стадії найбільш інтенсивного метаногенезу залежить від хімічного складу біомаси, яка зброджується, що, в свою чергу, визначається видовим складом рослинних рештків та видом тварин і відповідно раціоном, який вони отримують (табл. 22.3 та 22.4).
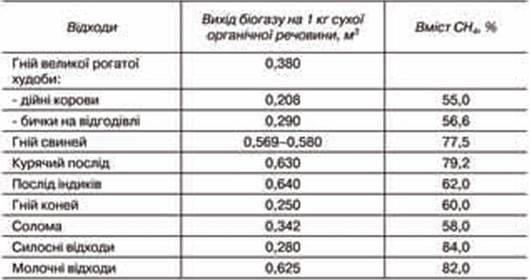
Так, з 1 кг сухої речовини гнойової біомаси великої рогатої худоби, внесеної в реактор біогазової установки, теоретично можна одержати в середньому 0,4-0,6 м3 біогазу. Враховуючи, що лише 40-60 % сухої речовини гною в процесі метаногенезу трансформується в біогаз, реальний вихід біогазу з 1 кг сухої речовини гною великої рогатої худоби становить у середньому 0,2-0,5 м3; з еквівалентної маси свинячого гною - 0,3-0,7 м3, а з біомаси курячого посліду ще більше (табл. 22.5).
При ферментації екскрементів від однієї тварини можна отримати біогазу в середньому за добу: великої рогатої худоби (жива маса 500-600 кг) - 1,5 м3; свині (жива маса 80-100 кг) - 0,2 м3; курки або кроля - 0,015 м3.
Таблиця 22. 3.
Хімічний склад відходів рослинництва, % на суху речовину
(за Баадером В., 1982)
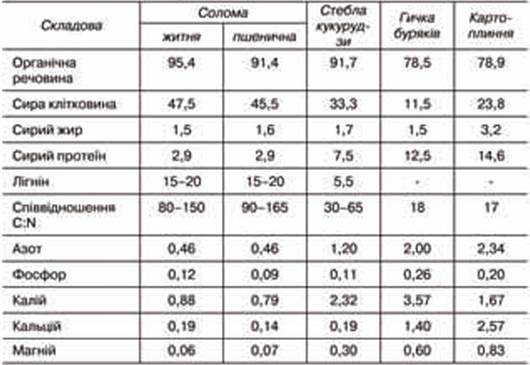
Таблиця 22.4.
Хічічний склад гною сільськогосподарських тварин і птиці,
% на суху речовину (за Бaадером В., 1982)
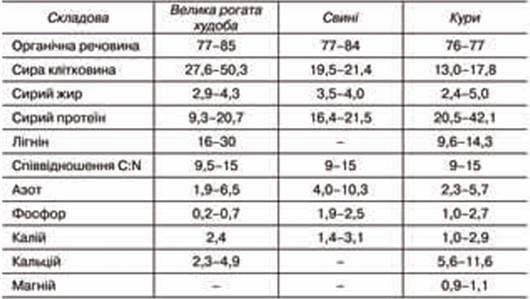
Таблиця 22.5.
Вихід біоіазу (метану) при анаеробному зброджуванні сільськогосподарських відходів
(за Лубравським В.С., Вієстур У.Е., 1988)
Середня кількість біоту, яку можна отримати з 1 м3 гною тварин оцінюється у 20- 25 м3 хоча з техніко-економічної точки зору рентабельною кількістю вважаються 40 -35 м3. Таку кількість біогазу можна отримати шляхом поєднання різних відходів тваринництва з іншою сировиною, яка відрізняється високим умістом сухої органічної маси, а саме з відходами підприємств харчової промисловості тощо.
Крім кількості сухої речовини, суттєвим параметром, який впливає на вихід біогазу, с вміст та склад органічної речовини, особливо кількість жирів, білків, вуглеводів.
Вуглеводи, як правило, знаходяться у формі полі цукрів, тому погребують більш тривалої ферментації. Помітно знижується утворення біогазу в присутності лігніну, тому що у процесі метановою бродіннм той практично не розкладається.
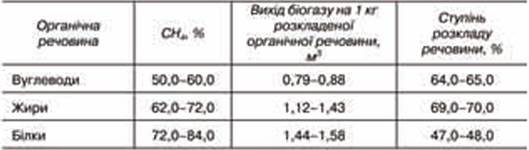
Найбільший вихід біогазу на 1 кг розщепленої органічної речовини дають білки (1,4 -1,6 м3), потім жири (1,1 -1,4 м3 ) і найменше вуглеводи 0,8- 0,9 м3 (табл. 22.6). Але. Враховуючи, що ступінь розкладання білків нижчий, ніж жирів, то реальний вихід біогазу з 1 кг білків становить 0,6 - 0,7 м3.
Таблиця 22.6.
Вихід біогазу і вміст СН4 при метановому бродінні жирів, білків, вуглеводів
(на Бієстру У. Е та ін.. 1987)
Співвідношення кількості біогазу, який можна виділіти з органічної речовини гнойової біомаси дійних корів (Д). відгодівельних бичків (Б), свиней (С) і курей (К) в процесі метанового бродіння при температурі 33 С, орієнтовно може бути таким: Д: Б: С: К ї 5:7:8:10.
Практично з розрахунку на 1 кг сухої органічної речовини максимальний вихід біогазу в середньому становить; 0,35 м3 - з гною ВРХ: 0,45 м3 з гною молочної худоби; 0,5 м3 - з гною свиней і 0,7 м3 — з пташиного посліду.
Від хімічного складу біомаси залежить і якість біогазу. При зброджуванні біомаси з великим умістом клітковини в біогазі містяться однакові кількості метану і діоксиду вуглецю. Збільшення у складі біомаси азотомістких речовин і жиру супроводжується підвищенням у біогазі концентрації метану ізменшенням кількості діоксиду вуглецю (табл. 22.6).
Заданими В.А. Бикова та ін. (1987). при зброджуванні 1 г жироподібних речовин в середньому утворюється 1200 мл біогазу, до складу якою входить метану 68 % і діоксиду вуглецю 32 %, а з 1г вуглеводистих речовин відповідно 800 мл біогазу з умістом СН4, - 50 % і СО2 - 50 %.
При використанні виходів рослинництва (соломи, гички буряків і картоплі, відходів переробки льону тощо) з високим умістом вуглецю для забезпечення високої швидкості біометаногенезу і виходу біогазу необхідно оптимізувати співвідношення вуглецю до азоту (С : N). В умовах виробництва з цією метою до біомаси, що утилізується, додають відходи з високим умістом азоту (гній курей або свиней).
В деяких країнах використовується технологія непрямої утилізації гною. Гній піддається механічній обробці, а потім подається не в біогазову установку, а використовується як субстрат для вирощування гідробіонтів, що спеціально селекціоновані для цих умов. Вони вирізняються високою швидкістю фотосинтезу й ефективним використанням поживних речовин гнойової біомаси. В Індії позитивний результат досягли при змішуванні біомаси водяного гіацинту з гноєм у співвідношенні 2 : 3. Вихід біогазу в цьому випадку збільшився майже на 50 %, а в шламі підвищився вміст азоту, фосфору, калію, що покращило якість шламу як органічного добрива.
Технологія непрямої утилізації гною має суттєві переваги над технологією утилізації гнойової біомаси шляхом прямої анаеробної ферментації з одержанням біогазу. Технологія непрямої утилізації ефективніша за рахунок акумулювання сонячної енергії, яка накопичується у вигляді енергії хімічних зв’язків органічних сполук.
Використання біотехнології виробництва біомаси гідробіонтів - є перспективним для одержання біогазу. В 1980 р. у Московському університеті була створена експериментальна бісолярна установка з виробництва біомаси мікроводоростей з подальшою утилізацією її у метан. Конструкція системи забезпечує рециркуляцію усіх біогенних елементів (рис. 22.2). Фотосинтетичний блок бісолярної установки площею 30 м2 забезпечує одержання біомаси хлорели, яка після концентрування і гомогенізації з метою руйнування клітинних структур подається у бродильну камеру, де проходить анаеробна ферментація біомаси й утворення біогазу, який складається з метану (80 %), діоксиду вуглецю (16 %) і водню (2 %). На частку інших домішок припадає близько 2 %. Конструкція бісолярної установки передбачає введення додаткових кількостей СО2 повітря у фотосинтетичний блок.
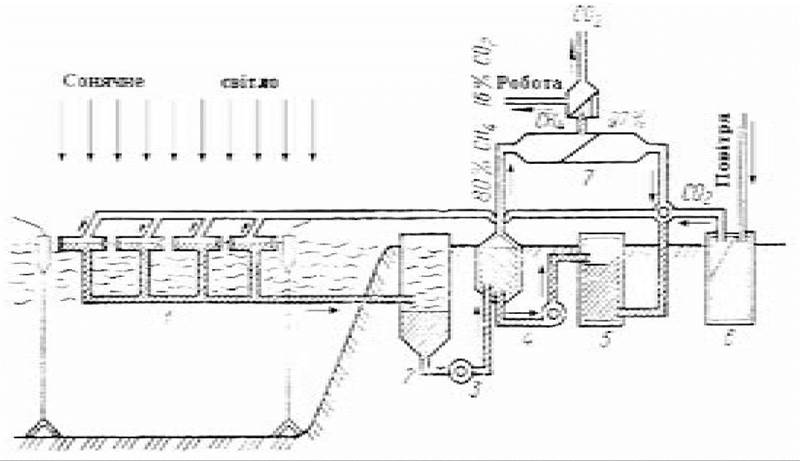
Рис. 22.2. Бісолярна установка (за Алексєєвим В.В., Ляміним М.Я., 1985):
1 — фотосинтетичний блок; 2 — відстійник; 3 — декомпресор; 4 — бродильна камера (метантенк); 5 — регенератор;
6 — концентратор СО2; 7 — сепаратор.