БІОТЕХНОЛОГІЯ - В. Г. Герасименко - 2006
Частина І. Загальна біотехнологія
РОЗДІЛ 5. ОСНОВИ ГЕНЕТИЧНОЇ ІНЖЕНЕРІЇ
5.1.БІОТЕХНОЛОГІЯ КОНСТРУЮВАННЯ РЕКОМБІНАНТНИХ ДНК
5.1.5.Експресія еукаріотичних генів у клітинах прокаріот
Наступна проблема, яка виникає у дослідників при вирішенні фундаментальних питань генетичної інженерії, — домогтися експресії еукаріотичного гена в чужорідному оточенні прокаріотичної клітини організму, найчастіше Е.соlі. Для цього одержаний і вже клонований ген, що підлягає експресії, ферментативним впливом елімінують з вектора, у складі якого він був клонований, і піддають певній модифікації. Такі складні додаткові маніпуляції необхідні в зв’язку з тим, що сигнали для транскрипції і трансляції в прокаріотичних і еукаріотичних організмів розрізняються. Крім того, ні кДНК, ні синтезований хімічним шляхом ген не містять у своєму складі промотору й інших сигналів, потрібних для експресії генів у бактеріях.
Так, до складу генів ссавців входять такі нуклеотидні послідовності, що виконують регуляторну функцію тільки в «рідних стінах», тобто у складі еукаріотичної клітини. Вихід з цього складного становища полягає в тому, що штучний еукаріотичний ген вбудовують у структурний ген вектора прокаріотичної клітини в місці, де прокаріотичні сигнали регуляції сприятимуть експресії еукаріотичного гена. Якщо еукаріотичний ген містить власні регуляторні нуклеотидні послідовності, їх заміняють на регуляторні послідовності із бактеріальних клітин. Потім рекомбінантну ДНК з модифікованим еукаріотичним геном трансформують у придатні чужорідні прокаріотичні клітини, найчастіше Е.соlі.
При експресії чужорідних генів синтезовані ними білкові продукти часто сприймаються клітинним оточенням як невласні речовини і тому розщеплюються ферментами клітини-хазяїна. Для подолання цієї перешкоди клітину-хазяїна перебудовують за допомогою добору мутантних форм, з яких еліміновані відповідні протеази. У зв’язку з цим нові для клітини речовини сприймаються її внутрішньоклітинним умістом як власні продукти.
Наступне завдання полягає в тім, щоб інтенсифікувати процес експресії клонованого гена. При цьому слід зазначити, що еволюція мікроорганізмів проходила в напрямку удосконалення механізмів, що забезпечують їхнє виживання і відтворення. За природного добору мікроорганізми досить добре пристосувалися до середовища існування і до конкуренції з іншими видами. Що стосується добору мікробних клітин за їх здатністю до виробництва потрібних для людини (та ще й у величезних кількостях) речовин, то в природних умовах еволюція мікроорганізмів у такому напрямку, зрозуміло, не відбувалася. Тому перед генетичною інженерією поряд з іншими порушено й успішно вирішується питання конструювання таких штамів мікроорганізмів, які мають здатність виробляти хоча й звичайний для них продукт, але в зовсім незвичних кількостях. Крім того, як уже було відзначено, конструювання рекомбінантних молекул ДНК призвело до синтезу таких речовин, що не були раніше метаболітами цієї клітини (рис. 5.5).
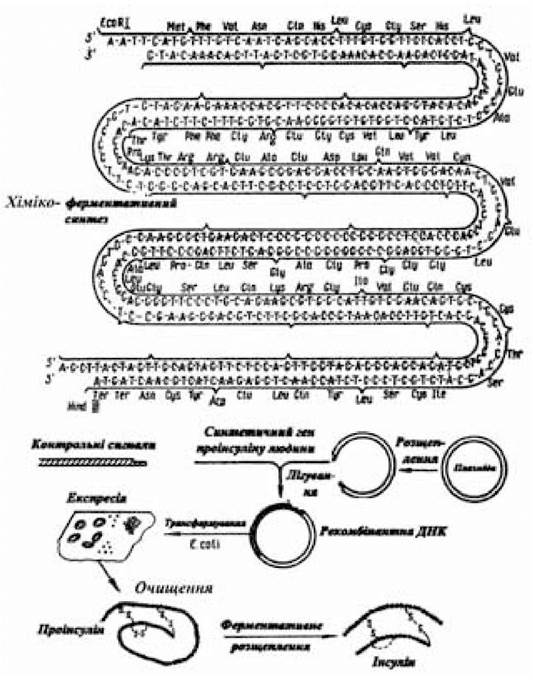
Рис. 5.5. Схема мікробного синтезу інсуліну людини
(за Овчінніковим Ю.А., 1986)
Використання методів і прийомів молекулярної біології та генетичної інженерії, за допомогою яких доведена принципова можливість біосинтезу мікробними чи дріжджовими клітинами дуже потрібних речовин з погляду забезпечення потреб людини не можна вважати біотехнологією. Наріжним каменем біотехнології є виробництво біологічно активних речовин для задоволення потреб охорони здоров’я, а також галузей агропрому в таких обсягах і за такою собівартістю, яка дозволила б виготовленій біотехнологічній продукції бути конкурентоспроможною. Так, на початкових етапах розробки біотехнології мікробного виробництва інсуліну бактеріальні клони, трансформовані інсуліновою кДНК, синтезували попередник інсуліну в незначній кількості — близько 100 копій білка на одну мікробну клітину. Однак уже тоді вважали, що комерційний стимул до виробництва інсуліну людини, а також гормону росту й інтерферону в стані здолати труднощі, що виникають на шляху організації виробництва цієї й іншої біотехнологічної продукції в необхідному обсязі.
Експресія структурних генів, як зазначено раніше, що включає етап транскрипції (синтез іРНК, комплементарній відповідній матриці ДНК) і трансляції (побудова білкової молекули на іРНК-матриці в рибосомах), контролюється послідовностями основ, приєднаних до ділянки структурного гена. Це коротка промоторна ділянка, що знаходиться від місця ініціації на відстані приблизно 10 і 35 пар основ, має підвищену спорідненість з РНК-полімеразою і сприяє переміщенню ферменту уздовж ДНК-матриці, ініціююючи транскрипцію ДНК у місці, що прилягає до кодуючої послідовності структурного гена. На кінці структурного гена знаходиться ділянка термінації, у якій РНК-полімераза припиняє процес транскрипції.
У деяких генах біля промотору розташовуються додаткові нуклеотидні послідовності, хімічно споріднені з білком, взаємодія яких зі згаданими ділянками ДНК зумовлює їхні регуляторні функції. Так, між промотором і структурним геном знаходиться операторна ділянка. З нуклеотидами, що формують операторну ділянку, за наявності в клітинному середовищі певних метаболітів, взаємодіє білкова речовина, яка кодується нуклеотидною послідовністю ДНК. Ця білкова речовина називається респресором, а ділянка ДНК, що кодує цей білок, — геном-регулятором.
Регуляція експресії на стадії трансляції здійснюється за допомогою нуклеотидних послідовностей, що входять до складу іРНК. Так, у іРНК є спеціальна ділянка, яка представлена відповідною нуклеотидною послідовністю і до якої приєднується рибосома таким чином, що процес трансляції завжди починається з першого кодону (AUG-кодон, чи стартова ділянка), а закінчується стоп-кодоном (UAА-нуклеотидна послідовність), що зумовлює відокремлення синтезованого поліпептидного ланцюга.
Підвищення ефективності експресії генів і збільшення кількості продуктів, синтез яких контролюється цими генами, досягається за допомогою методів генетичного програмування. Навіть незначні зміни послідовності нуклеотидів у промоторі здатні збільшити хімічну спорідненість РНК-полімерази до цієї ділянки ДНК і підвищити швидкість транскрипції. Істотне збільшення швидкості транскрипції може бути досягнуто і за рахунок змін послідовності нуклеотидів в ділянці оператора й у гені-регуляторі, внаслідок чого білок-репресор не зможе вступити у взаємодію з операторною ділянкою ДНК і загальмувати синтез іРНК. Варто також враховувати залежність активності синтезованого ферменту від амінокислотної послідовності його поліпептидного ланцюга.
У зв’язку з цим фермент, що характеризується низькою хімічною спорідненістю до свого субстрату, набуває здатності вступати у взаємодію майже з кожною молекулою перетворюваної ним речовини. Можлива також втрата хімічної спорідненості до одних і придбання спорідненості до інших субстратів, що мають іншу будову. У цьому випадку причиною зміни послідовності амінокислот у білку-ферменті є відповідні зміни послідовності нуклеотидів в кодуючій ділянці структурного гена, внаслідок заміни, втрати чи вставки пари азотистих основ чи невеликих ділянок ДНК. Передбачається, що подібні зміни є наслідком помилок, які виникають при реплікації і передаються спадково з покоління в покоління.
Частота таких помилок (спонтанних мутацій) украй низька. Імовірність одноразової зміни однієї пари основ може відбутися за 10 мільйонів актів реплікації. Фізичні фактори (наприклад, ультрафіолетове випромінювання, іонізуюча радіація й ін.) та деякі хімічні речовини можуть підвищити частоту мутації не менш ніж у 1000 разів. Однак мутагенні фактори впливають на гени і викликають мутації за принципом випадковості. Технологія рекомбінантних ДНК підвищує точність традиційних підходів; вона дозволяє замінити непередбачуваність звичайного мутагенезу мутацією певних ділянок у визначених генах.
Перебудовуються гени за рахунок зміни нуклеотидних послідовностей ДНК за допомогою локалізованого мутагенезу; один з рестрикційних фрагментів клонованого гена замінюється фрагментом із внесеними в нього змінами. Крім цього, розроблена методика заміни нуклеотидної послідовності, що міститься у гені, на нову чи просто додавання нових ділянок ДНК, які за своїм походженням є синтезованими поза організмом фрагментами ДНК.
Розроблено прийоми маніпулювання не тільки оліго- чи полінуклеотидними послідовностями, але й окремими нуклеотидами, що приводить до мінімальних змін гена (точкові мутації). Змінені тим чи іншим шляхом гени вводяться потім у природне для них біологічне середовище.
У зв’язку з модифікацією генів змінюються кількісні і якісні показники експресії. Наприклад, отримані штами Brevibacterium flavum і Sorynebacterium glutamicum перетворюють на лізин понад 33 % цукру, у результаті чого концентрація цієї критичної амінокислоти в живильному середовищі досягає 7,5 %; промислові штами Реnicillium chrysogenumі Streptomyces aureofaciens синтезують понад 20 г пеніциліну і тетрацикліну з розрахунку на 1 л живильного середовища (продуктивність диких штамів знаходиться на рівні декількох міліграмів); більш ніж у 500 разів вдалося збільшити за допомогою рекомбінантних молекул ефективність функціонування Е.соlі у процесі біосинтезу ДНК-лігази.
Модифікація керуючих біологічною системою генів супроводжується зміною взаємозв’язків, що раніше існували у цій системі. Так, білок, що транспортується у визначений компартмент клітини, після відповідної модифікації гена, що кодує біосинтез цього білка, може змінити цей відсік на інший; модифікація нуклеотидної послідовності гена може призвести до того, що сигнали, які регулюють його експресію до перебудови, замінюються на стимули, що мають іншу хімічну будову.
Мікроорганізми, що містять рекомбінантні молекули ДНК із модифікованими тим чи іншим шляхом генами, уже використовуються чи будуть використовуватися у недалекому майбутньому для великомасштабного виробництва цінних речовин. Це інтерферон (універсальний противірусний засіб і, можливо, засіб для боротьби зі злоякісним ростом); ренін (використовується у виробництві сиру з молока); фактор некрозу пухлин (у терапевтичних цілях застосовується при ракових захворюваннях);
целюлаза (фермент призначається для гідролізу рослинної целюлози й одержання в-глюкози); пептидні антигени вірусів, що є складовими компонентами в конструюванні нових безпечних вакцин; інсулін (при захворюванні на цукровий діабет); урокіназа і плазміноген (використовуються для розчинення тромбів); соматотропін (застосовується з лікувальною метою при карликовості, опіках, кісткових переломах); соматостатин (гальмує секрецію соматотропіну, інсуліну і глюкагону); ДНК-лігаза (широко використовується в генетичній інженерії).
Розроблені молекулярними біологами методи і прийоми конструювання рекомбінантних молекул ДНК, клонування і модифікації генів, з одного боку, є підґрунтям, на якому створюється будинок біотехнології; з іншого — за допомогою цих методів і прийомів вирішуються фундаментальні питання біології, що надалі будуть використані в прикладних цілях. Так, за допомогою методу клонування вивчаються такі фундаментальні питання біології, як функціонування гена і регуляція цієї функції, проводиться визначення послідовності нуклеотидів; завдяки клонуванню генів можна одержати в достатніх кількостях і в чистому вигляді основні макромолекули біологічних систем, що дозволяє заощаджувати матеріальні ресурси, а також сили і час дослідника.
Метод клонування генів дозволяє одержати в необмеженій кількості ДНК для електронно-мікроскопічних досліджень, вивчення специфічних ділянок ДНК, які обумовлюють рухливість генів, реплікацію і транскрипцію ДНК, порівняно швидко провести картування складних хромосом і поділ їх на окремі фрагменти, що піддаються змінам.
Створено широкі можливості для вивчення структури РНК, процесів її дозрівання (вирізання інтронів з первинного транскрипта і наступне ферментативне зшивання кінців за допомогою лігази). Доцільно ще раз наголосити, що в прокаріотичних клітинах процесинг (дозрівання) не розповсюджений; у клітинах еукаріот усі види РНК містять інтрони, які під час дозрівання рибонуклеїнових кислот вирізаються, а утворені при цьому кінці зрощуються (сплайсинг).
Розкриття біохімічних механізмів процесингу лежить в основі розуміння функціонування генів. За допомогою клонування стали можливими широкомасштабні дослідження з конкретизації функцій різноманітних білків. Клонування дозволяє модифікувати гени і кодовані ними білки, що призводить до зміни функцій останніх, а отже, і зв’язків між компонентами біологічної системи.
Метод клонування генів вносить істотний вклад в історію еволюційного розвитку. Шляхом клонування генів і наступної розшифровки їх нуклеотидних послідовностей удається відтворити зміни, що відбулися в клітинах організмів, які нині живуть. Аналіз нуклеотидних послідовностей клонованих фрагментів ДНК за допомогою розроблених досить складних комп’ютерних програм дозволяє з великою точністю установити ступінь еволюційного споріднення.
Така властивість нуклеотидних послідовностей, як консервативність (сталість у часі), з успіхом використовується молекулярними біологами для вирішення прикладних задач. Так, нуклеотидні послідовності, характерні для вірусів (онкогенів), які викликають ракову хворобу, виявлені в ДНК дріжджів. Це відкриття свідчить про роль цих генів у забезпеченні життєдіяльності одноклітинних організмів, яку вони відігравали задовго до появи на Землі багатоклітинних форм. З іншого боку, можливість тонкого експериментування з дріжджовими клітинами (поки недосяжна для багатоклітинних організмів) з наступною екстраполяцією отриманих даних на клітини ссавців є значним внеском у розвиток знань про молекулярні механізми раку.
Клонування варіантів генів, що зумовлюють схильність їхніх носіїв до серповидно-клітинної анемії, атеросклерозу, раку, гемофілії і багатьох інших захворювань обміну, відкриває можливість точної діагностики генетичної схильності до цих патологічних процесів і вишукування способів відновлення дефектних генів у їхніх носіїв і нащадків. Уведення недефектних варіантів клонованих генів у клітини, наприклад кісткового мозку чи шкіри, дозволяє послабити прояв генетичних захворювань чи усунути їх зовсім. Розробка способу введення недефектних клонованих генів у статеві клітини дозволить уникнути можливості передачі генетичних порушень нащадкам. Вже отримані еукаріотичні гени, біологічна активність яких реалізується не
тільки при введенні їх у бактерії, але й в еукаріотичні клітини. Клонований ген β-глобіну кролика за допомогою вірусу SV40, використаного як вектор, був перенесений у клітини нирок мавпи, де в результаті його експресії вдалося одержати значну кількість β-глобіну кролика. Цей приклад підтверджує можливість усунення генетичних дефектів, а також показує, наскільки такий підхід перспективний для розшифровки регуляторних механізмів експресії генів еукаріотичних організмів.