ОБЩАЯ И ПИЩЕВАЯ МИКРОБИОЛОГИЯ ЧАСТЬ II - Л. В. Красникова - 2016
ТЕМА 3. МИКРОБИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ КОЛБАСНЫХ ИЗДЕЛИЙ
Колбасные изделия являются достаточно благоприятной средой для развития микроорганизмов различных групп, вызывающих их порчу. К ним относятся молочнокислые термофильные бактерии, протеолитические и липолитические бактерии, мицелиальные грибы и др.
Микробиологический контроль колбасных изделий проводят:
✵ периодически для проверки соблюдения санитарного и технологического режимов производства, но не реже одного раза в 10 дней;
✵ по требованию контролирующих организаций;
✵ в случаях установления использования подозрительного по доброкачественности сырья и вспомогательных материалов;
✵ нарушения температурного или санитарно-гигиенического режима производства.
Периодические исследования по предупредительному контролю соблюдения санитарного и технологического режимов колбасного производства проводят в следующие сроки:
✵ для колбас фаршированных, ливерных, кровяных высшего, I и II сортов, зельцев высшего, I и II сортов - не реже одного раза в 15 дней;
✵ для колбас вареных высшего, I и II сортов, мясных хлебов, сосисок, сарделек - не реже одного раза в 15 дней;
✵ для колбас ливерных и кровяных III сорта, зельцев III сорта, студней и паштетов - не реже одного раза в 5 дней;
✵ для колбас полукопченых, варено-копченых и сырокопченых - не реже одного раза в месяц;
✵ для продуктов из свинины, говядины, баранины, мяса птицы и других видов убойных животных: вареных, запеченных, жареных - не реже одного раза в 15 дней; копчено-вареных, копчено-запеченных, сырокопченых - не реже одного раза в месяц.
Стойкость колбасных изделий при хранении неодинакова и зависит от ряда факторов: содержания поваренной соли, величины рН, степени обезвоживания, консистенции, химического состава фарша и коптильных компонентов.
Наиболее устойчивы при хранении сырокопченые и сыровяленые колбасные изделия, так как они имеют твердую консистенцию и наибольшую концентрацию поваренной соли, активность воды в них минимальна.
При неправильном хранении остаточная микрофлора колбасных изделий быстро размножается. Многочисленные микробы вызывают порчу колбасных изделий: гниение, прогорклость, кислое брожение, плесневение.
Бактериологическое исследование колбасных изделий включает в себя определение общего количества микробов в 1 г продукта (КМАФАнМ) (в сырокопченых колбасах не определяют), выявление бактерий родов Escherichia, Salmonella, Proteus, а также коагулазоположительных стафилококков и сульфитредуцирующих анаэробов.
3.1. Отбор и подготовка проб
Пробы для микробиологического исследования отбирают согласно нормативной документации от каждой партии (одного вида, сорта, наименования, выработанных в одной смене и др.).
Пробы хранят при температуре от 4 до 6 °С не более 4 ч с момента отбора.
Для микробиологического исследования составляют объединенную пробу массой 50 г. Объединенную пробу готовят следующим образом: отобранные для исследования изделия помещают в эмалированный тазик, который протирают тампоном, смоченным спиртом, и обжигают над пламенем. Батоны разрезают стерильным скальпелем на две половины, не рассекая оболочки противоположной стороны батона. Пробу отбирают из нескольких участков центральной части и из-под оболочки обеих половин батона.
Из объединенной пробы каждого образца берут в стерильную посуду навеску массой 20±0,1 г, которую помещают в стерильный стакан гомогенизатора, добавляют 80 см3стерильного физиологического раствора и гомогенизируют. При отсутствии гомогенизатора для приготовления взвеси используют стерильную ступку, растирая
20 г продукта с 2-3 г стерильного песка, постепенно приливая 80 см3 стерильного физиологического раствора.
Взвесь отстаивают при комнатной температуре в течение 15 мин. В 1 см3 приготовленной взвеси содержится 0,2 г исследуемого продукта.
3.2. Определение КМАФАнМ
Навеску исследуемого продукта (масса 10 г) помещают в стерильную фарфоровую ступку и тщательно растирают стерильным пестиком, постепенно приливая 90 см3 стерильного физиологического раствора с учетом разведения материала в соотношении 1:10. После отстаивания при комнатной температуре в течение 15 мин 1 см3 приготовленной взвеси высевают на питательные среды.
Определение общего количества микробов (КМАФАнМ), титра БГКП, выявление бактерий родов Salmonella и Proteus проводятся по методике, приведенной в разделе 1.3.
3.3. Выявление коагулазоположительных стафилококков
Из первого разведения колбасных изделий делают посев по методу Дригальского на желточно-солевой агар (ЖСА), содержащий 6,5 % NaСl, для выявления лецитиназной активности коагулазополо- жительных стафилококков. Посевы термостатируют при температуре 37 °С в течение 24 ч. Колонии токсикогенных стафилококков образуют на среде ЖСА «радужный венчик». Из подозрительных колоний готовят мазки и окрашивают их по Граму. Для подтверждения патогенности стафилококков ставят реакцию плазмокоагуляции.
Наличие грамположительных стафилококков, давших положительную реакцию плазмокоагуляции и реакцию на лецитиназу, свидетельствует о присутствии токсикогенных стафилококков.
3.4. Выявление сульфитредуцирующих клостридий
Сульфитредуцирующие клостридии широко распространены в природе, часто обнаруживаются в кишечнике человека и животных. Некоторые штаммы сульфитредуцирующих клостридий (в частности, Clostridium perfringens) могут вызвать у человека кишечные заболевания, характеризующиеся как пищевые токсикоинфекции, механизм действия которых обусловлен наличием у этих микроорганизмов энтеротоксинов.
Clostridium perfringens - грамположительные палочки, располагающиеся поодиночке, попарно или в виде цепочки, неподвижные, in vivo образуют капсулу. Эндоспоры овальные, расположены центрально, субтерминально или на конце клетки. На плотных средах формирует S- и R-колонии; S-колонии круглые, гладкие, с ровными краями, в начале роста, напоминающие капли росы; R-колонии неправильной формы, бугристые, с шероховатыми неровными краями, в глубине агара напоминающие комки ваты.
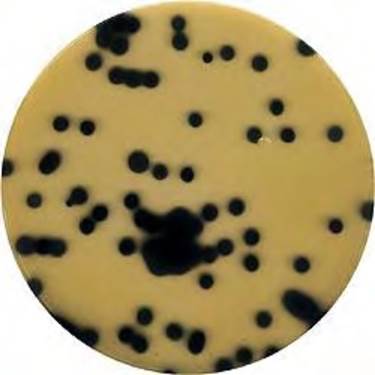
Определение этой группы бактерий основано на учете специфического роста клостридий в средах, содержащих железа сульфит. При взаимодействии натрия сульфита с железа хлоридом образуется железа сульфат, вызывающий почернение среды (рис. 3.1).
Рис. 3.1. Колонии сульфитредуцирующих клостридий на железосульфитной среде
Выявление вегетативных клеток сульфитредуцирующих клостридий в мясных продуктах включает два этапа:
✵ обнаружение сульфитредуцирующей способности микроорганизмов;
✵ определение принадлежности выделенных микроорганизмов к клостридиям.
Сульфитредуцирующую способность микроорганизмов определяют путем посева исследуемого продукта на среду Вильсона- Блера или железосульфитную. Если после инкубации чашек Петри на среде выросли темно-серые или черные колонии, вызвавшие почернение среды, их исследуют на принадлежность к клостридиям. Для этого материал из колоний пересевают в пробирки со средой Китта-Тароцци, инкубируют при температуре 37 °С в течение 24-72 ч. При наличии помутнения среды и выделения газа берут культуру со дна пробирки, готовят микроскопические препараты, окрашивают их по Граму и выявляют наличие спор, определяют каталазную активность. Сульфитредуцирующие клостридии не образуют каталазы.
Для выявления сульфитредуцирующих клостридий в пробирки, содержащие по 9 см3 расплавленной и охлажденной до 45 °С среды Вильсона-Блера, вносят по 1 см3 десятикратных разведений (от 10-1 до 10-7) взвеси исследуемого продукта. Тщательно перемешивают посевной материал, помещают в термостат и культивируют при температуре 46 °С в течение 8-12 ч или при температуре 37 °С в течение 20 ч. Появление на среде черных колоний или почернение среды свидетельствует о присутствии в исследуемом продукте сульфитредуцирующих клостридий.
За положительный титр клостридий принимают то максимальное количество взвеси, в посеве которой произошло почернение среды. Например, если характерные изменения наблюдаются в пробирках с разведением 10-2, то считают, что в 1 г исследуемого продукта содержится 1 x 102 микробных клеток.
В случае отсутствия роста на элективных средах и при наличии роста на средах обогащения посевы из этих сред пересевают в чашки Петри со средой Эндо и инкубируют в термостате с температурой 37 °С в течение 24 ч. В дальнейшем исследование проводят по методике бактериологического исследования мяса.
В табл. 3.1. приведены микробиологические показатели колбасных изделий.
Таблица 3.1. Микробиологические показатели колбасных изделий (ТР ТС 034/2013)
КМА-ФАнМ, |
Масса продукта (г), в которой не допускаются |
Дрожжи и плесени |
||||
Группа продуктов |
КОЕ/г, не более |
БГКП (коли-формы) |
Сульфитредуцирующие клостридии |
S. aureus |
Е. соli |
КОЕ/г |
Колбасные изделия сырокопченые, сыровяленые |
- |
0,1 |
0,01 |
1,0 |
1,0 |
|
Колбасные изделия полукопченые и варено-копченые |
- |
1,0 |
0,01 |
1,0 |
||
Колбасные изделия для детского питания |
1 х 103 |
1,0 |
0,1 |
1,0 |
1,0 |
Др.*- 100 Пл.*- 100 |
Колбасные изделия вареные |
2,5 х 103 |
1,0 |
1,1 |
1,0 |
- |
|
Др. - дрожжи; Пл. - плесени.
Задание по теме:
1. Ознакомиться с методами отбора проб колбасных изделий для проведения бактериологического исследования.
2. Провести определение КМАФАнМ и БГКП в колбасных изделиях.
3. Изучить культуральные и морфологические свойства микроорганизмов, выросших на питательных средах. Описать колонии микроорганизмов, приготовить фиксированные препараты, окрасить их по методу Грама, зарисовать микрокартину.
4. Сделать вывод о доброкачественности исследованных колбасных изделий.
Контрольные вопросы
1. От чего зависит стойкость колбасных изделий при хранении?
2. Как готовят объединенную пробу для микробиологического исследования колбасных изделий?
3. По каким критериям оценивают микробиологическую безопасность колбасных изделий?
4. По каким признакам определяют присутствие в колбасных изделиях сульфитредуцирующих бактерий?
5. Что такое титр БГКП, положительный титр клостридий?
6. Какие признаки характерны для коагулазоположительных стафилококков?