Общая микробиология - Шлегель Г. 1987
Основные механизмы обмена веществ и преобразования энергии
Биосинтез некоторых низкомолекулярных веществ
Биосинтез аминокислот. Большинство микроорганизмов и зеленые растения способны синтезировать de novo все двадцать аминокислот, из которых строятся белки. Углеродные скелеты аминокислот образуются из промежуточных продуктов обмена. Аминогруппы вводятся путем прямого аминирования или трансаминирования. Перевод неорганического азота в органические соединения происходит всегда через аммиак. Нитраты, нитриты и молекулярный азот предварительно восстанавливаются до аммиака (ассимиляционная нитратредукция) и только после этого включаются в состав органических соединений (рис. 7.16, а, б, в).
Лишь немногие из аминокислот образуются в результате прямого аминирования свободными ионами NH4. В первичной ассимиляции аммиака участвуют L-глутаматдегидрогеназа (рис. 7.16, е) и L-аланиндегидрогеназа (ж), которые осуществляют восстановительное аминирование 2-оксокислот; АТР в этом процессе не участвует. Образование глутамина из глутамата катализируется глутаминсинтетазой (г). Этот фермент имеет во много раз большее сродство к ионам аммония (меньшую константу КМ), чем названные дегидрогеназы, и поэтому активен даже при крайне низких концентрациях NH+4; для образования глутамина необходим АТР. С помощью глутаматсинтазы (д) амидная группа глутамина может быть перенесена на 2-оксоглутарат. Эта система включения аммонийного азота в органические соединения у многих бактерий и растений, видимо, создается и используется в тех случаях, когда концентрация ионов аммония в среде очень мала (меньше 1 мМ/л), а также при фиксации N2.
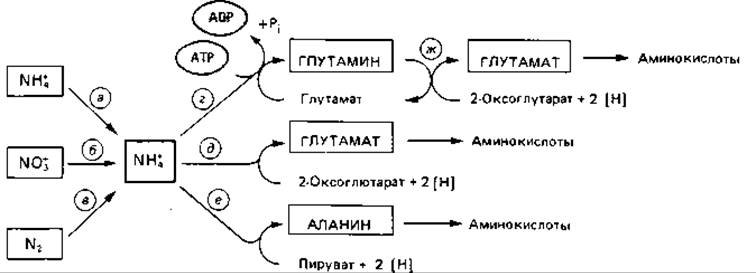
Рис. 7.16. Важнейшие пути ассимиляции азота. Ионы аммония, содержащиеся в питательной среде, непосредственно поглощаются клетками (а). Ионы нитрата при ассимиляционной нитратредукции (б), а молекулярный азот (N2) при фиксации азота (в) восстанавливаются до ионов аммония. В органические соединения аммонийный азот переводится либо при участии АТР путем образования глутамина, либо без затраты АТР путем прямого восстановительного аминирования 2-оксоглутарата или пирувата.
Большинство остальных аминокислот получает свою аминогруппу от одной из первичных аминокислот в результате трансаминирования. Из свободных аминокислот в цитоплазме количественно преобладает глутаминовая кислота (больше половины всего «пула» аминокислот).
У ряда микроорганизмов хорошо изучены пути синтеза всех двадцати аминокислот. Исходным материалом для синтеза служат простые промежуточные продукты обмена (пируват, 2-оксоглутарат, оксалоацетат или фумарат, эритрозо-4-фосфат, рибозо-5-фосфат и АТР). При синтезе большинства аминокислот аминогруппа вводится только на последнем этапе путем трансаминирования. Некоторые аминокислоты образуются в результате ряда превращений других аминокислот, и в этих случаях трансаминирования не требуется. Аминокислоты можно подразделить на группы, исходя из путей их синтеза (рис. 7.17). Синтез различных аминокислот включает разное число этапов, катализируемых ферментами. Примечателен тот факт, что аминокислоты, которые человек должен получать в готовом виде, синтезируются особенно длинным путем.
Относительно быстрое выяснение путей биосинтеза аминокислот и других соединений стало возможным благодаря использованию ауксотрофных мутантов грибов и особенно бактерий. Ауксотрофность многих мутантов обусловлена утратой способности к образованию какого-то фермента, участвующего в биосинтезе. Для роста мутанта нужен в этом случае конечный продукт того пути биосинтеза, который блокирован из-за выпадения функции фермента. Эти мутанты обладают еще одним ценным свойством: они растут не только в присутствии конечного продукта блокированного пути, но и в присутствии промежуточных продуктов, образующихся на отрезке между блокированным этапом и конечным продуктом. В то же время субстрат для блокированной реакции часто накапливается: если, например, отсутствует фермент b, то в среду выделяется промежуточный продукт В:
![]()
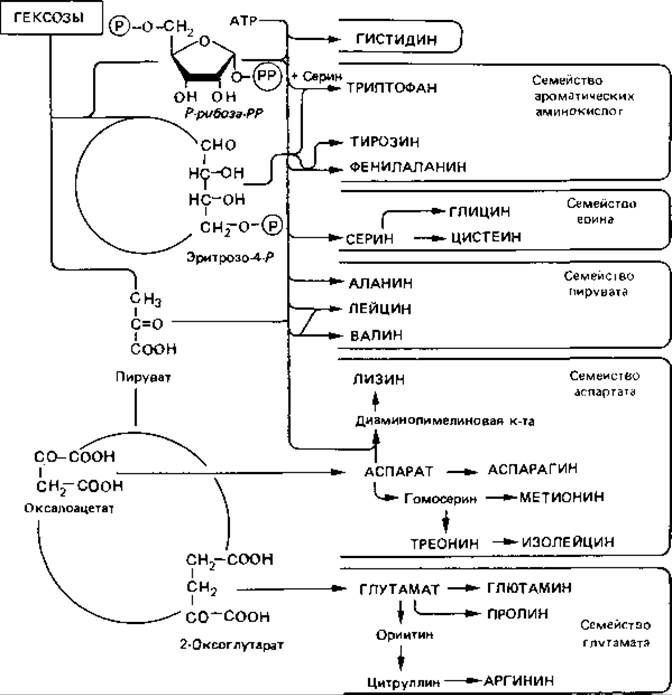
Рис. 7.17. Двадцать аминокислот, необходимых для синтеза белков, образуются из простых соединений - продуктов промежуточного обмена.
Благодаря этому некоторые мутанты, у которых блокированы разные этапы одного и того же пути синтеза, могут снабжать друг друга недостающими веществами. Мутант с блоком на более позднем этапе (отсутствие фермента d) обеспечивает недостающим промежуточным продуктом клетки другого мутанта с блоком на более раннем этапе (отсутствие фермента b). В результате таких опытов удается расположить определенных мутантов в ряд, в котором каждый предшествующий мутант будет поддерживать рост всех следующих за ним. Путем анализа накапливающихся промежуточных продуктов, выделения и очистки ферментов, а также с помощью других методов удалось уже выяснить многие пути биосинтеза.
Биосинтез нуклеотидов. Пуриновые и пиримидиновые нуклеотиды - это те структурные блоки, из которых синтезируются нуклеиновые кислоты; нуклеотиды входят также в состав многих коферментов и участвуют в активации и переносе аминокислот, сахаров, компонентов клеточной стенки и липидов. Синтез всех пуриновых нуклеотидов идет общим путем, разветвляющимся лишь на стадии инозиновой кислоты, после чего образуется либо адениловая, либо гуаниловая кислота. Общим является и путь синтеза пиримидиннуклеотидов. Здесь разделение происходит на уровне уридиловой кислоты.
Исходным соединением для образования пентозного компонента нуклеотидов служит рибозо-5-фосфат. Он может синтезироваться двумя путями: 1) окислительным - из глюкозо-6-фосфата через окислительный пентозофосфатный путь и 2) неокислительным - из фруктозо-6-фосфата и глицеральдегид-3-фосфата в результате реакций, катализируемых трансальдолазой и транскетолазой (разд. 7.2.2). Рибозо-5-фосфат используется для синтеза пуриновых и пиримидиновых нуклеотидов в высокоэнергетической форме-в виде фосфорибозилпирофосфата. Восстановление рибозы до дезоксирибозы происходит на стадии рибонуклеотида и может осуществляться различным образом.
Биосинтез жиров. Жиры и вообще липиды, с одной стороны, являются важными компонентами плазматических мембран и клеточных стенок, а с другой - служат запасными веществами. В бактериальных жирах преобладают жирные кислоты с длинной цепью (С14-С18), насыщенные и ненасыщенные с одной двойной связью. Ненасыщенные жирные кислоты с несколькими двойными связями и стероиды, видимо, отсутствуют; редки также триглицериды. Большое значение имеют сложные липиды. Они представляют собой сложный эфир глицерола, в котором две спиртовые группы этерифицированы жирными кислотами1, а третья - остатком фосфорной кислоты или сахаром. Остаток фосфорной кислоты в свою очередь связан с серином, этаноламином или глицеролом. Такие липиды обнаружены у многих бактерий; к этой группе соединений принадлежат, в частности, фосфатидилинозитол, фосфатидилглицерол и фосфатидилэтаноламин.
1 У архебактерий не обнаружено липидов, содержащих жирные кислоты — Прим. ред.
Жирные кислоты с длинной цепью синтезируются путем конденсации и восстановления ацетатных групп. Для повышения реакционной способности метальная группа ацетилкофермента А сначала карбоксилируется в биотин-зависимой реакции с образованием малонил-СоА:
![]()
В последующих реакциях конденсации карбоксильная группа снова отщепляется в виде СO2. Синтез жирных кислот происходит при участии мультиферментного комплекса согласно уравнению
![]()